皮肤鳞状细胞癌相关差异表达基因及信号通路的生物信息学筛选
任秀玲,张江林,李伟,乔芳
(1.中南大学湘雅公共卫生学院 流行病与卫生统计学系,湖南 长沙 410008;2.中南大学湘雅医院 皮肤科,湖南 长沙 410008;3.中南大学湘雅医院 老年医学科,湖南 长沙 410008)
近年来,随着人类居住环境的日益恶劣,皮肤癌发病率逐年上升,已成为当前一个全球性的公共健康问题。皮肤癌分为恶性黑色素瘤和非黑色素瘤性皮肤癌两大类,其中非黑色素瘤皮肤癌是当前全球人类癌症中最流行的恶性肿瘤之一,约占所有皮肤癌患者的95%,且其发病率呈正逐年增加趋势[1],严重危害人们的身体健康。探讨非黑色素瘤的发病特点,寻找有效的诊治方法具有重要的临床意义。皮肤鳞状细胞癌(cutaneous squamous cell carcinoma,cSCC)是一种常见的非黑色素瘤,尤其在老年人群中更为普遍。cSCC 源于表皮角质形成细胞,恶性程度高,其早期表现不典型,难以诊断,导致临床上大部分患者确诊时往往已形成侵袭性的cSCC,常常转移至其他组织器官,患者的治疗效果不佳,长期预后较差。高度转移的cSCC 患者1 年疾病特异性存活率为44%~56%,区域淋巴结受累的患者10 年生存率降至20%以下,而发生远处转移的患者10 年生存率降至10%以下[1-2],严重危害患者的生命。目前,对这类转移性癌症的治疗方法主要包括化学疗法、靶向疗法和免疫疗法[3-4],不仅会给患者带来严重的副作用,还会产生巨大的经济压力,美国每年因治疗cSCC 的总费用支出超过10 亿美元[5]。因此,进一步探讨cSCC 发病的分子机制,寻找cSCC 的早期诊断生物标志物,改善临床治疗结果具有重要的现实意义。
本研究中,我们利用生物信息学的方法对cSCC 相关基因芯片数据进行整合分析,筛选出cSCC 组织中的差异表达基因,并探讨这些基因的生物学功能及调控网络,以期为解读cSCC 的发病机制提供新的理论依据,为cSCC 的早期诊断和临床治疗提供潜在的生物靶点。
1 材料和方法
1.1 芯片数据的获取
从基因表达综合数据库(Gene Expression Omnibus,GEO)(http://www.ncbi.nlm.nih.gov/geo)中检索并下载cSCC 相关基因芯片数据GSE42677和GSE53462,前者包含13 例cSCC 组织以及10 例正常的皮肤组,后者包含5 例cSCC 组织以及5 例正常皮肤组织。
1.2 差异表达基因的筛选
利用Affy 软件包(http://www.bioconductor.org/packages/release/bioc/html/affy.html)对数据进行预处理和标准化。利用Limma 包(https://bioconductor.org/packages/release/bioc/html/limma.html) 以 |logFC|≥1.5且调整P<0.05 为标准筛选差异基因。
1.3 功能富集分析
利用DAVID(https://david.ncifcrf.gov/)工具包对差异表达基因进行基因本体论(Gene Ontology,GO)和功能富集分析,以P<0.05 为差异有统计学意义。
1.4 蛋白质相互作用网络的构建
利用 STRING 数据库 (https://string-db.org/)分析这些基因的相互作用,结合Cytoscape 软件构建蛋白质相互作用网络,利用MCODE 插件筛选关键模块,利用CytoHubba 插件筛选核心基因。
1.5 数据验证
利用 Oncomine(https://www.oncomine.org/resource/login.html)数据库中的皮肤鳞状细胞癌相关基因表达数据对筛选的差异基因结果进行验证,并生成热图。
2 结果
2.1 差异表达基因的筛选
从GSE42677 芯片数据中共获得2 539 个差异表达基因,包括在肿瘤组织中上调表达的基因1 245 个,下调表达的基因1 294 个(图1A);从GSE53462 芯片数据中共获得375 个差异表达基因,其中肿瘤组织中上调表达的基因112 个,下调表达的基因263 个(图1B)。在这些差异表达基因中,两组芯片共同上调表达基因43 个,共同下调表达基因65 个。
2.2 GO富集分析和KEGG通路分析
低表达的差异基因主要富集在细胞增殖和皮肤发展等生物学过程、轴突和聚合物细胞骨架纤维等细胞组份、跨膜受体蛋白激酶活性和阳离子结合等分子功能。高表达差异基因主要富集在防御反应和先天免疫反应等生物学过程、细胞外区域和细胞外泌体等细胞组份、趋化因子受体结合和细胞因子活性等分子功能。高表达的差异基因主要富集在Toll 样受体信号通路、趋化因子信号通路和癌症中的转录失调等信号通路;低表达的差异基因主要富集在色氨酸代谢、精氨酸和脯氨酸代谢和p53 信号通路。
2.3 蛋白质相互作用分析
将差异表达基因导入STRING 数据库,分析相互作用,利用Cytoscape 3.5.1 软件构建PPI 网络,其中总共包含节点72 个,边146 条(图2)。
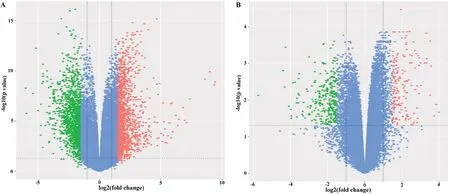
图1 差异表达基因分布火山图

图2 差异表达基因的PPI 相互作用网络
2.4 差异表达关键基因模块分析
利用Cytoscape 软件的MODE 插件进行模块分析,筛选代表性的模块,根据打分高低,获得前三个核心模块。其中核心模块一得分5.185,包含节点28 个,边70 条,节点蛋白分别为KRT6B、S100A7、SERPINB3、CCL27、SPRR2B、KRT23、KRT2、 KRT31、 LYZ、 RRM2、 PI3、 KIT、DEFB4A、 SCEL、 S100A2、 S100A12、 S100A11、CTSL、SPP1、CCL3L3、PLLP、ALOXE3、PLAU、PLAUR、CCND1、CXCL1、CXCL8 和 KRT16,主要富集在外胚层发育、趋性、趋化作用、表皮发育、损伤反应和细胞因子信号通路。核心模块二得分3.75,包含节点9 个,边15 条,节点蛋白分别为 AIM2、OAS1、SG15、IFI6、OASL、CCND1、CXCL8、ISG20 和CYP1B1,主要富集在免疫反应、对病毒的反应和RNA 结合。核心模块三得分3.6,包含节点 26 个,边45 条,节点蛋白分别为CCL27、 LCE2B、 SPRR2B、 ALDH3A2、 CAT、GATA3、 DSC2、 KYNU、 PI3、 TFAP2B、 KIT、LONRF1、 ZBTB16、 AKR1B10、 CD24、 SPRY1、RORA、 NTRK2、 BTC、 GZMB、 PLLP、 DCT、SERPINB1、CLDN7、CCND1 和 CXCL8。
2.5 核心基因的筛选
利用CytoHubba 插件筛选核心基因,算法采用MCC 法,按得分高低获得排名前20 的核心蛋白 分 别 为 CXCL8、 CCND1、 KIT、 PI3、 SPP1、PLAU、 GATA3、 PLAUR、 CDKN2A、 S100A7、KRT16、 CXCL1、 DEFB4A、 ISG15、 KRT2、S100A12、KRT6B、ISG20、OASL 和 IFI6,它们彼此间的相互作用网络如图3 所示,其中包含20 个节点,53 条边。这20 个核心蛋白中,CCND1、KIT、GATA3 和KRT2 四个蛋白在皮肤鳞状细胞癌组织中低表达,其他16 个蛋白均在皮肤鳞状细胞癌组织中高表达,提示异常高表达基因在皮肤鳞状细胞癌的发生发展过程中起着重要作用。
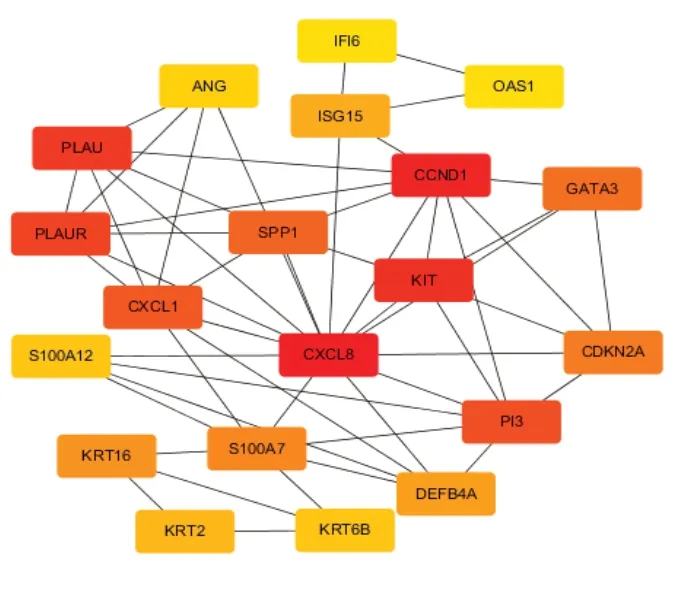
图3 PPI 网络中前20 个Hub 基因相互作用图
2.6 数据验证
为了进一步验证差异表达基因的表达情况,在Oncomine 数据库中检索皮肤鳞状细胞癌相关基因芯片数据,对在GEO 中筛选到的差异表达基因结果进行验证。根据基因表达情况,分别对在肿瘤组织中高表达和低表达的前42 个基因做热图(图4),Oncomine 数据库所得cSCC 相关的差异基因的表达情况与对GEO 数据进行筛选所得结果基本一致,表明本研究的结果具有较好的准确性。
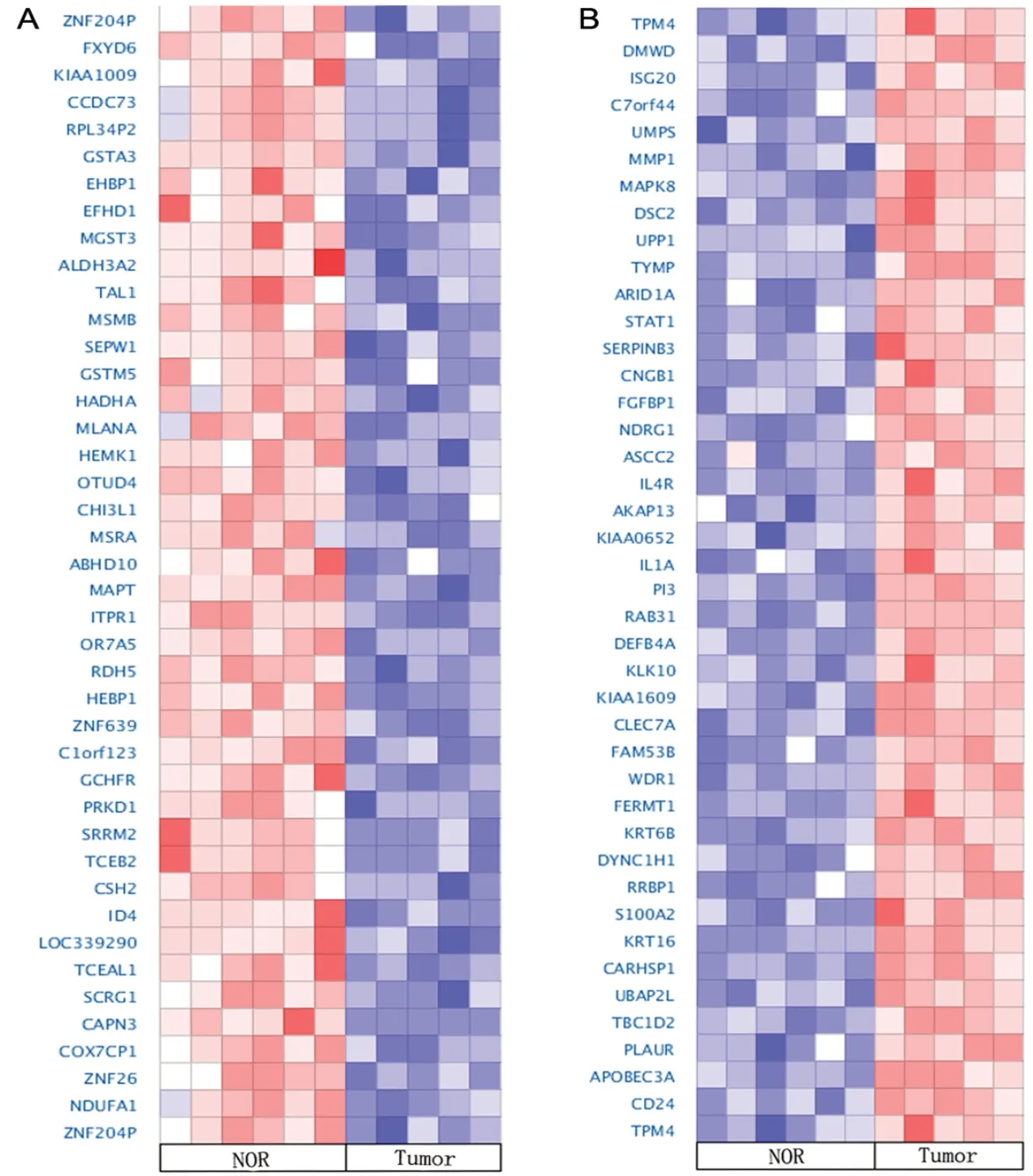
图4 Oncomine 数据库中差异表达基因的验证
3 讨论
在本研究中,笔者通过对GEO 数据库中的基因表达谱数据集GSE42677 和GSE53462 进行深度分析,获得cSCC 肿瘤组织与正常皮肤之间的上调差异表达基因43 个,下调差异表达基因65 个。同时构建了这些差异表达基因之间的相互作用网络,并筛选获得了前20 个关键基因,这些差异表达基因在cSCC 的发生发展过程中很可能起着重要作用。
GO 和全基因组及代谢途径数据库(Kyoto Encyclopedia of Genes and Genomes,KEGG)途径分析发现这些差异表达基因主要富集在细胞增殖、皮肤发育、免疫反应、Toll 样受体信号通路、趋化因子信号通路、精氨酸和脯氨酸代谢和p53 信号通路等功能途径。许多研究表明,机体异常的免疫反应在cSCC 的发生发展过程中起着重要作用,免疫治疗也是当前cSCC 治疗的研究热点[4]。Toll样受体信号通路在天然免疫中扮演重要角色,许多肿瘤细胞表面表达多类Toll 样受体,参与肿瘤的生长转移[6]。TLR4 是Toll 样受体的重要组成部分,作为一种先天免疫受体,其在皮肤、角质形成细胞以及cSCC 中表达,而过表达TLR4 的cSCC细胞的增殖能力减弱,迁移能力增强,体内肿瘤的生长速度减缓[7]。趋化因子受体是一类跨膜蛋白,其介导的通路与多种疾病的发生关系密切,在cSCC 的组织和细胞中,许多趋化因子受体高表达,并参与介导肿瘤的发生发展[8]。精氨酸和脯氨酸代谢对于细胞的生长、增殖起着至关重要的作用,在肿瘤细胞中代谢重编程导致能量下调,需要精氨酸生物合成途径提供能量[9]。p53 是经典的抑癌基因,其基因突变和功能丧失在cSCC 中较为常见,且p53 信号通路与Notch 信号通路之间在cSCC 中存在密切的相互作用,很可能是导致cSCC形成和进展的关键因素[10]。
笔者也通过构建PPI 网络筛选出了20 个在网络中处于核心地位的基因,分别为CXCL8、CCND1、 KIT、 PI3、 SPP1、 PLAU、 GATA3、PLAUR、 CDKN2A、 S100A7、 KRT16、 CXCL1、DEFB4A、 ISG15、 KRT2、 S100A12、 KRT6B、ISG20、OASL和IFI6,这些基因绝大多数都在cSCC 等肿瘤的发生发展过程中扮演重要角色,如:CXCL8 是一种重要的细胞因子,肥大细胞能诱导cSCC 细胞中CXCL8 的表达,参与肿瘤的生长、侵袭和新血管形成[11];CCND1 作为 G1/S-特异性周期蛋白,研究表明约6%的cSCC 患者发生CCND1基因改变,参与肿瘤的发生和进展[12],而CCND1基因的过表达与cSCC 细胞对mTOR 抑制剂抗性密切相关,提示CCND1参与cSCC 的临床耐药[13];SPP1 是一种基质细胞糖蛋白,研究发现其在cSCC 和光化性角化病中显著表达,能保护紫外线暴露下角质细胞的存活,促进cSCC 的发展[14]。当然也有PI3、PLAU等部分基因与cSCC发病的关系目前并不明确,值得笔者进一步深入挖掘和探讨。为了评价笔者筛选结果的准确程度,笔者利用Oncomine 数据库中的cSCC 相关表达谱数据对GEO 中的筛选结果进行验证,发现两者的一致性很好,提示本研究筛选的结果可靠性较高。
总之,本研究中笔者对cSCC 组织与正常皮肤组织芯片数据进行分析,获得了cSCC 相关的关键差异表达基因及生物途径,主要涉及细胞增殖、皮肤发育、氨基酸代谢、免疫反应、Toll 样受体信号通路、趋化因子信号通路和p53 信号通路等生物学过程。笔者的结果可为解读cSCC 的发病机制提供新的实验依据,为cSCC 的诊断及预后评估提供潜在的新生物标记。但是,笔者的结果仅停留于初步的数据分析阶段,鉴于方法学的限制,存在一定的假阳性和假阴性,需要进一步的分子生物学实验进行验证。

