PM2.5通过NF-κB/NLRP3途径促进金黄色葡萄球菌肺炎的研究
黄佳伟,鲁娴娴,崔海燕,张斌,陈鹏,杨少萍,杨旭,李睿,*
1.华中师范大学生命科学学院,武汉 430079 2.华中科技大学同济医学院附属武汉儿童医院,武汉 430016
近年来,频发的雾霾天气使空气污染问题成为公众关注的焦点,而雾霾空气中的细颗粒物(PM2.5),即直径≤2.5 μm的颗粒物,因其含有多种重金属以及多环芳烃等有害物质,且粒径小,可随人的呼吸沉积于支气管和肺泡中,因而可对呼吸系统产生巨大危害[1]。
大量流行病学调查表明,PM2.5与多种呼吸道疾病如哮喘、慢性阻塞性肺疾病(COPD)和肺癌的发生发展具有明显的相关性[2-4]。其中PM2.5与肺炎发生的关系格外引人关注。据报道,空气中PM2.5浓度增加可导致肺炎的住院率增加[5]。李玉荣等[6]进行了合肥市大气污染与肺炎门诊量的时间序列研究,得出PM2.5浓度升高可能引起医院肺炎日门诊量增加。在肺炎中细菌性肺炎最为常见,而其中金黄色葡萄球菌肺炎的致死率高,治疗费用昂贵,且近年来耐甲氧西林金葡菌的出现使得金葡菌感染的治疗和控制越来越难,已给大众健康和社会经济带来严重危害[7]。因此,进行动物学实验探讨PM2.5在细菌性肺炎发生发展中的作用具有重要意义。
动物学实验侧重从分子水平揭示环境污染物诱发相关疾病发病的机制,已有大量实验证明,PM2.5能够引起肺部损伤[8]。核因子κB(NF-κB)是机体产生炎症反应过程中重要的转录因子之一[9],已知包括过量的活性氧(ROS)、缺氧条件和肿瘤坏死因子-α(TNF-α)等多种因素都可活化NF-κB通路[10]。研究表明,PM2.5可以通过增强NF-κB活性使肺部炎症因子生成增多[11]。然而,关于NF-κB通路的上下游分子以及在具体肺炎模型中发挥的作用,仍需要进一步探究。作为目前研究最多的一类炎性小体,NLRP3的表达受到NF-κB的调控[12]。它由病原识别受体NLRP3、接头蛋白ASC和效应蛋白procaspase-1组成[13]。NLRP3被活化后可激活caspase-1,进而促进白细胞介素1(IL-1)家族细胞因子包括白细胞介素1β(IL-1β)、白细胞介素18(IL-18)和白细胞介素33(IL-33)的成熟和分泌,导致组织局部炎性细胞浸润[14]。Rho蛋白A(RhoA)是Rho-GTP酶家族的小分子量G蛋白成员之一,Rho激酶(ROCK)是RhoA的下游目标分子之一[15]。已知RhoA/ROCK通路参与前炎性因子产生过程[16],在炎症发生过程中,RhoA可能充当NF-κB通路上游的调控分子[17]。近期有研究以人肺上皮细胞(BEAS-2B)为材料,证明工业PM2.5可能通过活化RhoA/ROCK通路,进而激活NF-κB引起肺部炎症[18],但仍缺乏体内水平的证据。
本研究以Balb/c小鼠作为实验对象,通过不同浓度的PM2.5暴露,同时建立金黄色葡萄球菌肺炎模型,以探究PM2.5在细菌性肺炎发生发展中的作用以及其中存在的分子机制,为与PM2.5相关的肺炎疾病提供防治基础与依据。
1 材料与方法(Materials and methods)
1.1 实验动物
采用约5周龄的SPF级雄性Balb/c小鼠作为实验动物模型,购自湖北省三峡大学。将小鼠饲养在华中师范大学实验动物管理中心的SPF级环境中,条件为12 h:12 h光/暗周期,温度20~25℃,湿度50%~70%。随时供给小鼠充足的饮水和饲料。适应环境一周后开始实验。
1.2 试剂与仪器
主要实验试剂包括:金黄色葡萄球菌MRSA(StaphylococcusaureusMRSA),购自武汉大学菌种保藏中心;2’,7’-二氯荧光黄双乙酸盐(DCFH-DA-荧光染料,99.9%),购自美国Sigma公司;微量还原型谷胱甘肽(GSH)试剂盒,购自南京建成生物工程研究所;小鼠TNF-α、IL-1β酶连免疫吸附试剂盒,购自美国eBioscience公司;小鼠NF-κB p65、RhoA、ROCK1和NLRP3酶连免疫吸附试剂盒,购自上海源叶生物科技有限公司;ChamQ SYBR qPCR Master Mix、HiScript Ⅱ Q RT SuperMix for qPCR,购自南京诺唯赞生物科技有限公司;Trizol(99%),购自美国Invitrogen公司;氯仿、异丙醇、无水乙醇、液氮、TBA和TCA,均为分析纯,购自国药集团;Mueller-Hinton琼脂和MH肉汤,均购自青岛海博生物技术有限公司。
主要实验仪器包括:空气/智能TSP综合采样器(崂应2050型),细菌摇床(THZ320,武汉大风),恒温培养箱(HP400S,武汉瑞华),超净工作台(SW-CJ-2D型,苏州净化),荧光定量PCR仪(CFX96 Touch,美国BioRad),细胞计数仪(MTN-21,上海精密),荧光酶标仪(FLx800型,美国Bio-Tek),全波长酶标仪(DNM-9602型,北京普朗),低温冷冻离心机(Eppendorf-514R)等。
1.3 PM2.5收集和预处理
PM2.5收集在华中师范大学某建筑物楼顶(高约10 m)进行,采用PM2.5采样器,石英纤维滤膜收集。采样后将含有PM2.5的滤膜裁剪后浸入去离子水中,超声振荡并过滤取滤液于-80 ℃冷冻。过夜后置于冷冻真空干燥机中冻干至粉末状,于-20 ℃保存备用。PM2.5染毒前,用无菌生理盐水配制成相应浓度的悬液。
1.4 PM2.5暴露浓度设置
世界卫生组织(WHO)确定的人日均PM2.5暴露的限值为25 μg·m-3[19],小鼠每日潮气量为0.035 m3,体重按20 g计算,则25×0.035/0.02 ≈ 50 μg·kg-1,因此,确定暴露低浓度为0.05 mg·kg-1,10倍等比往上确定中、高浓度依次为0.5和5 mg·kg-1,高浓度PM2.5(5 mg·kg-1)与相关毒理学实验中的所设置的浓度相当[20]。
1.5 实验分组与暴露方案
将42只Balb/c小鼠随机分成6组,每组7只,分别为:A. 生理盐水对照;B. 5 mg·kg-1PM2.5;C. 肺炎模型;D. 肺炎模型+0.05 mg·kg-1PM2.5;E. 肺炎模型+0.5 mg·kg-1PM2.5;F.肺炎模型+5 mg·kg-1PM2.5。PM2.5采用气道滴注的方式染毒,每天10:00进行,持续7 d。在第7天16:00时进行金黄色葡萄球菌滴鼻,构建肺炎模型。
人们往往是先接触PM2.5再得肺炎,而且考虑到肺炎模型建立后小鼠可能的死亡及传染性,为更好地模拟现实情况,本实验采用先暴露PM2.5再建模的方式进行。
1.6 金黄色葡萄球菌培养与肺炎模型建立
取金黄色葡萄球菌菌株冻存管,用MH琼脂平板复苏,37 ℃过夜培养。挑取单个菌落接种于MH液体培养基,37 ℃、210 r·min-1震荡过夜培养约8 h。离心收集菌体,用生理盐水洗涤并重悬菌体。采用分光光度计检测菌液的OD600,并按照1 OD = 2×109CFU·mL-1计算细菌浓度。最终给每只小鼠滴鼻浓度为5×1010CFU·mL-1的菌液50 μL,分2次进行,间隔30 min。为保持菌液的活性,菌液收集于PM2.5暴露的最后一天,即给小鼠滴鼻接种的当天进行。
1.7 肺组织匀浆制备
在PM2.5暴露周期结束后,即实验的第8天,麻醉小鼠后取肺组织,于PBS(pH 7.5)中漂洗,以去除表面血迹。在滤纸上拭干,称重,加入一定量PBS(pH 7.5),用玻璃匀浆器在冰上制成10%的组织匀浆,将匀浆液离心(10 000 r·min-1、10 min、4 ℃),取上清,将上清液分装后冻存于-80 ℃冰箱,用于指标的测定。
1.8 肺泡灌洗液中菌落计数与炎症细胞计数
采用体全肺灌洗法获得小鼠肺泡灌洗液。小鼠深度麻醉后,剥离气管,气管插管,将生理盐水注入小鼠肺部,回吸液体即为肺泡灌洗液。离心并重悬于0.5 mL生理盐水中,取其中0.1 mL加入0.9 mL生理盐水,即稀释10倍,均匀涂于MH平板上,12 h后进行菌落计数。使用细胞计数仪对剩余0.4 mL重悬液进行各类炎症细胞计数。
1.9 各项生物学指标的测定
用分装好的肺组织匀浆进行各指标的测定。活性氧簇(ROS)含量用DCFH-DA荧光法检测,GSH含量采用GSH试剂盒测定,丙二醛(MDA)采用TCA法检测,TNF-α、IL-1β、NF-κB p65、NLRP3、RhoA和ROCK1均采用ELISA试剂盒检测。所有检测严格按照说明书要求进行。
1.10 肺组织病理学切片制备
肺组织病理切片的制备流程依次包含取材、固定、洗涤脱水、透明、石蜡包埋、切片粘片、脱蜡、染色、脱水、透明和封片等步骤。进行苏木精伊红(HE)和Masson染色,评价小鼠肺组织病理学变化[21]。
1.11 荧光定量PCR
采用TRIzol法提取0.1 g肺组织中的RNA,之后用HiScript Ⅱ Q RT SuperMix for qPCR(Vazyme)试剂盒进行逆转录得到cDNA。最后用ChamQ SYBR qPCR Master Mix(Vazyme)试剂盒并按照其程序进行qPCR检测,考察NF-κB、NLRP3、RhoA、ROCK和β-actin(内参)等基因的表达,基因的引物设计如表1所示。

表1 引物序列Table 1 Primer sequence
1.12 统计分析
实验数据均采用平均值±标准误表示。采用SPSS 13.0软件进行统计学分析。用Graphpad Prism 5.0软件作图。采用单因素方差分析(one-way ANOVA)检验组间均值差异,之后用Tukey-检验进行差异显著性分析。“*”或“#”表示2组之间有显著性差异(P<0.05);“**”或“##”表示2组之间有显著性差异(P<0.01)。
2 结果(Results)
2.1 小鼠体重与脏体比变化
各组小鼠实验期间体重变化如图1所示,对照组小鼠在实验期间体重稳步增长,而经PM2.5暴露的小鼠体重的增长均减缓,5 mg·kg-1PM2.5浓度组小鼠体重甚至呈现下降趋势。而在第7天建立肺炎模型后,各模型组的小鼠体重都明显减小。
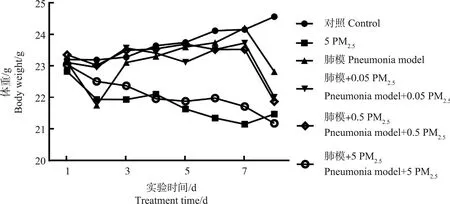
图1 实验期间小鼠体重变化注:1~7 d为PM2.5暴露期,第7天建立肺炎模型,第8天处死小鼠。5 PM2.5、0.5 PM2.5和0.05 PM2.5分别表示5、0.05和0.5 mg·kg-1剂量的PM2.5气道滴注。Fig. 1 Changes in body weight of the mice during the experimentNote: the PM2.5 exposure was from 1 d to 7 d, the pneumonia model was established on the 7th day, and mice were sacrificed on the 8th day. 5 PM2.5, 0.5 PM2.5, and 0.05 PM2.5 represent 5, 0.5 and 0.05 mg·kg-1 doses of PM2.5 airway instillation, respectively.
如图2所示,肺模组、5PM2.5组同对照组相比,小鼠肺脏体比都显著增大(P<0.01),表明肺部可能出现充血或水肿等情况。同时,经金黄色葡萄球菌建模的各组中,随着PM2.5浓度的升高,肺脏体比逐渐增大,且肺模+5PM2.5组与肺模组相比出现显著差异(P<0.01)。这表明高浓度的PM2.5能使肺炎充血现象更加严重,而中低浓度则不明显。

图2 小鼠肺脏体比注:** 表示与对照组相比具有显著差异(P<0.01),## 表示与肺炎模型组相比具有显著差异(P<0.01),下同。Fig. 2 The ratio of lung weight to body weight of miceNote: ** means a significant difference compared with the control group (P<0.01); ## means a significant difference compared with the pneumonia model group (P<0.01). The same below.
2.2 肺泡灌洗液(bronchoalveolar lavage fluid, BALF)菌落计数与炎症细胞计数
为检验金黄色葡萄球菌模型的建立是否成功,在MH平板上进行肺泡灌洗液涂板菌落计数,结果如图3所示。各肺炎模型组(肺膜、肺膜+0.05 PM2.5、肺膜+0.5 PM2.5、肺膜+5 PM2.5)在平板上均长出约1.2×105个菌落,而对照组与5 PM2.5组未长出金黄色葡萄球菌菌落,表明肺炎模型成功建立。
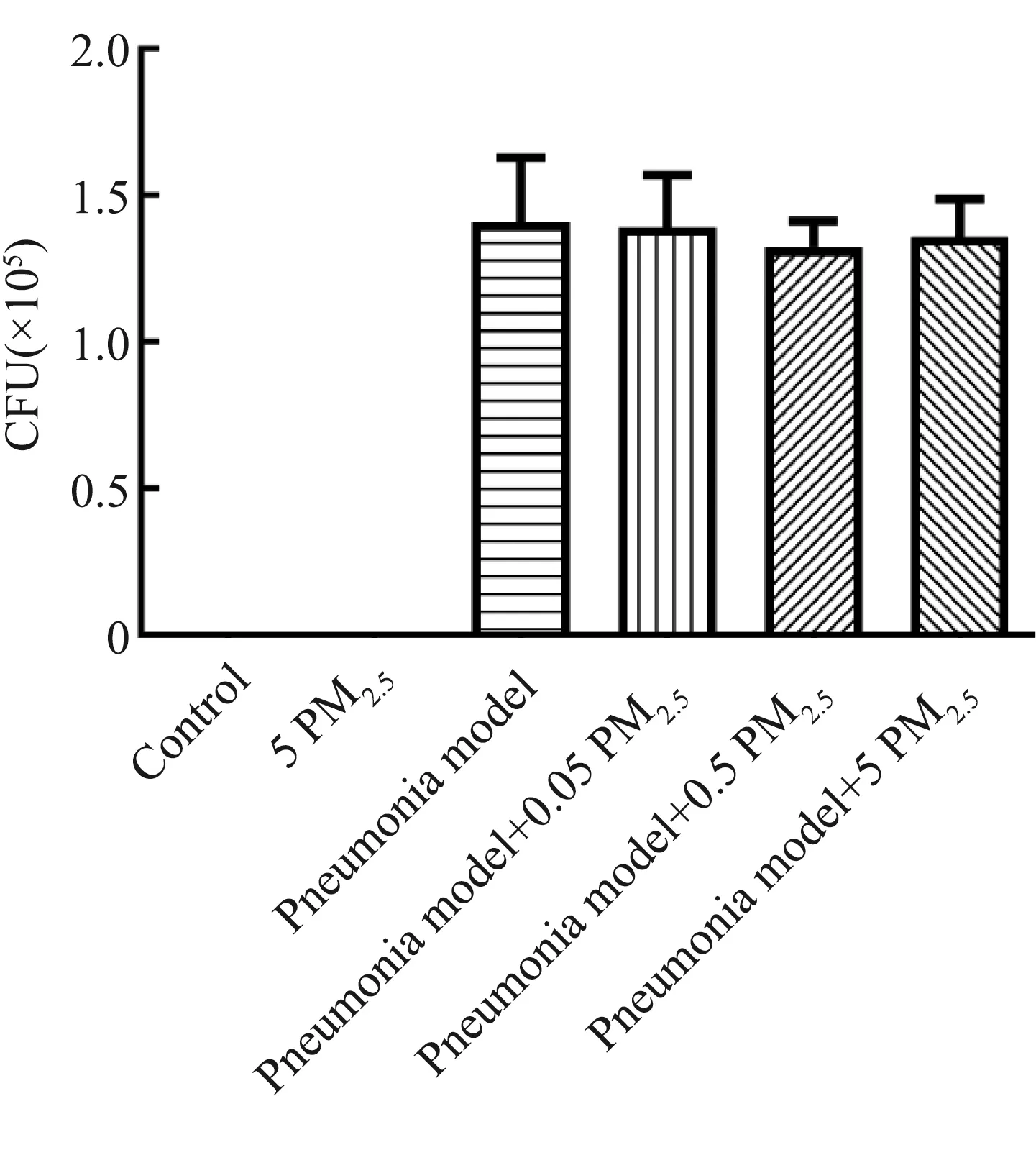
图3 小鼠肺泡灌洗液(BALF)中菌落计数Fig. 3 Colony count in bronchoalveolar lavage fluid (BALF) of mice
各组小鼠BALF中各类炎症细胞数量如图4所示,白细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞数量的变化趋势基本一致,即表现为5 PM2.5组与对照组相比显著增多(P<0.05),而肺炎模型建立后炎症细胞进一步增多。肺模+5 PM2.5较5 PM2.5显著增多(P<0.05),而各肺炎模型组之间并无显著差异。以上结果进一步证明,肺炎模型成功建立,同时经PM2.5暴露染毒使得小鼠肺部炎症细胞增多,发生炎症反应。
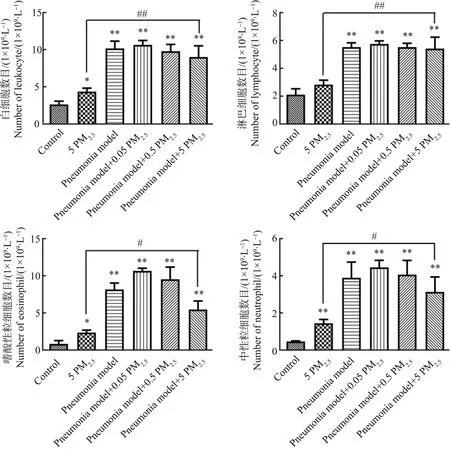
图4 小鼠BALF中炎症细胞数量注:* 表示与对照组相比具有显著差异(P<0.05),# 表示与肺炎模型组相比具有显著差异(P<0.05);下同。Fig. 4 Number of inflammatory cells in BALF of miceNote: * means a significant difference compared with the control group (P<0.05), # means a significant difference compared with the pneumonia model group (P<0.05). The same below.
2.3 病理学染色切片
肺组织HE染色结果如图5所示,与对照组相比,5PM2.5组与肺模组均出现了不同程度的气道重塑现象。而经PM2.5暴露的肺模组中,随着PM2.5浓度的升高,气道重塑现象愈发明显,具体表现为严重的结构变化,包括气道平滑肌增厚并出现向内突起褶皱,气道周围的间质组织中炎症细胞浸润逐渐增多。结果表明,PM2.5不但直接造成肺部损伤,而且进一步恶化肺炎引起的病理效应。
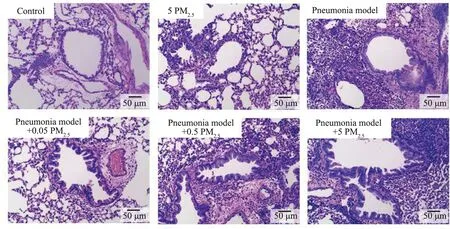
图5 小鼠肺组织HE染色Fig. 5 HE staining of lung tissue of mice
通过Masson染色来检测肺组织纤维化程度,结果如图6所示,在气道重塑方面与HE染色结果呈现类似特征。在各肺炎模型组中伴随着PM2.5暴露浓度的提升,气道周围被染成蓝色的部分逐渐增多,即显示纤维化程度逐渐升高。结果表明,PM2.5能够进一步加重肺组织的纤维化。
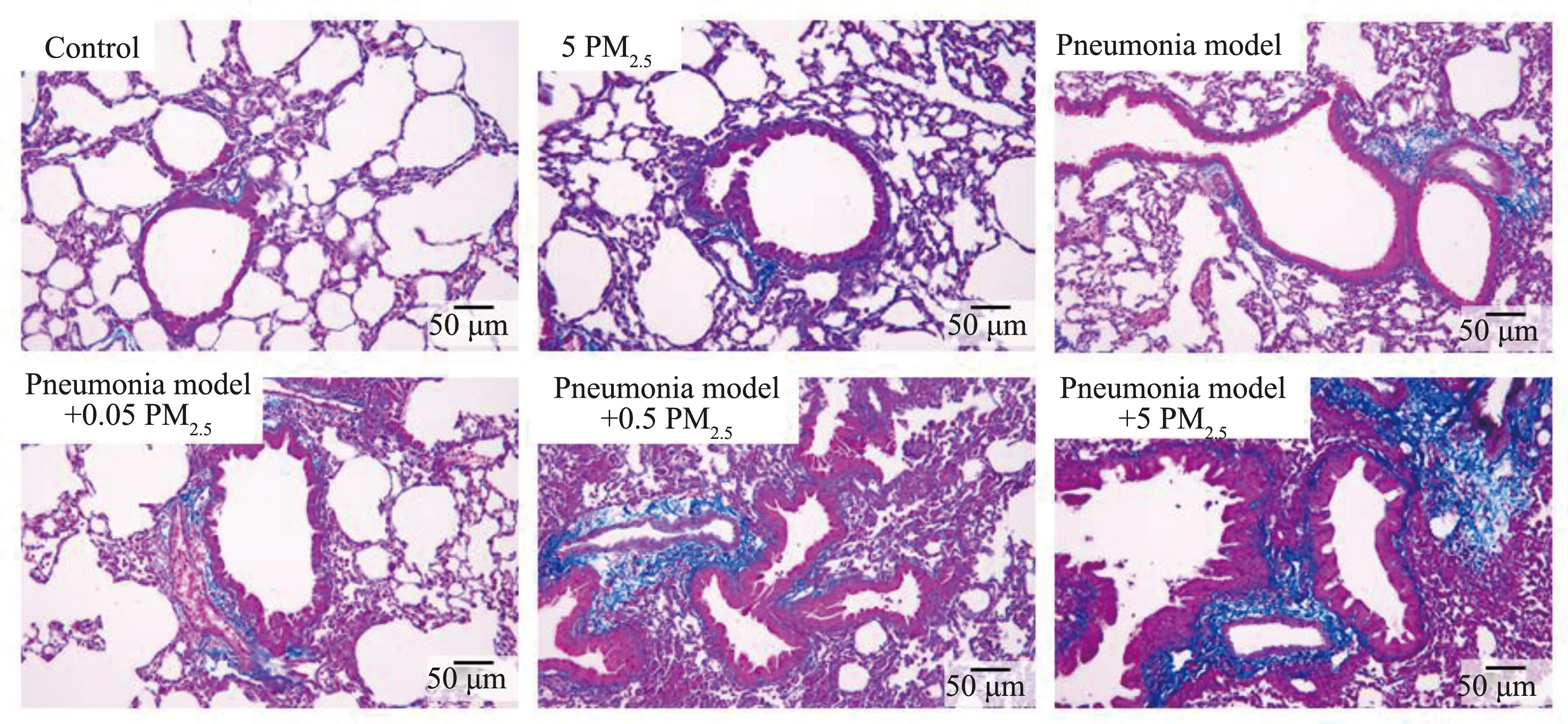
图6 小鼠肺组织Masson染色Fig. 6 Masson staining of lung tissue of mice
2.4 氧化应激水平检测
通过ROS、MDA和GSH等典型指标检验小鼠肺部氧化应激程度。如图7所示,5 PM2.5组与对照组相比,ROS和MDA的含量都显著提高(P<0.05)。同时肺炎模型建立后,随着PM2.5浓度的升高,ROS和MDA的含量呈现逐步上升趋势,且肺模+5 PM2.5组的ROS含量显著高于肺模组(P<0.05)。另一方面,还原性物质GSH的变化趋势正好相反,即PM2.5暴露后GSH含量显著下降(P<0.05);而肺炎模型组中随着PM2.5浓度的提高,GSH含量逐渐减少。以上结果均表明,PM2.5气道滴注能使小鼠肺部发生明显的氧化应激现象,同时也会加剧肺炎过程中出现的氧化损伤。
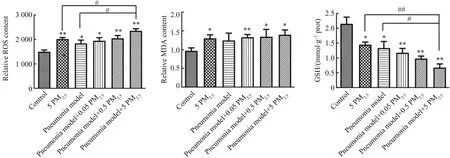
图7 小鼠肺部氧化应激水平注:ROS、MDA和GSH表示活性氧、丙二醛和还原型谷胱甘肽。Fig. 7 Oxidative stress level of mice lungNote: ROS, MDA, and GSH represent reactive oxygen species, malondialdehyde, and reduced glutathione, respectively.
2.5 相关信号蛋白的检测
为探究PM2.5引起肺部损伤并促进肺炎发生的具体机制,对NF-κB、NLRP3、RhoA和ROCK等信号蛋白进行qPCR和ELISA检测,分别从基因和蛋白层面进行探究,结果如图8所示。NF-κB的含量在PM2.5暴露和肺炎模型建立后与对照组相比均显著上升(P<0.05)。同时随着PM2.5浓度的提高,肺炎模型组中的NF-κB含量也逐步提升,而NF-κB的mRNA表达也表现出相同的趋势,进一步印证这一改变。对于NLRP3,PM2.5暴露和肺炎模型建立后都呈现一定的上升趋势,不过只有肺炎模型+5 PM2.5组与对照组比较有显著性差异(P<0.05),相比而言,NLRP3在mRNA层面的改变更为明显。而对于RhoA蛋白及其调控的下游分子ROCK,在PM2.5组和各肺炎模型组中,从mRNA和蛋白水平上均未检测到明显的变化趋势,各组之间均无显著性差异。
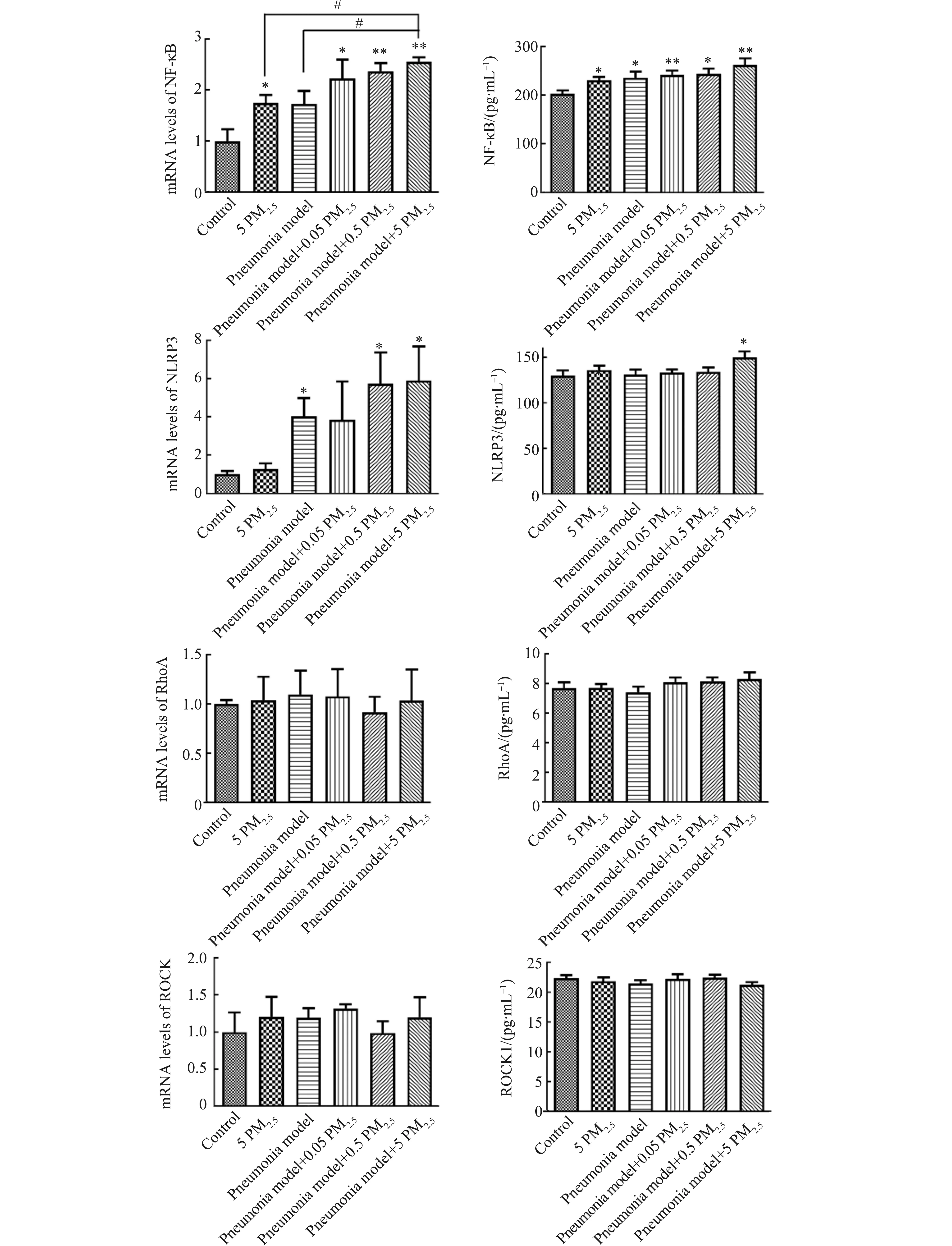
图8 相关信号蛋白的检测Fig. 8 Detection of related signal proteins
通过检测炎症因子IL-1β、TNF-α来反映小鼠肺部炎症水平,结果如图9所示。IL-1β、TNF-α的变化呈现相似的趋势,在5 PM2.5染毒后,二者的含量显著升高(P<0.05),而肺炎模型组与对照组相比显著上升(P<0.05)。另外,在各肺炎模型组中,随着PM2.5浓度的增大,IL-1β和TNF-α的含量都逐步提升,并且肺模+5 PM2.5组与肺模组相比有显著性差异(P<0.05)。以上结果更进一步表明,PM2.5对于肺部炎症的发生起到了明显的促进作用。
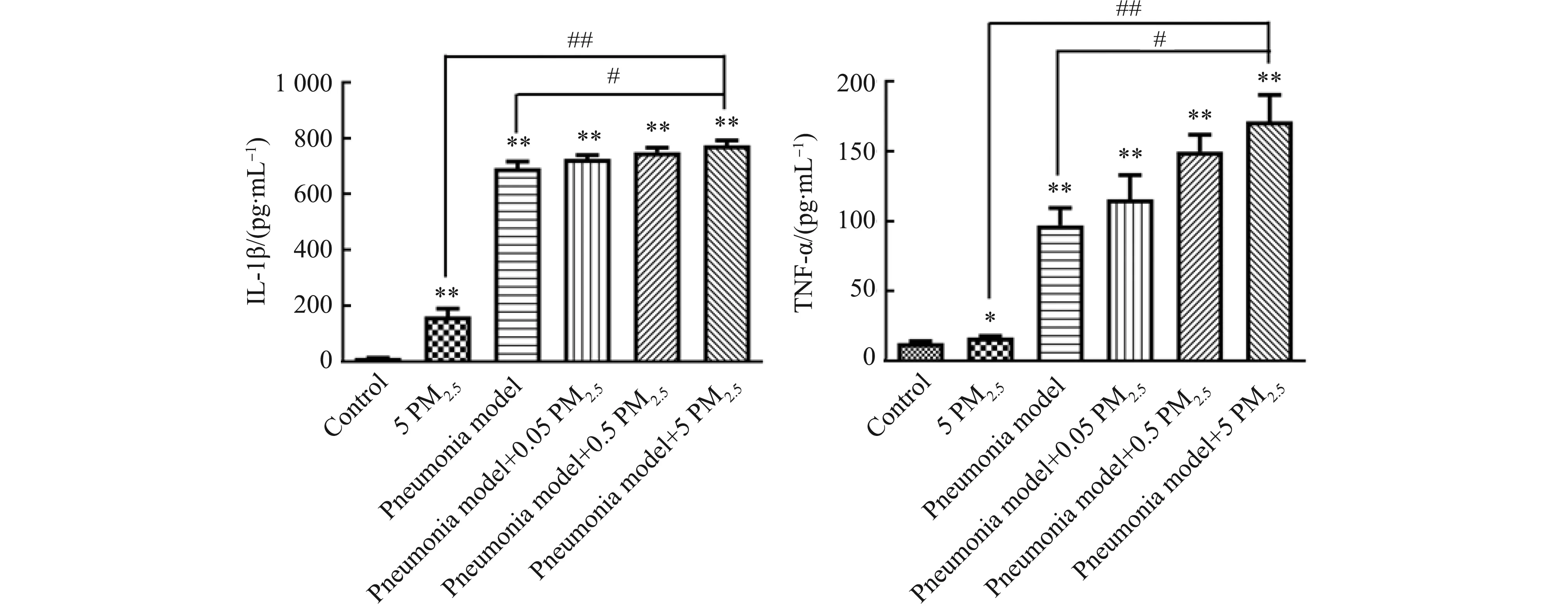
图9 炎症因子检测Fig. 9 Detection of inflammatory factors
3 讨论(Discussion)
3.1 PM2.5引起肺部损伤与加重肺炎的作用
大量研究已经证实,PM2.5急性暴露能够引发机体肺部损伤。本实验选用Balb/c小鼠作为实验动物模型,通过连续7 d进行5 mg·kg-1剂量的PM2.5气道滴注暴露染毒,发现小鼠的体重显著下降,肺脏体比显著升高,提示PM2.5引起肺部充血或水肿。肺泡灌洗液中淋巴细胞、中性粒细胞和嗜酸性粒细胞的数量较生理盐水对照组均显著增多,且炎症因子IL-1β、TNF-α的含量也明显上升,表明PM2.5引起肺部炎症损伤。另一方面,选用耐甲氧西林金黄色葡萄球菌菌株作为病原微生物,采用一次性滴鼻的方式成功构建金黄色葡萄球菌肺炎模型[22]。研究发现,经PM2.5暴露的建模组发生了更为严重的病理反应,且呈现剂量-效应关系,即随着PM2.5浓度从0.05 mg·kg-1增加到5 mg·kg-1,肺炎程度逐步加重。此外,从病理学切片中可以看出,小鼠的肺气道壁逐步增厚并皱缩、气道重塑和炎症细胞浸润现象愈发明显,肺部纤维化程度也逐步加深。
3.2 PM2.5促病的分子机理——NF-κB信号通路
NF-κB是一种广泛存在于真核细胞内,能与多种细胞基因启动子或增强子序列的特定位点结合的核转录因子,它与炎症反应过程的密切相关性已被广泛报道[23]。本研究中,通过qPCR和ELISA的实验发现,在mRNA和蛋白水平上,小鼠NF-κB的含量在PM2.5暴露和肺炎模型建立后与对照组相比均显著上升,同时随着PM2.5暴露浓度的加大,肺炎模型组中NF-κB含量也逐步提升。这表明,在PM2.5导致肺损伤以及加重肺炎的过程中NF-κB被活化,NF-κB信号通路在该过程中发挥重要作用。
3.3 NF-κB被激活的原因
氧化应激是由机体氧化和抗氧化水平失衡引起的[24]。氧化系统中的主要成分ROS会攻击生物膜和亚细胞结构中的不饱和脂肪酸等易被氧化的位置,脂质过氧化过程中产生的MDA会对机体造成巨大损伤[25],而GSH的减少则意味着机体抗氧化系统的减弱,无法发挥清除氧自由基的作用[26]。本研究中发现,小鼠在PM2.5暴露后肺部的ROS、MDA含量显著下降,同时GSH含量显著上升,这表明小鼠肺部出现显著的氧化应激反应。氧化应激刺激可以直接激活NF-κB信号分子,进而诱导下游的炎症反应[27]。
RhoA/ROCK信号通路是体内普遍存在的一条信号转导通路,该信号通路的关键信号分子包括Rho-GTP酶、ROCK和肌球蛋白磷酸酶。其中RhoA是Rho家族的Rho亚族中的一个重要的成员,活化的RhoA可激活其靶蛋白Rho激酶,即ROCK(Rho相关卷曲螺旋形成蛋白激酶)。ROCK接受RhoA传递的活化信号后可介导其下游一系列磷酸化/脱磷酸化反应,进而影响多种细胞效应[28]。研究表明,RhoA/ROCK途径可调节NF-κB从而加剧炎症反应[29]。最近Yan等[18]对人肺上皮细胞进行PM2.5染毒,发现RhoA/ROCK通路被活化,进而激活NF-κB引起肺部炎症。然而在本研究中,发现小鼠在PM2.5暴露和金黄色葡萄球菌肺炎模型建立后RhoA、ROCK的表达水平在mRNA和蛋白层面较对照组均无显著改变。因此,笔者认为在PM2.5加重肺炎的过程中NF-κB的激活主要是由氧化应激介导的,而关于RhoA/ROCK通路在其中发挥的作用则有待进一步探究。
3.4 NF-κB下游分子事件NLRP3
炎症小体是由胞浆内模式识别受体参与组装的多蛋白复合物,是机体免疫系统的重要组成部分,NLRP3炎症小体在机体免疫反应和疾病发生过程中具有重要作用,而NF-κB信号是NLRP3被激活的必要前提[30]。本研究结果表明,在PM2.5加重肺炎过程中,随着NF-κB的激活,NLRP3也随之被活化。而在NLRP3被活化后,又会进一步导致促进细胞凋亡的蛋白Caspase-1和炎症因子IL-1β的表达,从而加剧机体炎症反应[31]。本研究中发现IL-1β的水平在PM2.5暴露后显著提高,进一步证明了NLRP3在此过程中发挥重要调控作用。
本研究结果表明,Balb/c小鼠经5 mg·kg-1PM2.5暴露7 d后小鼠体重明显下降,肺部出现显著病理损伤;更为重要的是,PM2.5暴露对于金黄色葡萄球菌肺炎起到了明显的促进作用,在0.05~5 mg·kg-1范围内呈现剂量-效应关系,加剧气道重塑、炎症细胞浸润以及肺纤维化。PM2.5暴露使肺部出现了氧化应激效应,进而激活NF-κB信号通路,活化炎症小体NLRP3,导致炎症因子TNF-α、IL-1β表达升高,最终恶化了金黄色葡萄球菌肺炎。

