Mirizzi综合征腹腔镜治疗的安全性分析
王晔飞,连凌云
(榆林市第一医院,陕西 榆林,719000)
Mirizzi综合征(Mirizzi syndrome,MS)于1948年根据术中胆道造影被报告以来,因缺乏特异性生化表现及临床症状,目前虽有B超、MRCP、CT、经皮肝穿刺胆道造影、内镜逆行胰胆管造影等先进的影像学诊断技术,使诊断水平大为提高,但由于胆囊三角区反复炎症及局部解剖结构变化,影像学检查显影分辨困难,术前诊断率仍不高,而手术治疗是MS唯一有效的方法,在此情况下传统开腹手术治疗可感知胆囊三角区域结石分布及解剖变化,能更好地保障手术安全[1],然而随着腹腔镜技术在临床的广泛应用及技术的进步,有学者认为,部分MS分型行腹腔镜治疗,逆行分离解剖可更好地显露胆囊三角,有助于手术安全进行[2]。现回顾分析2013年1月至2018年7月我院经腹腔镜探查证实为MS的31例患者的临床资料,以探讨腹腔镜手术治疗MS的安全性。
1 资料与方法
1.1 临床资料 本组31例患者中男12例,女19例;18~86岁,平均(50±16)岁。病程2个月至11年,均伴反复发作的上腹或肩背部疼痛,其中4例伴单纯黄疸;2例除黄疸外,同时伴有高热、寒战。均有右上腹压痛体征,其中9例Murphy征阳性并伴有右上腹局限性腹膜炎,9例除Murphy征阳性及右上腹局限腹膜炎外,同时伴有肝区叩痛。
1.2 生化及影像学资料 11例伴有不同程度的血清胆红素、丙氨酸转氨酶、碱性磷酸酶升高。患者均行腹部B超检查,其中9例提示胆囊结石伴肝内胆管扩张,9例提示胆囊管或颈部嵌顿结石,3例提示胆囊、胆总管结石,10例仅提示胆囊大伴胆囊结石。MRCP检查28例,其中9例提示胆囊颈部嵌顿结石并伴肝总管局部受压变细或肝总管上段增宽,7例提示胆囊管或胆囊颈部结石嵌顿,3例提示胆总管中上段结石,1例胆囊管未显示,8例仅提示胆囊结石。
1.3 病例分型 本文中MS Ⅰ~Ⅳ的分型依据Csendes等[3]提出的标准分型。V型则根据Beltran等[4]提出的胆囊与肠道形成内瘘是否引起肠梗阻分为Va型(无肠梗阻)与Vb型(有肠梗阻)。选用上述分型标准有助于根据瘘口大小选择更加适宜的手术方式,最大可能地保留胆道系统正常的生理解剖,维持正常生理功能,提高患者的生活质量。本文MS分型及相应手术方式见表1。
表1 患者MS分型及相应手术方式
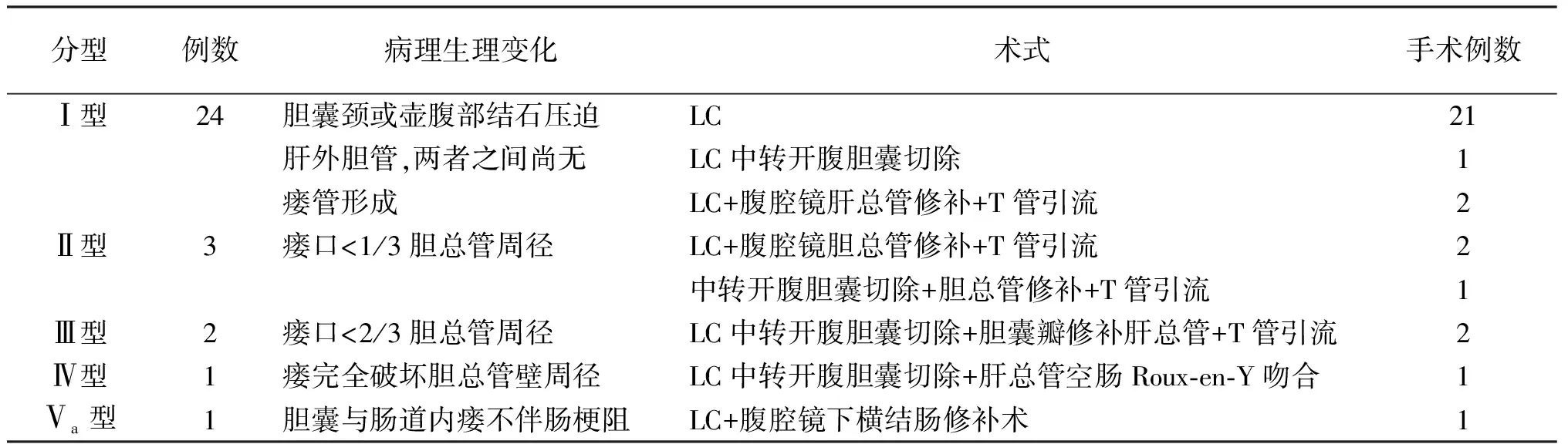
分型例数病理生理变化术式手术例数Ⅰ型24胆囊颈或壶腹部结石压迫LC21肝外胆管,两者之间尚无LC中转开腹胆囊切除1瘘管形成LC+腹腔镜肝总管修补+T管引流2Ⅱ型3瘘口<1/3胆总管周径LC+腹腔镜胆总管修补+T管引流2中转开腹胆囊切除+胆总管修补+T管引流1Ⅲ型2瘘口<2/3胆总管周径LC中转开腹胆囊切除+胆囊瓣修补肝总管+T管引流2Ⅳ型1瘘完全破坏胆总管壁周径LC中转开腹胆囊切除+肝总管空肠Roux-en-Y吻合1Ⅴa型1胆囊与肠道内瘘不伴肠梗阻LC+腹腔镜下横结肠修补术1
注:瘘口均指胆囊管或胆囊颈部结石长期外压胆总管壁后形成的胆囊胆管瘘
1.4 手术方法 采用气管插管静脉复合麻醉,气腹压力维持在10~13 mmHg,开始采用传统三孔法LC,即脐下缘1 cm Trocar为观察孔,剑突下及右锁骨中线与肋缘交汇处1 cm、0.5 cm Trocar为主操作孔与辅操作孔,置入器械,探查腹腔,术中均可见结石嵌顿胆囊颈部或胆囊管,导致胆囊管短缩并推挤邻近肝总管(图1、图2),部分肝总管扭曲,近端胆管扩张(图3),远端胆管正常(图4)。分离显露胆囊前后三角,辨清胆囊管、肝总管及胆总管关系,如果胆囊三角关系清晰,胆囊颈或胆囊管与肝总管有间隙,前后胆囊三角入路会师钝性分离解剖(图5),遵循宁伤胆勿伤管的原则,顺逆结合法切除胆囊。如果胆囊三角区域关系不清(图5),则切开胆囊取出胆囊颈或胆囊管结石,并保留瘘口周围胆囊组织,以便后续修补胆管,同时经瘘口置入胆道镜进一步判断瘘口大小及局部胆管走行,适时选择适宜位置增加Trocar或中转开腹,根据患者情况、瘘口及局部炎症情况选择腹腔镜或开腹胆道单纯修补或胆囊瓣修补+T管引流或开腹Roux-en-Y胆肠吻合术,文氏孔常规留置引流管。
2 结 果
Ⅰ型患者24例,腹腔镜下完成23例,其中21例(87.5%)行LC,手术时间平均(57±15)min,术后平均住院(3.0±0.5)d,2例行LC+腹腔镜下肝总管修补+胆总管探查T管引流,另1例行LC中转开腹胆囊切除;Ⅱ型3例,其中2例行LC+腹腔镜胆总管修补+T管引流,手术时间分别为115 min、155 min,另1例中转开腹行胆囊切除+胆总管修补+T管引流术;Ⅲ型2例,均行LC中转开腹胆囊切除+胆囊瓣修补肝总管+T管引流,手术时间分别为165 min、225 min;Ⅳ型1例,行LC中转开腹胆囊切除+肝总管空肠Roux-en-Y吻合,手术时间155 min;Ⅴa型1例,行LC+腹腔镜下横结肠修补术,手术时间75 min。1例患者术后第5天出现胆漏,予以再次腹腔镜胆漏修补及置管引流治疗康复;1例术后出现肺部感染,积极抗感染治疗后康复;2例Ⅰ型患者术中胆总管侧壁出现胆漏,予以术中缝合并留置T管引流;2例术后出现切口感染,换药后康复;无死亡病例。7例患者带T管出院,术后2~3个月行T管造影,无异常后拔除,留置T管的中位时间为61.15(43~95)d。随访至今,患者均无胆管狭窄表现。
3 讨 论
3.1 MS的病理生理 MS也称肝管综合征,是指胆囊结石或其他良性病变持续嵌顿于胆囊管或胆囊颈部,造成邻近肝总管或胆总管受压梗阻,引起反复发生的胆囊炎、胆管炎、胆绞痛、梗阻性黄疸及严重的胆囊胆管瘘等。Didlake等[5]研究发现,胆囊管开口过低或平行于肝总管,或相邻两管壁间缺如,或仅间隔一层纤薄的纤维膜是本病发生的解剖学基础,本病与胆道解剖变异密切相关,因此又称解剖功能综合征。

图1 结石压迫邻近肝总管 图2 胆囊管缩短变粗(箭头所示)
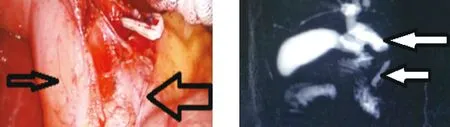
图3 近端扩张的肝总管(大箭头为肝总管,小箭头为胆囊管) 图4 大箭头为肝总管,小箭头为胆总管
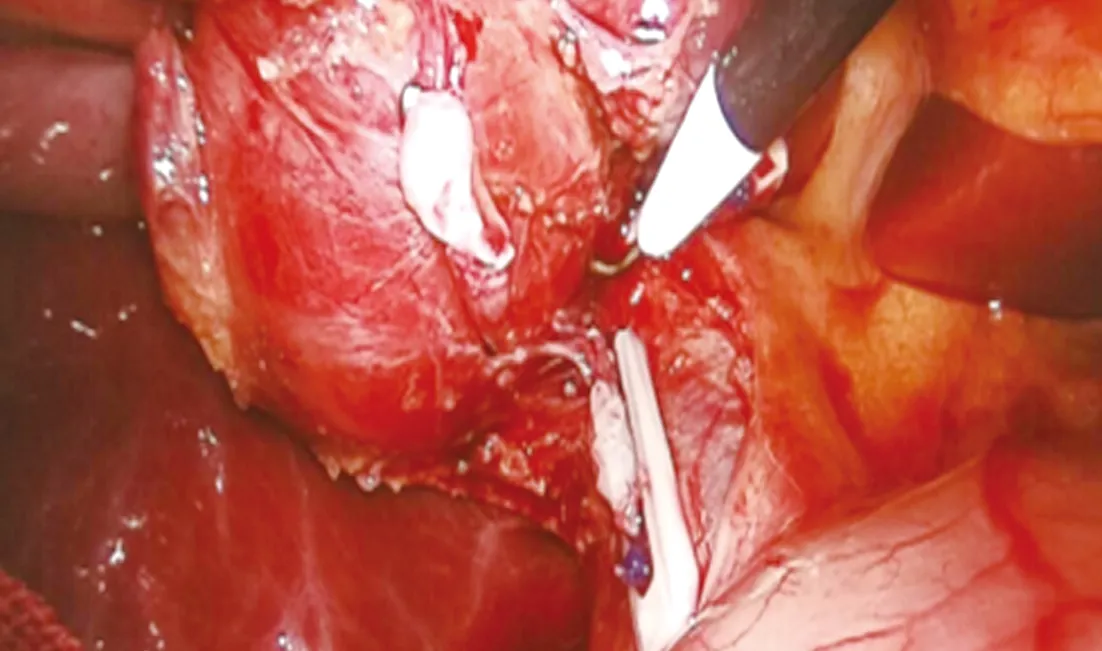
图5 前后三角入路解剖离断胆囊管,钛夹所示为胆囊管
3.2 MS临床辅助检查 临床上MS的发生率较低,为0.7%~1.4%[6],文献报道,术前明确诊断率仅为27%[7],而术前未确诊者胆道系统损伤高达17%[8],造成患者与医生的“双重灾难”。MS缺乏特异性临床表现,术前明确诊断主要依靠影像学检查。由于B超对胆囊结石及其部位、肝总管及胆总管扩张诊断敏感,是胆道系统首选检查项目,文献报道,对MS确诊率约为27%[9],初筛可疑病例进一步结合其他检查可较好地提高术前诊断率,本文回顾分析发现31例MS中B超结合MRCP检查术前确诊率可提高至35%,体现了这一联合应用的益处。CT检查不能很好地显示胆道系统,仅在排除肝胆胰占位性病变时有参考价值。内镜逆行胰胆管造影的确诊率可达55%~90%[10],同时可行取石、引流等治疗,优势明显,但内镜逆行胰胆管造影的技术要求及其导致的胆道感染、创伤性胰腺炎、肠道出血穿孔等风险,限制了临床常规应用,仅在有条件的医疗中心开展。MRCP则在胆道系统中利用重T2加权技术,使含水样组织的胆管在周围组织中信号突出,表现为高信号,而胆道系统的结石缺失氢离子则表现为低信号,明显的信号差使得结石在胆道系统中更明显,得到类似于ERCP的影像效果,而且其无创、可重复操作及临床应用普及,目前认为MRCP是诊断MS最佳的无创检查。本研究发现,结合分析患者B超及MRCP检查结果,尤其B超发现胆囊大、胆囊充满结石、胆囊颈部结石、肝内胆管扩张、肝总管扩张,结合MRCP定位结石,发现胆囊管以上胆管扩张,胆囊颈部或胆囊管结石及结石以下正常胆管(图4),即可确诊MS,对提高术前诊断意义重大。当然B超发现临床典型的“三管征”,即扩张的胆囊管、肝总管及门静脉也可确诊本病,但本研究中无一例发现。
3.3 MS手术方式的选择 首选手术治疗,开腹及腹腔镜治疗遵循的手术原则均为切除病变胆囊,取净结石,解除梗阻,修补瘘口,通畅引流胆汁,尽可能保留乳头功能。遵循以上原则,针对MS不同的病理分型,根据具体情况选择适宜的手术方式,保障手术安全。目前随着腔镜技术在临床中的普及、肝胆外科医师对MS认识的加深,腹腔镜治疗Ⅰ型MS总体是安全、有效的,而且住院时间短、康复快[11]。本组24例中成功施行21例,占总体Ⅰ型病例的87.5%。对于胆囊三角区域炎症纤维化明显,分离困难的患者,为避免副损伤,应及时中转开腹行胆囊大部切除,残余胆囊黏膜烧灼处理。Ⅱ型、Ⅲ型根据瘘口大小,可选择直接缝合或使用胆囊瓣[12]、脐静脉瓣[12]、胃瓣[13]修补,恢复胆道完整通畅,尽可能保留乳头正常生理功能,提升患者生活质量,为预防瘘口狭窄可切开瘘口下段正常胆管,放置T管引流,并且T管引流应留置足够时间。Ⅳ型患者胆总管周径几乎全部缺损,需行胆肠吻合术。Ⅴ型伴有胆肠内瘘,明显增加了手术的处理难度。对于Ⅴa型(胆肠内瘘不伴结石性肠梗阻),通常选用可吸收线缝合胃、十二指肠、小肠或结肠瘘口,视情况行胆囊全切或次全切除术[14]。结合本文病例,采用腹腔镜即是治疗方式同时也是诊断方法。本研究中绝大部分Ⅰ型及部分Ⅱ、Ⅴa型在腔镜下顺利完成,但微创不应作为衡量手术成功的标志,及时中转开腹保证患者安全是手术的根基。Ⅲ型、Ⅳ型解剖复杂,开腹手术相对安全[15]。
结合临床及生化检查结果,同时多种影像学联合检查可提高对MS的术前诊断[16],结合病史及腹腔镜探查情况选择适宜的手术方式,是MS手术治疗安全防范的积极措施。相信随着3D腹腔镜及胆道荧光显像技术的创新应用,腹腔镜在部分MS治疗中是安全、可行的[17]。

