右美托咪定对腹腔镜全子宫切除术患者早期
池成妹,马玉峰,李希明
(1.青岛大学,山东 青岛,266071;2.临沂市中心医院;3.临沂市人民医院)
全子宫切除术为妇科常见手术,随着医学内镜技术的不断发展,腹腔镜逐渐在子宫切除术中得到广泛应用,并具有创伤小、术后康复快、并发症少等优点[1],是目前常用的手术方式。研究表明,女性切除子宫后容易出现强烈失落感,产生焦虑、抑郁情绪[2]及早期认知功能障碍等并发症[3],不利于术后康复及生活质量的提高。术后认知功能障碍(post operative cognitive dysfunction,POCD)是麻醉手术后较常见的中枢神经系统并发症[4],包括精神错乱、焦虑、睡眠障碍、性格改变、社交能力及记忆受损等[5]。围术期神经认知障碍包括术后谵妄、POCD[6],术前或术中尽早干预,可预防术后早期发生的认知功能改变,改善预后,加速术后快速康复,是临床医生需关注的重要内容之一。右美托咪定(dexmedetomidine,DEX)是新型的高选择性α2-肾上腺素受体激动剂,有镇静、镇痛、抑制交感、抗焦虑、稳定血流动力学等作用[7],可减少急性术后谵妄[8],在一定程度上抑制炎症因子释放[9]。本文现探讨DEX对腹腔镜下全子宫切除术患者早期认知功能的影响,将体会报道如下。
1 资料与方法
1.1 临床资料 随机选择2017年12月至2018年6月临沂市中心医院择期行腹腔镜下全子宫切除术的60例患者;45~60岁,ASAⅠ~Ⅱ级。随机分为对照组与DEX组(观察组),每组30例。纳入标准:(1)子宫肌瘤、子宫腺肌病等良性病变;(2)美国麻醉医师协会(ASA)分级为Ⅰ级、Ⅱ级;(3)患者临床症状严重经保守治疗无效,无生育要求;(4)近期未服用激素类药物;(5)患者能配合临床诊疗操作;(6)经过临床诊断、B超、影像学或实验室检查等确诊为子宫肌瘤;(7)患者和(或)家属知情同意,签署知情同意书。排除标准:(1)妇科恶性肿瘤;(2)近期有急性炎症反应;(3)合并严重盆腔粘连无法进行腹腔镜操作;(4)严重心脑血管、呼吸系统疾病,糖尿病、高血压、精神神经疾病、中枢神经系统或心理疾病,身体重要脏器疾患不能耐受手术、麻醉;(5)长期服用镇静、镇痛药或抗抑郁药,窦性心动过缓或房室传导阻滞;(6)对麻醉药物成分过敏,有酗酒、吸毒史;(7)有精神疾患不能配合手术与检查,严重的听力或视觉障碍,简易精神状态评价量表(mini-mental state examination,MMSE)评分低于23分;(8)有出血倾向。本研究获得医院伦理委员会批准,患者与家属均签署知情同意书。
1.2 麻醉方法 两组术前均禁食8 h,禁饮6 h,无术前用药,进行术前访视。患者入手术室后开放外周静脉通路,予以心电监护、脉搏血氧饱和度、呼吸末二氧化碳分压、脑电双频指数监测,桡动脉穿刺置管监测有创动脉压,右颈内静脉穿刺置管监测中心静脉压。麻醉诱导采用咪达唑仑0.05~0.10 mg/kg、依托咪酯0.2~0.4 mg/kg、舒芬太尼0.4~0.6 μg/kg及罗库溴铵注射液0.6~1 mg/kg静脉给药,行气管插管后机械通气,潮气量为8~10 mL/kg,调整吸氧体积分数0.50,吸呼比为1.0∶(1.5~2.0),呼吸频率为10~15次/min,维持呼吸末二氧化碳分压为35~45 mmHg。观察组于麻醉诱导前15 min静脉缓慢泵注DEX(负荷剂量1.0 μg/kg,泵注时间15 min,然后以0.5 μg/(kg·h)持续泵入,手术结束前30 min停药,其维持的输注速率根据心率、血压等变化随时调整。对照组在同等条件下相应时间泵注等量生理盐水,手术完毕停用麻醉药物。麻醉维持:静脉维持输注丙泊酚4~10 mg/(kg·h)、瑞芬太尼0.05~0.20 μg/(kg·min),根据需要间断静脉推注罗库溴铵注射液0.2 mg/kg维持肌松,根据需要追加舒芬太尼,术中根据血流动力学变化,相应予以血管活性药物,以维持血液动力学稳定。将脑电双频指数维持在40~60。术后患者送麻醉恢复室继续观察至麻醉苏醒,术后采用自控静脉镇痛,药物为舒芬太尼2 μg/kg+昂丹司琼8 mg+生理盐水,稀释至200 mL。
1.3 血清中肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)浓度的检测 分别于术前1 d(T0)及术后第1天(T1)、第2天(T2)、第3天(T3)采集两组患者外周静脉血5 mL,置于促凝管中,3 000 r/min离心10 min,分离血清,采用酶联免疫吸附试验法分别测定血清中TNF-α的浓度,操作均严格按试剂盒说明书进行操作。
1.4 认知功能的评价 分别于术前1 d(T0)及术后第1天(T1)、第2天(T2)、第3天(T3)采用MMSE对两组患者进行认知功能测试,由固定且经过专门训练的医师执行,MMSE评分标准:28~30分为认知正常;24~27分为轻度认知功能障碍;19~23分为中度认知功能障碍;0~18分为重度认知功能障碍。计算并比较两组术后3 d的认知功能障碍发生率。POCD的判断采用国际POCD小组推荐的Z计分法:患者术前、术后得分的变化值减去对照组变化值的均数,然后除以对照组变化值的标准差,即为该患者的Z计分,如果Z计分绝对值≥1.96,则可认为出现POCD。术前、术后测试时间、地点及测试人员保持一致,以减少干扰因素。

2 结 果
2.1 两组患者一般资料的比较 两组患者一般资料包括ASA分级、手术时间、补液量、尿量、失血量等差异均无统计学意义(P>0.05)。见表1。


组别年龄(岁)身高(cm)体重(kg)ASA分级(n)ⅠⅡ级手术时间(min)补液量(mL)尿量(mL)失血量(mL)对照组52.5±2.4161±561.2±6.581218123±202 260±250358±52118.5±16.3观察组51.4±3.1162±360.6±5.341416118±192 180±310352±65124.3±16.7 t/χ2值1.4921.2460.3894.01.0971.1000.4311.373P值0.1410.2180.6990.2610.2770.2760.6680.175
2.2 两组患者麻醉药物使用情况的比较 与对照组相比,观察组舒芬太尼、瑞芬太尼等阿片类镇痛药用量降低,丙泊酚用量低于对照组,差异有统计学意义(P<0.05)。见表2。

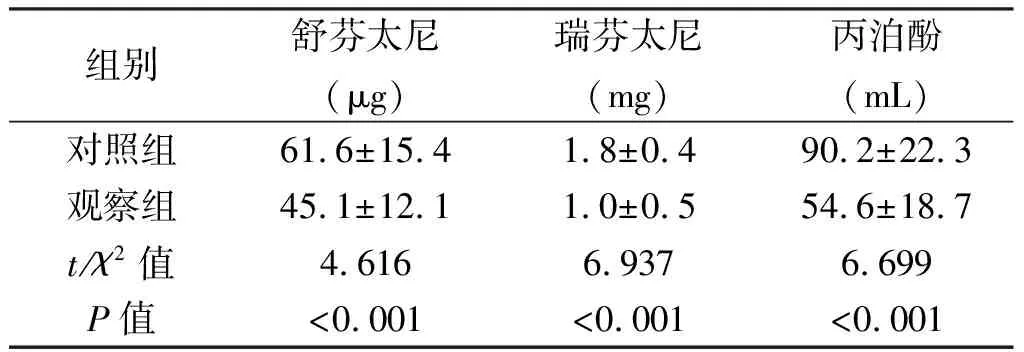
组别舒芬太尼(μg)瑞芬太尼(mg)丙泊酚(mL)对照组61.6±15.41.8±0.490.2±22.3观察组45.1±12.11.0±0.554.6±18.7t/χ2值4.6166.9376.699P值<0.001<0.001<0.001
2.3 两组患者不同时点血清TNF-α水平的比较 T0时,两组患者TNF-α水平差异无统计学意义(P>0.05);与T0相比,T1~T3时两组患者血清TNF-α水平均提高,差异有统计学意义(P<0.05);与对照组相比,观察组血清TNF-α水平降低明显,差异均有统计学意义(P<0.05),而且不同干预措施与不同时点间,TNF-α浓度有交互效应(F=167.5,P<0.05)。见表3、图1。
2.4 两组MMSE评分及POCD发生率的比较 患者均完成MMSE测试。T0时,两组患者MMSE评分差异无统计学意义(P>0.05);与T0相比,T1~T3时两组患者MMSE评分均降低,差异有统计学意义(P<0.05;与对照组相比,观察组MMSE评分较高,差异有统计学意义(P<0.05);不同干预措施与不同时点MMSE评分之间有交互效应(F=126.516,P<0.05)。见表4。对照组11例发生POCD,发生率36.67%;观察组4例发生POCD,发生率13.33%,两组相比差异有统计学意义(P<0.05)。


组别T0T1T2T3F值P值对照组6.42±1.2616.52±1.09∗13.25±1.56∗11.23±1.61∗组内=3373.2<0.001观察组6.36±1.3212.97±1.22∗,#10.17±1.18∗,#9.26±1.23∗,#组间=167.5<0.001t值0.18111.8598.5795.343P值0.857<0.001<0.001<0.001
*P<0.05 vs. T0;#P<0.05 vs.对照组


组别 T0T1T2T3F值P值对照组28.4±0.622.6±0.7∗23.2±0.5∗24.3±0.6∗组内=2200.234<0.001观察组28.3±0.724.8±0.5∗,#25.0±0.6∗,#26.2±0.7∗,#组间=126.516<0.001t值0.20213.99111.84110.439P值0.84<0.001<0.001<0.001
*P<0.05 vs. T0;#P<0.05 vs.对照组
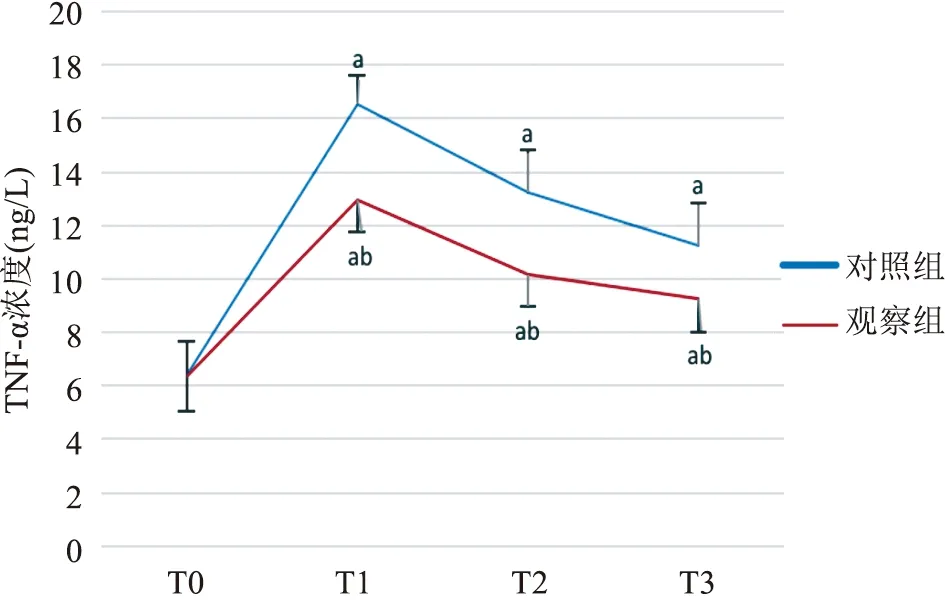
图1 TNF-α浓度趋势图
2.5 不良反应 与生理盐水对照组相比,DEX组患者未出现明显的过敏反应、高血压、心率过缓及心律失常等。
3 讨 论
目前,术后认知越来越成为一个重要的研究领域,麻醉、术后认知功能改变与一般人群的神经认知障碍保持一致,属于围术期神经认知障碍,包括术前已存在的认知功能改变、术后谵妄、神经认知恢复延迟、术后轻度神经认知障碍、术后重度神经认知障碍。POCD的发生机制尚未明确,发生的可能机制包括神经炎性反应学说、神经递质学说、基因学说及淀粉样蛋白学说等,POCD可由多种因素引起,包括患者年龄、麻醉、手术、术后疼痛等,越来越多的证据显示其发病机制与中枢炎症机制关系密切[10],POCD评定没有统一标准,本研究采用传统的认知功能评价量表MMSE评估患者认知功能。
DEX是一种选择性α2-肾上腺素受体激动剂,能抑制应激反应,提供围术期镇痛与镇静,减少麻醉药物的用量,减少术后谵妄及认知功能障碍的发生,通过降低TNF-α水平,减少炎性因子的产生、抑制细胞外调节蛋白激酶,产生一定的保护作用[7]。Peng等[11]发现高剂量的DEX通过减少TNF-α的释放,抑制炎性反应产生,发挥对脑胶质细胞神经保护作用。陈洁娟等[12]的研究发现,DEX能改善全麻患者术后认知功能,降低认知功能障碍发生率。研究表明[13],全麻诱导前予以DEX有助于降低POCD发生率。徐惠平[14]的研究发现,中高剂量DEX对防治POCD更有效,其机制可能与抑制炎症反应水平有关。
TNF-α是一种由单核巨噬细胞所分泌的介导炎性反应的细胞因子,是机体损伤期间反应较早的炎性介质,手术创伤可直接引起TNF-α合成及释放明显增加,引起机体全身炎性反应,而TNF-α可直接或间接透过血脑屏障,激活中枢神经系统中的小胶质细胞,分泌活性氧、炎症细胞因子及趋化因子等,加重炎症反应,抑制海马区的神经元功能,产生认知功能障碍。有动物实验提示[15],海马区的炎性因子表达增高可导致海马区细胞损害,促使其产生POCD。Wang等[16]的研究显示,参与老年大鼠POCD发病机制的海马区小胶质细胞是通过TLR4途径激活的,活化后的小胶质细胞增加了促炎因子TNF-α的表达。
DEX促进了抗炎细胞因子的激活,使机体产生适度的免疫应答,减少了神经元的炎症反应,从而对POCD的发生起到一定的干预作用[17]。曹福羊等[18]发现,DEX可减轻患者术后早期的炎症反应,减少POCD的发生。近期研究发现[19],POCD观察组不同时点TNF-α水平显著高于非POCD观察组,表明POCD的发生与TNF-α水平相关,与本研究结果一致。刘芳等[20]的研究也证实了DEX能降低患者POCD发生率,其机制与降低围术期炎性因子水平有关。
本研究选择于麻醉诱导前泵注DEX负荷剂量1.0 μg/kg,泵注时间15 min,维持0.5 μg/(kg·h),至术毕前30 min。结果显示,与对照组相比,观察组舒芬太尼、瑞芬太尼、丙泊酚用量减少,其机制与DEX具有镇痛、镇静作用有关[7];与术前相比,两组患者术后1~3 d的血清TNF-α水平均显著升高,MMSE评分降低,表明手术与麻醉创伤已引起了患者的机体炎症反应,导致POCD的发生。MMSE进行认知测试结果表明,对照组与观察组术后3 d神经认知功能改变的发生率分别为36.67%与13.33%,术后3 d内观察组POCD发生率低于对照组,从而表明DEX可有效降低术后早期神经认知功能改变的发生率;与对照组相比,术后1~3 d患者血清TNF-α水平均明显降低,表明DEX能下调患者血清TNF-α水平表达,减轻腹腔镜下子宫切除术与麻醉所引起的炎性反应。从而推断DEX能降低腹腔镜下全子宫切除术患者围术期神经认知障碍的发生率,可能与抑制机体炎症反应、下调TNF-α的水平表达有关。
综上所述,DEX能下调围术期血清中炎性细胞因子TNF-α的水平表达,降低腹腔镜下全子宫切除术患者术后早期认知功能改变的发生率,改善预后,加速术后快速康复。

