一步法合成特异性pH响应碳量子点及其发光机理研究
高 东,张煜亮,孙 静,范宏筠
(1.四川轻化工大学 生物工程学院,自贡 643000;2.四川大学 生物材料工程研究中心,成都 610041;3.成都盛讯科技有限公司,成都 610061)
碳量子点作为一类新兴的荧光纳米材料,引起了人们的广泛关注和兴趣。由于其优异的荧光性能(如可调荧光、光学稳定性)[1-4],低细胞毒性[5],良好的生物相容性和溶解性(水相和有机相)[6-8],易于制备和表面改性等特点[9],碳量子点在生物成像、荧光传感、光催化和光电装置等领域展现出诱人的应用潜力[7,10]。
碳量子点的荧光特性与其表面状态息息相关,因此,绝大多数碳量子点都表现出依赖 pH的荧光特性,具体表现为碳量子点的荧光强度随 pH值的变化而变化[11],这一特性通常归因于碳量子点表面的质子化和去质子化效应[12]。除荧光强度外,碳量子点的发射峰位置也会随着 pH的变化而改变[12],但这一类变化通常体现为碳量子点固有发射峰的轻微移动,到目前为止,尚未见到碳量子点能在不同pH环境下产生新发射峰的报道,尤其是由pH变化引起的红光发射。因此,迫切需要对这类独特的pH响应行为及其机理进行深入研究。
本研究设计了以柠檬酸为碳源,甲酰胺和水为混合溶剂的溶剂热反应体系,可以简单地一步合成氮掺杂荧光碳量子点,且所得到的碳量子点具有独特的pH响应性,在强碱性溶液中,会产生新的不依赖于激发光的红光发射,类似的红色荧光也出现在富含羟基的醇类溶剂中。
1 实验方法
1.1 材料和试剂
柠檬酸(AR,99.99%)、甲酰胺(AR,98%)、乙醇(AR,≥99.7%)、盐酸(AR,≥98%)及氢氧化钠(AR,≥98%)购自成都科龙化学试剂厂。3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(MTT) (SIGMA)用于碳量子点细胞毒性测试。所用去离子水均为超纯水(18.2 Ω)。
1.2 碳量子点的制备
碳量子点的制备过程如下:首先,将1.5 g柠檬酸溶解在甲酰胺(30 mL)和水(20 mL)的混合溶液中;然后,将所得的均匀透明溶液转移到 100 mL聚四氟乙烯反应釜中,在 180 ℃的温度下反应 5 h;待反应釜自然冷却至室温后,将反应所得暗红色溶液离心(1000 r/min),收集沉淀;用丙酮清洗数次以除去反应残留物及小分子物质;然后,用 0.22 μm 的滤膜过滤;最后,将所得溶液冻干。
1.3 仪器与表征
荧光分光光度计(F-7000,HITACHI)和紫外分光光度计(LS-650,Perkin-Elemer)用于表征碳量子点的光学性质;透射电子显微镜(FEI Tecnai F20)用于表征大小和形貌;傅里叶变换红外光谱仪(Nicolet 6700)和X射线光电子能谱(Kratos Axis Ultra DLD)用于表征表面基团和元素组成;X射线衍射(Dandong Fangyuan DX-1000)用于表征碳量子点的结构;拉曼光谱(LabRAM HR)用于表征杂化程度。
1.4 细胞毒性及成像实验
细胞毒性实验:MTT法检测碳量子点的细胞毒性。将MG63(人体骨肉瘤细胞)以每孔105个细胞接种于 24孔板,将培养板置于细胞培养箱中(37 ℃,5% CO2)培养24 h ,然后加入不同浓度(10、20、50、100 μg/mL)的碳量子点继续培养24和72 h,把无碳量子点组设为对照组。培养1和3 d后,细胞进一步用0.5 mg/mL MTT培养4 h,然后,移除加入的溶液,加入二甲基亚矾(DMSO)溶解,摇床振荡10 min。最后,酶标仪测定细胞溶液在波长490 nm处的吸光度,记录并处理实验结果。
细胞成像实验:将MG-63细胞以每孔105个细胞接种于 24孔板,将培养板置于细胞培养箱中(37 ℃,5% CO2)培育 24 h。将 100 μg/mL 的碳量子点溶液通过一层 0.22 μm的滤膜,然后加入到孔板中。混合物培养12 h后,去除DMFM培养基,接着用PBS清洗三次以除去剩余的碳量子点,最后用荧光显微镜(Laika,DMI8)采集图像。
2 结果与讨论
2.1 形貌与结构表征
图1(a~b)为样品的TEM和HRTEM照片,由图可知,所制备的碳量子点近似于球型,尺寸比较均匀,对其粒径进行统计分析,发现其尺寸主要分布在4~5 nm之间(图1(a)插图)。高分辨率TEM表明,所制备的碳量子点呈现出明显的晶格化特点,晶面间距经测量约为 0.21 nm,与石墨类材料的[100]晶面相对应[13],这表明所制备的碳量子点具有类似石墨的结构。进一步对碳量子点进行 XRD和拉曼光谱表征,以便深入地了解其结构。在 XRD图谱中,衍射角26°的位置出现了一个较窄的特征峰(图1(c)),对应于石墨结构的(002)晶面[14],这表明所制备的碳量子点具有较高的石墨化程度,这与 HRTEM 照片的结果一致。拉曼光谱显示在~1300和1530 cm-1处出现了明显的特征峰(图1(d)),分别对应于表示无序碳结构(sp3)的D峰和有序碳结构(sp2)的G峰[15]。此外,在1100和963 cm-1处也出现了明显的特征峰,分别对应于吡咯环和吡啶环结构[16]。
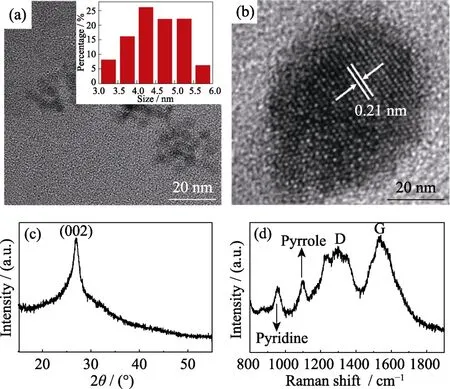
图1 碳量子点的 TEM 照片(插图为粒径分布图)(a)、HRTEM照片(b)、XRD图谱(c)和拉曼光图谱(d)Fig.1 TEM image (a),HRTEM image (b),XRD pattern (c),and Raman spectrum (d) of the prepared CDs with inset in (a)showing diameter distribution
随后,用FT-IR和XPS对所制备的碳量子点的结构和表面基团进行了表征。FT-IR谱图如图2(a)所示:1641、1597和 1347 cm-1处的吸收峰分别为C=N/C=O,C=C和C-N的伸缩振动峰,这表明所制备的碳量子点具有芳香结构,1196和1096 cm-1处的吸收峰是 C-O-C的不对称和对称伸缩振动峰;3000~3500 cm-1为N-H和O-H的伸缩振动峰,表明所制备的碳量子点具有丰富的表面基团,如氨基、羟基等。图2(b~c)分别为碳量子点的 XPS高分辨C1s、N1s和O1s图谱,由图可知,C1s经拟合后可分裂为4个峰,峰位分别为284.4、285.2、287.1和288.8 eV,分别对应四种含碳结构:C=C、C-N、C-O和C=N/C=O。N1s可分裂为三个峰,分别为吡啶型氮化物(399.1 eV)、氨基氮(399.6 eV)和吡咯型氮化物(401.3 eV),这一结果与拉曼光谱一致。O1s分裂为两个峰,分别对应C=O(530.7 eV)和C-O (532.4 eV),上述结果与 FT-IR的表征一致,表明该碳量子点含有丰富的含氮及含氧基团。
2.2 光学性质研究
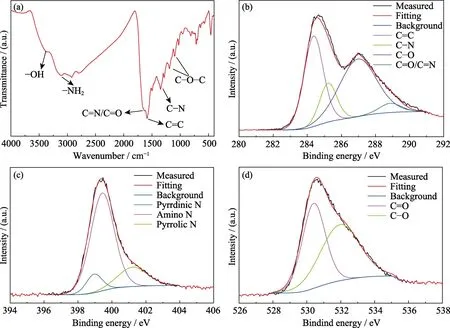
图2 (a)碳量子点的FT-IR谱图及高分辨XPS能谱图;(b) C1s;(c) N1s;(d) O1sFig.2 (a) FT-IR spectrum of prepared CDs,high-resolution XPS spectra of C1s (b),N1s (c) and O1s (d) of prepared CDs
图3(a)为所得碳量子点的紫外吸收光谱,如图所示,在250~300 nm出现了一个窄的吸收,这主要归因于碳量子点的 sp2区域的 π-π*跃迁[17];此外,在360 nm处出现了一个较宽的吸收峰,这是由于碳量子点的表面态捕获激发态的能量产生的,这一吸收峰通常会产生蓝色荧光[18]。所制备的碳量子点具有良好的水溶性,其溶液在紫外灯照射下发出明亮的蓝色荧光,与其发射波长一致(图3(a))。图3(b)是碳量子点在不同激发波长下的荧光光谱,碳量子点的最佳激发波长为360 nm,与其吸收峰位置一致,其对应的发射峰为448 nm。此外,所制备的碳量子点表现出了典型的依赖于激发波长的特征,即发射波长随着激发波长的增大而红移,且伴随着荧光强度的降低,这与文献报道相符[11,19-21]。
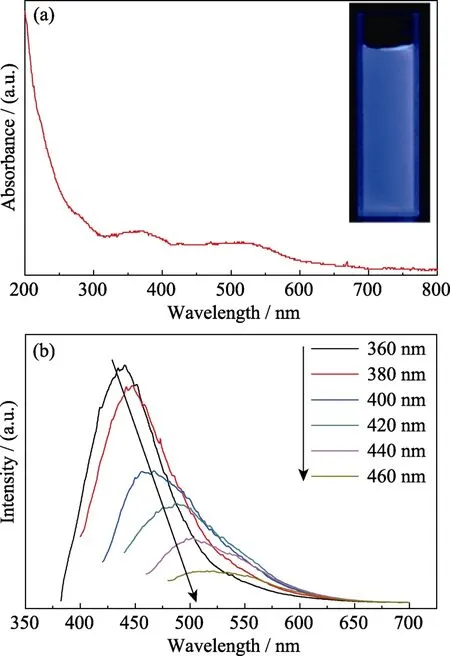
图3 紫外吸收光谱(插图为碳量子点在紫外光下的光学照片) (a)和不同波长激发下的荧光光谱(b)Fig.3 UV-Vis absorption spectrum of prepared CDs with insets showing optical images of prepared CDs under UV lamp(365 nm) (a) and fluorescent spectra under various excitation wavelengths (b)
2.3 羟基诱导的碳量子点的特异性pH响应行为与机理探讨
图4(a~g)为所制备的碳量子点在不同 pH条件下的荧光光谱。由图可知,当 pH值从 1增大到 9时,碳量子点的荧光图谱基本相同,但其荧光强度在pH从3增至9时呈线性减弱(图4(h)),但幅度较小,在紫外灯下光强并没有明显减弱(图4(i))。但当pH增至11和13后,除了在蓝绿光区域依赖于激发光的发射以外,碳量子点在红光区域出现了一个新的发射峰,该发射峰随着激发波长的增大有轻微的红移,从600 nm红移至610 nm,且这个新的发射峰的强度会随着 pH的增大而增强,这一变化直观地体现在紫外灯的照射下,碳量子点溶液的颜色从蓝色变成了粉红色(图4(i))。
在不同的 pH条件下,可以看到碳量子点位于蓝绿光区域的发射峰基本相同,而在较强的碱性条件下,碳量子点却产生了独特的pH响应,即在红光区域产生了新的发射峰。通常,蓝绿光区域的发射峰是碳量子点固有的,主要来自于其表面状态,因而具有依赖于激发的荧光特征[4,22];而在较强碱性条件下产生的红光发射不具有依赖激发光的荧光发射,应来自于碱中的氢氧根。由之前的表征可知,该碳量子点表面富含含氮和含氧基团,因此,碱中含有的大量氢氧根通过氢键的方式结合在碳量子点表面[23-24],形成新的、稳定的发光中心。值得注意的是,并不是在所有碱性溶液中都会产生新的红光发射,比如在pH等于9时,就没有产生(图4(e)),这很可能是由于在较弱的碱性溶液中,氢氧根的数量不够导致的。
为了证明这一猜想,本研究中将碳量子点分散在富含羟基的两种常见的醇类溶剂甲醇和乙醇中,其荧光图谱如图5(a,b)所示。由图可知,碳量子点在两种醇类溶剂中的荧光图谱与其在较强碱性溶液中的荧光图谱(图4(f,g))基本相同,在红光区域都出现了基本不依赖激发光的发射峰,且位置相近,这一结果初步证明在较强碱性溶液中碳量子点新出现的发射峰来源于碱中的氢氧根。而在较弱的碱性溶液中并没有出现新的红光发射是因为在该条件下溶液中的氢氧根数量不够。
为了进一步证明这一假设,将甲醇和水按不同的比例进行混合来改变混合溶液中羟基的含量,结果如图6所示。按甲醇的含量设的三个比例(体积比),分别为75%甲醇溶液、50%甲醇溶液和25%甲醇溶液。由图可知,当甲醇的含量超过50%时(图6(a,b)),碳量子点的荧光谱图中均出现了新的红光发射峰,但是,当混合溶剂中甲醇的含量降到 25%时,碳量子点的荧光谱图中没有出现新的发射峰,这可以直观地从荧光照片中看出,如图6(d)所示,在紫外灯的照射下,较高甲醇含量的溶液发射的是粉红色荧光,且甲醇含量越高,荧光强度越高;而 25%甲醇溶液发出的是蓝色荧光。这一结果表明,溶液中羟基含量的多少直接决定了红光区域的发射是否会产生,羟基的含量需要达到一定水平才能让碳量子点表面形成新的发光中心从而产生新的红光发射。同时这一结果也证明了碱性强弱与红光发射之间的联系。
2.4 碳量子点的应用
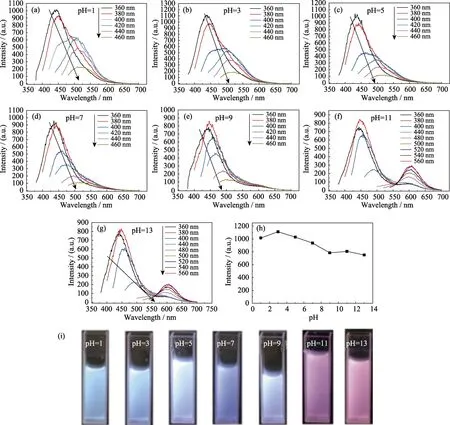
图4 不同pH条件下碳量子点的荧光光谱(a~g)、pH值与碳量子点荧光强度的关系(EX=360 nm)(h)和不同pH值的碳量子点溶液在紫外灯下的荧光照片(i)Fig.4 Fluorescent spectra of as-prepared CDs with different pH values under various excitation wavelengths (a-g),fluorescent intensity at different pH under excitation of 360 nm (h) and optical images of prepared CDs with different pH under UV lamp (365 nm) (i)
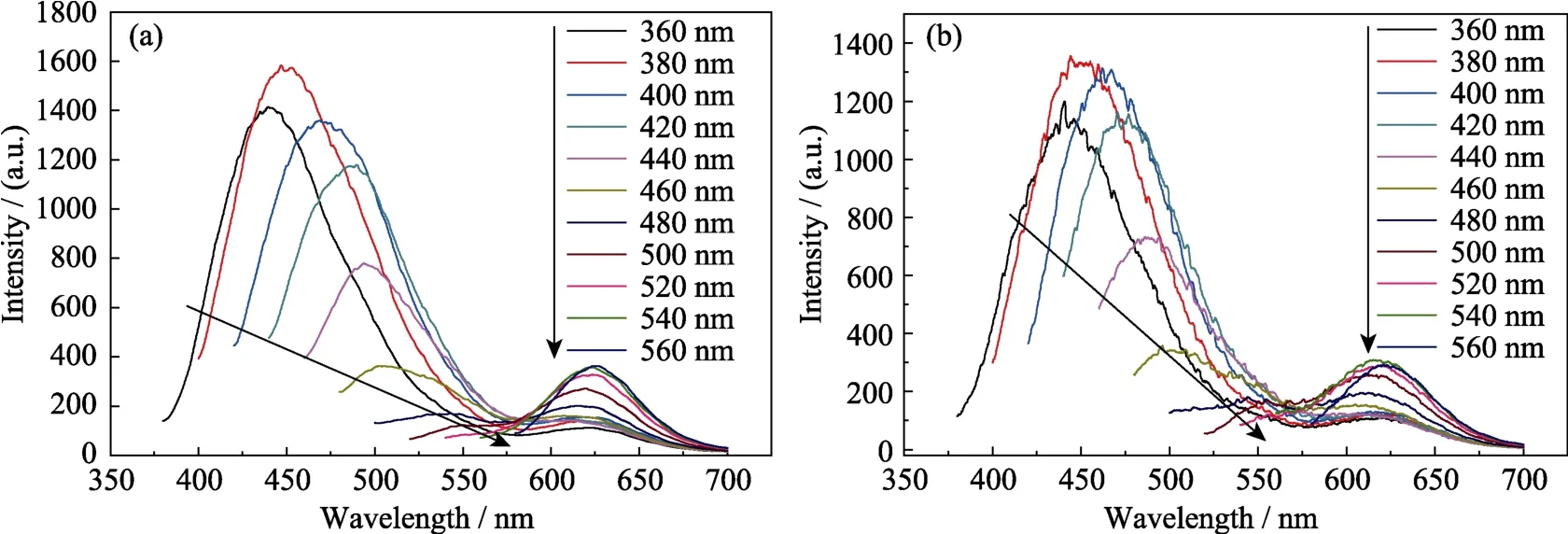
图5 所制备的碳量子点在甲醇中的荧光光谱(a)和所制备的碳量子点在乙醇中的荧光光谱(b)Fig.5 Fluorescent spectra of prepared CDs in methanol (a) and ethanol (b) under various excitation wavelengths
为探究所获得的碳量子点可能的生物应用,本研究首先检测了其细胞毒性,如图7(a)所示,细胞随培养时间延长正常增殖,碳量子点的存在并未显著降低细胞的增殖,表明所制备的碳量子点具有较低的细胞毒性。从将碳量子点与MG-63细胞共培养的荧光显微镜照片可以看出,碳量子点可被 MG-63细胞摄取并分布在细胞质中,细胞在 405、488和543 nm激发下分别发出蓝光、绿光和红光。这一结果表明该碳量子点可用于细胞标记,显示出在生物成像领域的潜在应用价值。
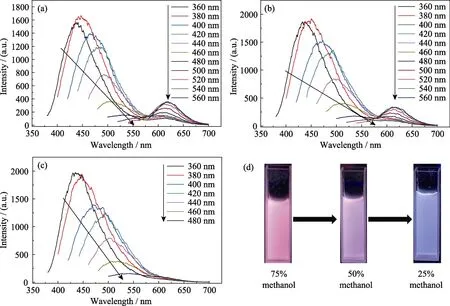
图6 碳量子点在不同比例甲醇和水混合溶液中的荧光图谱Fig.6 Fluorescent spectra of prepared CDs in the mixed solution of methanol and water at methanol concentration of 75% (a),50% (b) and 25% (c) under various excitation wavelengths,and their optical images under UV lamp excitation (365 nm) (d)

图7 碳量子点对MG-63细胞活性没有显著影响(a),所标记的MG-63细胞在紫外(b)、蓝光(c)和绿光(d)照射下的荧光照片Fig.7 Cell viability (a) and fluorescence images of MG-63 cells excited by UV (b),blue (c),and green light (d)
3 结论
本研究采用柠檬酸为碳源,甲酰胺和水为混合溶剂,通过溶剂热的方式合成了氮掺杂的碳量子点。该碳量子点具有良好的水溶性且在水中具有明亮的蓝光发射,同时细胞毒性低,因此可以作为荧光探针应用于细胞成像领域。此外,该碳量子点还具有独特的pH响应,即在较强碱性溶液中,碳量子点会产生新的不依赖于激发的红光发射峰,在紫外灯的照射下,其溶液也从明亮的蓝色变成粉红色,但值得注意的是,随着碱性的逐渐减弱,红光发射会消失。经实验证明,同样的红光发射也出现在富含羟基的醇类溶剂中,且随着醇类溶剂含量的逐渐减少,产生的红光发射同样会消失。这些结果表明,碳量子点新产生的红光发射来自氢氧根或羟基,氢氧根或羟基可以通过氢键与碳量子点表面的含氮及含氧基团结合,形成新的、稳定的发光中心。

