伏立康唑致急性胰腺炎一例及相关文献复习
徐欢 朱星星 唐从胜 潘志杰
1海宁市人民医院呼吸内科314400;2浙江大学附属第一医院呼吸内科,杭州310000
侵袭性肺部真菌感染病死率较高,其中以曲霉感染最常见,占所有侵袭性肺部真菌感染的5.9%~12%[1]。美国感染病协会推荐伏立康唑作为大多数侵袭性肺曲霉病 (invasive pulmonary aspergillosis,IPA)的一线治疗药物。伏立康唑是一种广谱的三唑类抗真菌药,主要通过抑制真菌中由细胞色素P450介导的14a-甾醇去甲基化,从而抑制真菌细胞壁麦角甾醇的生物合成,产生抗真菌作用。随着该药在临床治疗中的广泛应用,其不良反应的报道也日益增多。本文报道与伏立康唑相关临床少见不良反应急性胰腺炎1例,同时回顾近年来国内外相关文献,对其发病机制及防治加以阐述,以期提高临床医师在治疗过程中对其相关少见不良反应的认识,从而保障患者用药安全。
1 临床资料
患者,女,74岁,既往有高血压、痛风病史,身高155 cm,体质量40 kg。因“反复咳嗽、咳痰10余年,加重伴胸闷、气促5 d”于2018年1月18日入院。入院后完善相关辅助检查。血常规:白细胞2.5×109/L,中性粒细胞比例65.5%,血红蛋白100 g/L,血小板计数220×109/L;C反应蛋白47.7 mg/L;降钙素原0.11μg/L;血气分析:p H 7.21,PaO263.5 mm Hg (1 mm Hg =0.133 k Pa),PaCO2115.3 mm Hg,血氧饱和度91%;肝功能正常 (丙氨酸氨基转移酶40 IU/L,门冬氨酸氨基转移酶23 IU/L);甘油三酯1.32 mmol/L,血胆固醇5.29 mmol/L,血钙2.11 mmol/L。入院诊断: (1)COPD 急性加重,Ⅱ型呼吸衰竭; (2)高血压2级 (很高危); (3)痛风。治疗上给予无创呼吸机辅助改善肺通气,头孢哌酮舒巴坦针 (2.0 g,静脉滴注,每12小时1次)抗感染,甲强龙针 (40 mg,1 次/d)抗炎(用药5 d),同时给予埃索美拉唑针护胃、氨溴索化痰、多索茶碱平喘等对症处理;同期完善辅助检查,送检痰细菌及真菌培养等。患者咳嗽、咳痰症状有所缓解,但活动后仍胸闷、气急明显。入院后第7天,患者2 次痰培养结果提示曲霉菌 (+),复查肺部CT:两肺多发感染性病变 (图1)。结合临床表现,考虑患者可能存在侵袭性肺曲霉菌病。于2018 年1 月27 日起给予伏立康唑胶囊(200 mg,2次/d)抗曲霉菌治疗,患者咳嗽及胸闷不适症状逐渐缓解。用药第23天患者突发腹痛,腹部查体:腹平软,中上腹压痛,无反跳痛,Murphys'征阴性。血淀粉酶1 334 U/L,丙氨酸氨基转移酶675 U/L,门冬氨酸氨基转移酶1 193 IU/L;血常规:白细胞5.4×109/L,中性粒细胞比例72.5%,血红蛋白106 g/L,血小板计数103×109/L,C反应蛋白12.5 mg/L;腹部CT:急性胰腺炎,胆囊结石。上腹部磁共振胰胆管成像:胆囊结石,胰尾部略肿胀伴周围少量渗出,考虑为急性胰腺炎可能,腹腔少量积液 (图2)。结合患者病史及前期临床治疗经过,急性胰腺炎不排除和药物相关可能,故停用伏立康唑胶囊,改用卡泊芬净针继续抗真菌治疗,同时给予禁食、埃索美拉唑钠针抑酸、生长抑素抑制胰腺分泌、加贝酯抑制胰蛋白酶等对症处理。患者腹痛逐渐缓解,肝功能及淀粉酶逐步恢复正常。

图1 肺部CT 示两肺多发渗出性病变
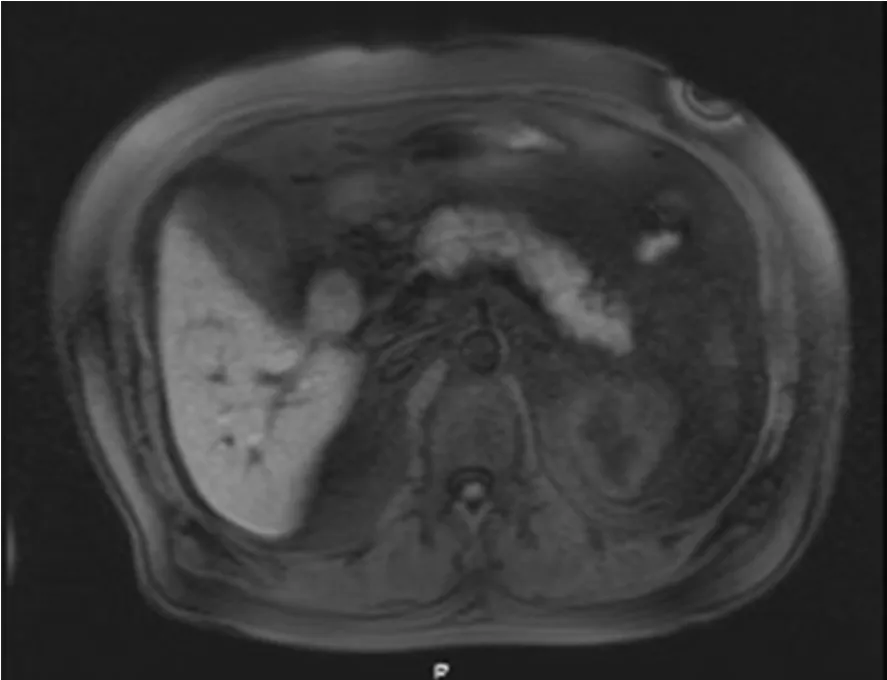
图2 腹部磁共振胰胆管成像示胰尾部略肿胀伴周围少量渗出
2 讨论
IPA 是临床上常见的一种肺部侵袭性真菌病,是由曲霉菌感染或吸入曲霉菌抗原所引起的一组急性或慢性肺部感染性疾病。广谱抗生素使用、长期糖皮质激素应用、大剂量糖皮质激素应用 (总剂量>700 mg)、免疫抑制剂应用、低蛋白血症、COPD、糖尿病、粒细胞缺乏、反复住院等都是IPA 的危险因素[2]。
本例患者为老年女性,有COPD 基础,近期反复住院,存在IPA 高危因素;此次起病出现咳嗽、咳痰伴胸闷、气促不适症状,CT 检查影像示两肺有渗出性病变,2次痰培养为曲霉菌,临床诊断IPA。根据2016年美国感染病协会曲霉菌诊断处理实践指南,IPA 治疗推荐首选伏立康唑针,第1天静脉滴注6 mg/kg (每12小时1次),以后静脉滴注4 mg/kg (每12 小时1 次);或者口服200~300 mg (每12小时1次)或者按体质量4~6 mg/kg给药[3]。因考虑该患者高龄,药物不良反应耐受性差,结合体质量,故给予伏立康唑胶囊200 mg (每12小时1次)口服治疗。
患者既往否认有胆道疾病,否认饮酒史,无高脂血症、高钙血症,排除酒精性、高脂血症、高钙血症等原因导致胰腺炎。患者在服用伏立康唑23 d后出现突发腹痛不适,血淀粉酶升高,腹部B 超、腹部CT 检查提示并发急性胰腺炎,磁共振胰胆管成像提示无胆道结石及胰管近端扩张等表现,故胆石症所致胰腺炎无依据,首先考虑患者急性胰腺炎和伏立康唑相关。
伏立康唑作为一种广谱的三唑类抗真菌药,主要通过抑制真菌中由细胞色素P450介导的14a-甾醇去甲基化作用,从而抑制真菌细胞壁麦角甾醇的生物合成,产生抗真菌作用。在人体中,伏立康唑主要通过肝脏代谢,抑制肝细胞色素P450 系统,代谢产物约有80%经尿排出,20%从粪便排出。多数患者耐受性良好,但仍有部分患者会出现伏立康唑相关性药物不良反应,发生率为20.6%~30.0%[4-7]。在一项随机双盲多中心的安全性和耐受性研究中,对137 例使用伏立康唑患者的适应证、疾病谱、疗效及安全性进行相关评估,指出伏立康唑最常见的不良反应为短暂的视觉障碍(23%)、 发 热 (12%)、 腹 泻 (9%) 及 呕 吐(7%),另外还表现为肝功能异常、恶心、头痛、皮疹。伏立康唑的其他少见不良反应还包括低血糖、肺炎、光敏性皮疹和银屑病恶化等[8-9]。伏立康唑片剂导致肝功能异常较常见,但继发急性胰腺炎国内尚无报道。
Philip等[10]曾报道1例真菌感染患者服用伏立康唑治疗后出现急性胰腺炎。该病例为1例急性髓系白血病化疗后的患者,继发鼻窦及肺部侵袭性曲霉感染,口服伏立康唑200 mg (每12小时1次),12 d后出现急性腹痛,血淀粉酶升高,考虑继发急性胰腺炎,停药并给予对症处理好后症状缓解,12 d后淀粉酶恢复正常。因患者病原体药敏提示对两性霉素B耐药,同时患者无法负担卡泊芬净,遂将伏立康唑减量,改为100 mg (每12 小时1次)口服继续治疗,患者无明显不良反应。期间患者自己不慎再次将药物加量 (200 mg,每12小时1次),用药1周后再次并发急性胰腺炎,调整用药后症状缓解,后续持续给予口服伏立康唑(100 mg,每12 小时1次)治疗IPA 8 个月,期间未再出现急性胰腺炎症状。另外也有应用伊曲康唑治疗甲癣、泊沙康唑治疗耐药口腔、阴道白色念珠菌病过程继发急性胰腺炎报道[11-12]。
药物是引起急性胰腺炎的罕见原因,发生率为0.1%~2%,药物性胰腺炎的发病机制尚不清楚。药物引起的急性胰腺炎的潜在机制包括胰管收缩、细胞毒性和代谢效应、毒性代谢物或中介性和超敏反应的积累反应。药物的不良反应,如高甘油三酯血症和慢性高钙血症,也是药物引起的急性胰腺炎的机制。目前伏立康唑导致急性胰腺炎机制不明。有文献报道唑类导致急性胰腺炎,考虑为药物的质变型异常,即B 型药物不良反应,其特点为发生率低,死亡率高,难以预测,和药物本身的药理作用无关,常和剂量无关。其机制尚不明确,考虑很可能和药物结合的蛋白形成的活性物质激活机体免疫应答,导致细胞损伤,造成机体损害有关[12]。伏立康唑使用的剂量或血药浓度与药物不良反应/不良事件发生之间是否相关,目前也尚未有统一的结论。Pieper等[13]认为,伏立康唑的使用剂量与血药浓度之间无可以预见的线性关系,同时用药剂量与疗效之间也无一致的关系。伏立康唑的血药浓度与是否发生药物不良反应/不良事件之间也无明显的相关性[14-15]。然而,Quintard等[16]研究表明,伏立康唑主要通过肝脏代谢,另外约有2%以原形从肾脏排出。对于肝肾功能不全患者,伏立康唑的血药浓度可能会偏高,从而导致药物不良反应/不良事件增多。Alffenaar等[17]认为,考虑到口服对消化道反应大于静脉,故口服唑类出现消化道不适症状的可能性比静脉用药更大。
临床医师在使用伏立康唑治疗过程中,对于患者治疗期间出现的新症状,需要进一步鉴别,应密切关注有无药物不良反应,以及药物之间是否存在相互作用而导致的少见不良反应。
利益冲突所有作者均声明不存在利益冲突

