转子的光学标测技术及进展
王泽呈 秦牧 刘旭
心房颤动(简称房颤)是临床上常见的一种心律失常的类型,它的发病率高且随着年龄的增长而升高。房颤会明显的影响患者的心脏功能,并降低其生活质量,增加其死亡率[1]。目前临床上常用的治疗房颤的方式主要为药物控制心室率以及抗凝治疗以预防血栓[2],药物治疗可以改善患者症状,预防房颤的并发症,但无法彻底治愈房颤。
目前临床上认为导管射频消融术是能治疗房颤的方法之一,而环肺静脉隔离(CPVI)又被认为是房颤导管消融的“基石”,它被广泛的运用于阵发性房颤、持续性房颤及永久性房颤的治疗中。对于阵发性房颤,目前临床上主要以CPVI为主,而对于持续或永久性房颤,除CPVI外,术者通常还会采用线性消融或碎裂电位消融等补充术式,然而由于房颤的机制目前仍未阐明,对于房颤的射频消融手术目前仍有较高复发率,医生们迫切的希望寻找到一种更个体化、针对性的治疗策略以改善这一困境。在Narayan等[3]的研究中,转子(ROTOR)的概念被首次提及,在这项CON-FIRM研究中,术者在房颤患者的心房内可以标测到一种螺旋波,他们把这种螺旋波称为“转子”,随后对转子进行消融可以有效的终止房颤。在研究者针对转子进行进一步的研究证实中,运用了多种不同的标测方式,包括且不限于无创电生理成像(ECGi)[4]、腔内全景式电生理标测[3]、对比剂延迟增强核磁共振显像[5]、相位标测[6]等,而 “光学标测”(optical mapping)技术也被运用于研究转子。笔者即针对光标测技术在转子标测中的运用进行阐述。
1 光学标测技术的原理及方法
自Davila等[7]于1973年最早运用光学标测技术记录了神经细胞的动作电位,Salama等[8]于1976年运用光学标测技术记录了心脏细胞的电活动,后于1990年,Davidenko等[9]运用光学标测在动物心脏中发现了螺旋波的存在,并证明它可以诱发室性心动过速,光学标测技术在细胞电活动的研究中已运用了很久。
光学标测技术的原理是基于波长相关的光与组织的相互作用,包括了光子的散射、吸收、反射和荧光效应。通过光学标测技术研究心脏的电位变化,即是通过运用电压敏感的荧光性染料作为标记物,使细胞跨膜电位的变化表现为荧光物质亮度的变化,并被相关检测装置记录下来。电压敏感的荧光材料通常为钙离子螯合剂,经过荧光染料标记的细胞,其内钙离子与荧光染料相结合,使细胞内钙离子浓度的变化可以被即时观测,由此反应出心肌细胞除极和复极的过程。再运用光学探头,可以让我们可以了解同一片心肌组织的不同区域在同一时间的除极和复极的情况,进而了解到这一片心肌组织在一个时间段内的电活动过程,也正是如此光标测技术能非常好的运用于转子的标测中。
在目前的光学成像技术中,接收成像装置包括电子扩增管(photomultipliers,PMT),激光扫描(laser scanning),电荷耦合(charge-coupled device,CCD)照相机,光电二极管阵列(photodiode arrays,PDA)以及互补金属氧化物半导体(complementary metal-oxide semiconductor,CMOS)照相机。其中PDA技术和CCD相机在心脏的成像中运用的较多,而CCD技术相较于PDA有着更高的空间分辨率,这得益于它感应器上较多的像素点,但这与此同时也带来了较低的灵敏度和较高的信噪比。
任意一个光学标测系统都包括一个二维的光学感受器和一个稳定的光源,可选择的光源包括了激光、钨卤素灯或者发光二极管。图1展示的是一个单透镜的光学标测系统的构造[10],它包括一个光电二极管阵列,一个256通道的信号调整器/增幅器,模拟-数字信号转换器以及一台电脑。激发光束通过一个(520±30) nm的干涉滤光片并聚焦在预先放置于组织室内的组织表面,相机镜头负责收集荧光,并将其引导通过一个610 nm长的滤镜,将所选择的心脏区域的图像聚焦在PDA上面。

图1 光标测试验系统图例[10]
2 光学标测技术在转子标测中的运用
在房颤的维持机制中,折返一直占领着主要的地位。20世纪40年代,研究者们认为折返可能维持并驱动着房颤[11],到了2012年,Narayan等[3]利用最新的腔内全景式电生理标测技术,将两个64极的篮网电极分别置入患者的左、右房内,并在房颤的状态下进行心房电活动的同步记录,通过计算机的分析处理,找到转子靶点,对其进行消融能有效的终止房颤的发作。而在随后的研究中,研究者们发现转子作为一种特殊的功能性折返,具有可移动的特点[12],转子发出的螺旋波围绕着一个核心旋转,且转子的周长也具有不定性。当转子的波前(wave front)在移动时如遇到障碍,会分裂产生更多子波[13]。以上这些对转子更深入的研究,离不开各种标测技术的帮助,而光标测技术,就是在转子研究中极为重要的工具之一。
早在1998年,Skenes等[14]就利用光学标测技术在房颤发作的羊心脏上发现了其电活动在时间及空间上具有周期性,而在此之前,房颤发作时不规则的电活动被普遍认为是无序的、随机的。他们利用高分辨率的成像技术以及光学频谱分析来研究置于6个灌注系统里的20个离体羊心脏,以确认连续的波前(wave fronts)具有时间及空间上的周期性。对房颤心脏的频谱分析中显示,所有的标本均有多个窄带峰和一个主峰[(平均(9.4±2.6) Hz;周长(112±26)ms)]。20例右房光学标测记录中的12例以及全部的左房标测结果证明了时间和空间上的周期性。在他们看来,在个别例子中,这种周期性的电活动来源于心外膜的转子或周期性的可能代表了跨心房壁的折返的突破点(breakthroughs)。而在大多数情况下,他们观察到的周期性的波是由视野外进入成像区域的。
图2中的上图是Skenes等离体羊心脏实验装置的示意图,在这次实验中,研究者们取活体羊的心脏标本置入灌注装置,冠状动脉通过主动脉根部的套管在115~140 mL/min的恒定流量下持续灌注,在实验开始时,确保心脏处于窦性节律,并有节奏地有力收缩。甲氧基维拉帕米(D600, 2×10-6mol/L)作为电解耦剂添加到台式液(Tyrode′s solution)中。注射5~10 ml的电位染料di-4-ANEPPS (10 mg/mL)以同时成像心外膜电位变化引起的荧光。研究者们使用两个相同的摄像机同时记录了右房游离壁的20 000个位点和左房附着物的10 000个位点。利用准单色光(535 nm)直接照射到心房的心外膜表面。发射的荧光通过645 nm滤波器,投射到CCD摄像机上,以每秒120帧的速度采集(采样间隔为8.33 ms)。两个摄像机都是由一个脉冲同时触发的。随后研究者们用心外膜的高频刺激诱发房颤,并开始进行光学标测,如图2中下图所示,4张连续的等时线图记录了490 ms时间内左房的激活情况,从图中可以看出这段时间内,左房被相同的空间定向的波阵面(右下角来源)反复激活,波阵面的周长为120 ms,这也与连接于心外膜的双极心电图的主频一致。
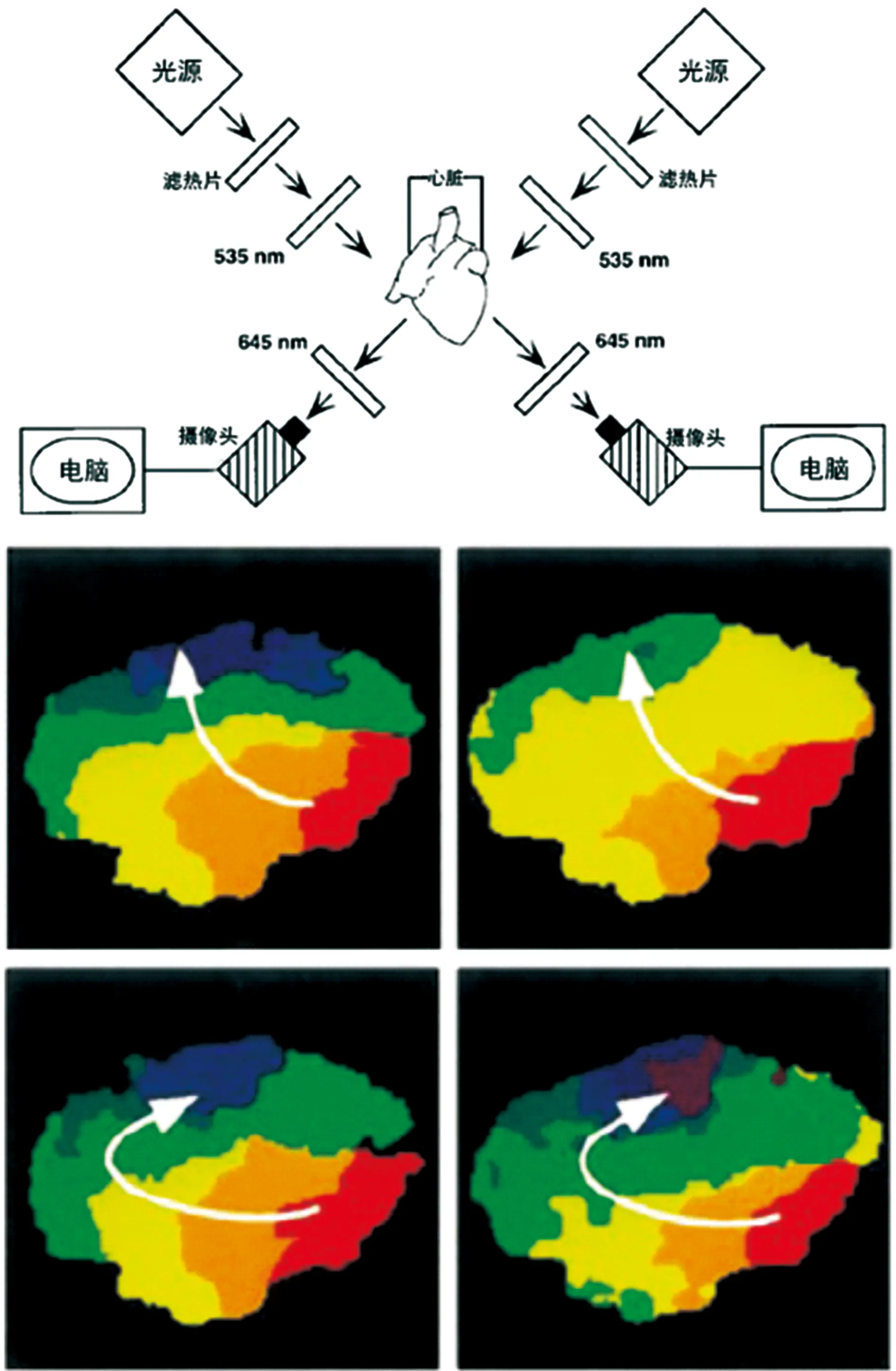
图2 离体羊心脏的光学标测装置示意及标测结果[14]
Skenes等的实验,利用高精密度的光学标测技术证实了房颤发作时,心房电活动在时间及空间上具有周期性,改变了以往人们对房颤发作时的心电活动规律的看法,房颤发作时,心房的电活动并非是无组织,无规律的活动。同时,如图3所示,Skenes等首次在左房中利用光学标测技术发现了转子的存在,提出了转子的概念,并指出,转子是基于组织传导的异质性和不应期而形成的。不过当时虽有提及转子的理念,但研究者们并没有深入研究转子在房颤维持机制中发挥的巨大作用,也没有发现对转子的消融能有效终止房颤,转子的概念仍未得到广泛的重视。
到了2015年,在Hansen等[15]的研究中,研究者们在人类心脏的内外膜同时进行光学标测,提出了房颤由转子维持的新证据。如图4中所示,在这项研究中,研究者们取用8个冠状动脉灌注下的患有房颤的人类右房,并用近红外光谱的di-4-ANBDQBS染料染色。他们使用双面的光学标测系统[(内膜以及外膜,分辨率330 μm2和一个全景的,分辨率940μm2的CMOS照相机(100×100像素)]对心脏的内膜以及外膜的动作电位同时进行标测,同时计算得到内外膜间的电位延迟,由全景相机得到的平均的主频率可计算出房颤的周长。研究者们还利用3D钆对比增强核磁共振(GE-MRI,分辨率80μm3)来显示心房壁的结构,包括其厚度、跨膜纤维的角度差异以及间质的纤维化程度。研究者们同样是以高频刺激来诱发房颤并使其维持。
图5中展示了Hansen等的一部分研究成果,A、B两图是三维钆对比剂增强核磁共振显像结果,该结果显示出了房颤的传导路径(红箭头)以及驱动它的折返(黑箭头)。B图通过三维钆对比剂增强核磁共振成像显示的心肌截面,在这些截面中发现了在折返环路上存在着的间质纤维化(白箭头所指)。C图展示了通过光学标测得到的房颤的主频率,其中a区显示了驱动灶的频率,达到了15.6 Hz,b区则为驱动灶外的频率,平均在8.9 Hz。D图展示了相同区域,心内膜和心外膜光学标测的成像结果,在心内膜发现了折返,其路径由黑色箭头所指,而在心外膜则表现为一个突破,黑色虚线显示了心内膜折返环的位置。E图展示了这个折返的光学动作电位情况,可以观察到透壁电位传导的延迟。

图5 离体人类心脏在房颤下的内外膜同步光学标测及三维对比剂增强核磁共振(GE-MRI)显像结果[15]
这次光学标测的结果再次证实了折返是房颤维持的重要机制,而心内外膜同时的标测更清晰的展示出了动作电位在透壁传导时出现的延迟,同时揭示出在心内膜标测到的转子有多种表现形式的原因——即转子具有空间立体的结构。当我们在心内膜进行标测时,转子可能表现一个局部高频且离散的电位、一个局灶的兴奋点抑或是高频的电位,这三种多样化的标测结果所形成的原因主要取决于转子的空间结构,当转子在内膜平面上旋转时,它表现为局部高频且离散的电位;当它在内外膜间折返时,转子在心内膜表现为一个突破;当转子在心外膜旋转时,我们则可以在内膜标测到多个高频的电位。再结合对比增强核磁共振的显像,让我们对折返环上的解剖结构有了更直观的认识,也证明了纤维化在转子形成和维持中发挥着巨大的作用。该实验结果不仅揭示出转子是呈现空间立体的结构,也指导我们在心内膜对转子进行标测时须注意到转子不同的表现形式,提高了转子消融的成功率。
光学标测自1998年第一次运用于转子的标测,如今已走过20个年头,作为转子研究中最重要的武器之一,多次光学标测的结果让我们对转子有了更清晰的了解与认识,本文取两例有代表性的转子光学标测的研究进行介绍,仅是光学标测在转子研究中贡献的冰山一角。通过目前各光学标测的研究结果,结合无创电生理成像(ECGi)、腔内全景式电生理标测、相位标测等不同标测方式的成果,研究者们对于转子的形成以及维持运转的认识愈发清晰,临床上对转子消融的结果也在陆续发表,且成绩喜人,我们有理由相信,随着转子研究的更加深入以及转子消融技术的逐渐展开,房颤这一疾病的治疗也将逐渐变得个体化、精确化,房颤消融术的成功率也将得到明显改善。

