硬化性肺细胞瘤临床病理分析
雷瑞雪,郭 梅,苗兰芳
(安阳市肿瘤医院病理中心,河南 安阳 455000)
2015版WHO将肺硬化性血管瘤更名为硬化性肺细胞瘤,并归入肺腺瘤[1]。肺硬化性血管瘤是一种少见的肺部良性肿瘤,最早由Liebow和Hubbell提出[2],因其无特异性临床表现,病理表现多样且复杂,临床上很容易造成误诊。本文回顾性分析8例硬化性肺细胞瘤患者的临床病理资料,以提高对该疾病的认识,从而为该病的临床诊治提供数据参考。
1 资料与方法
1.1 一般资料收集安阳市肿瘤医院2014年5月至2016年7月经病理学确诊的8例硬化性肺细胞瘤患者的临床病理资料,并由2位病理科医师对所有病例的病理切片进行重新阅片,以进一步确诊。
1.2 方法所有标本均用质量分数4%中性多聚甲醛固定,常规脱水,石蜡包埋,4 μm厚切片,行苏木精-伊红染色(HE染色)和免疫组化(Envision法)全自动染色机染色。抗体甲状腺转录因子-1(thyroid transcription factor,TTF-1)、细胞角蛋白7(cell keratin 7,CK7)、上皮膜抗原(epithelial membrance antigen,EMA)、广谱细胞角蛋白(pan cytokeratin,pCK)、波形蛋白(Vimentin)、Ki-67均购自福州迈新生物技术开发有限公司。
1.3 结果判读TTF-1、Ki-67阳性颗粒定位于细胞核,CK7、pCK、Vimentin阳性颗粒定位于细胞质,EMA阳性颗粒定位于细胞膜和细胞质。染色结果根据组织内部阳性对照和阴性对照进行判读。所有切片均经2位副主任医师职称以上病理科医师仔细阅片和审核。
2 结果
2.1 临床特征8例硬化性肺细胞瘤患者均为女性;年龄27~61岁,平均年龄48岁;2例有咯血症状,其余6例均为体检时发现,其中1例合并甲状腺癌、1例合并乳腺癌;计算机断层扫描检查结果示:3例为硬化性肺细胞瘤,1例为孤立性纤维性肿瘤,2例为炎性假瘤,1例错构瘤,1例结果不明确;原发部位:左上肺2例,左下肺3例,右上肺1例,右肺中叶1例,右肺下叶1例。
2.2 病理特征大体检查示均为界限清楚的类圆形结节,2例有完整包膜,肿物长径1.1~5.0 cm,切面质中等至稍硬,灰白到灰褐色。8例患者中,7例送检术中快速诊断,5例考虑硬化性血管瘤,2例倾向良性肿瘤性病变。常规切片,组织学上含4种结构:乳头状结构,乳头表面被覆立方上皮细胞,乳头不含纤维血管轴心,其内充满圆形间质细胞;实性结构,由大片圆形间质细胞构成,大小较一致;硬化区,在乳头轴心,实性区或血管瘤样区周围见纤维组织增生伴胶原变性,可见钙化;血管瘤样区,见较多扩张的不规则血管样腔隙,内充满红细胞,似海绵状血管瘤。细胞上存在间质圆形细胞和表面立方上皮细胞2种细胞类型,圆形细胞位于乳头内部或实性区,细胞小,有明显边界,细胞质嗜酸或空亮,细胞核形态温和,圆到卵圆形,位于中央,染色质细而分散,缺乏清楚的核仁,核分裂相少见;立方上皮细胞位于乳头表面,也可陷于实性区内形成腺样结构,形态上类似于Ⅱ型肺泡上皮细胞,乳头表面的立方细胞可融合成多核巨细胞。见图1。
2.3 免疫组化特征7例行免疫组化染色,结果显示,间质圆形细胞表达TTF-1(7例)、Vimentin(7例)、EMA(5例)、CD56(3例),部分表达CgA、SYN及NSE(1例);表面立方上皮细胞表达TTF-1(7例)、EMA(6例)、pCK(6例)、CK7(6例)、Vimentin(2例)。2种细胞均未表达孕激素受体、雌激素受体。见图2。
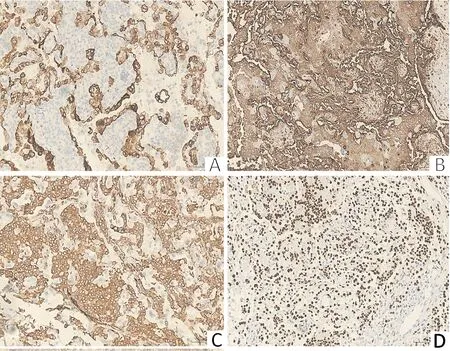
图2 硬化性肺细胞瘤免疫组化特征(Envision法,×100)
2.4 随访本组8例患者均行手术楔形肺切除,其中3例行开胸手术、5例行胸腔镜手术,随访至今,未见复发及转移。
3 讨论
3.1 临床特征硬化性肺细胞瘤好发于中年人,且女性多见。大多数患者无症状,少数可能发生咯血、咳嗽和胸痛。肿瘤多为孤立的,胸部X线显示孤立的界限清楚的肿块,很少钙化,偶尔呈囊性。计算机断层扫描显示界限清楚的肿块伴有明显的对比增强,以及有显著边缘的低度衰减灶。本组8例患者均为女性,平均年龄48岁,仅2例有临床症状,均为单发病灶,1例合并甲状腺癌,1例合并乳腺癌,无明显肺叶分布趋势。影像学易误诊为炎性假瘤、错构瘤、孤立性纤维性肿瘤等。
3.2 病理特征硬化性肺细胞瘤大体上边界清楚,切面黄褐色,绝大部分位于肺外周,也可发生于支气管内或表现为胸膜息肉样肿物,肿物直径0.3~7 cm[3],镜下主要表现为乳头状结构、实性结构、硬化区及血管瘤样区等4种结构,存在间质圆形细胞和表面立方上皮细胞等2种细胞,4种结构常以不同比例混合存在[4]。本组病例仅4例全部包含4种典型的结构,2例未见典型的乳头状结构,2例未见典型的血管瘤样区域。免疫表型方面,多项研究表明,表面立方上皮细胞及间质圆形细胞均表达EMA和TTF-1[5-6],除此之外,表面立方上皮还表达pCK、SP-B、NapsinA,间质圆形细胞还表达Vimentin。本组病例,7例行免疫组化染色,间质圆形细胞表达TTF-1(7例)、Vimentin(7例)、EMA(5例)、CD56(3例),部分表达CgA、SYN及NSE(1例);表面立方上皮细胞表达TTF-1(7例)、EMA(6例)、pCK(6例)、CK7(6例)、Vimentin(2例),2种细胞成分均未表达PR、ER。本结果与文献报道较一致,提示肿瘤本质并非神经内分泌来源,而是来源于原始的、未分化的呼吸道上皮,并与激素水平无明显关系[7],另外,间质细胞和立方上皮细胞均表达EMA和TTF-1,提示两者是来源相同,只是分化的方向不同而已。有文献[8]报道,肿瘤细胞Ki-67特征性表达于细胞膜。
3.3 鉴别诊断1)炎性假瘤:成分较复杂,主要由纤维母细胞和肌纤维母细胞构成及多种炎细胞构成,无典型的乳头状、实性、硬化区及血管瘤样区结构;2)乳头状腺瘤:好发于男性,中央型,呈乳头状生长,间质为纤维血管轴心,被覆立方到柱状的上皮细胞;3)类癌:呈乳头状排列时易与硬化性肺细胞瘤混淆,但后者免疫组化神经内分泌标记物染色阴性;4)腺癌:硬化性肺细胞瘤易与乳头状生长的浸润型腺癌混淆,尤其是冰冻时,但前者结构复杂,细胞形态温和;5)透明细胞肿瘤:由于硬化性肺细胞瘤间质圆形细胞可呈泡沫样或空泡样,因此要与此类肿瘤鉴别,免疫组化可有一定帮助。
3.4 治疗及预后虽然关于硬化性肺细胞瘤发生淋巴结或远处器官转移的病例相继被报道[9-10],但是硬化性肺细胞瘤仍然被认为是一种良性肿瘤,硬化性肺细胞瘤界限清楚,常单发,楔形肺切除是治疗硬化性肺细胞瘤的首选方案,术后一般不需要放疗、化疗等后续治疗,预后较好,本组8例患者随访至今,均无复发及转移。

