二硫化镍/氢氧化镍空心球的制备及其电容器性能研究
罗惜情,王同振,江苗苗,熊 凡,程凤如
(合肥工业大学化学与化工学院,安徽合肥230009)
超级电容器拥有充放电速度快、容量大、功率高、循环寿命长等优点,可作为绿色无污染小型储能元件[1]。超级电容器根据储能机理不同可分为双电层电容器和赝电容电容器,前者材料主要为碳[2],后者材料主要为过渡金属化合物[3]。过渡金属化合物因具有优良的电子导电性、高比电容等优点而受到研究者的青睐。过渡金属化合物主要包括过渡金属氧化物、氢氧化物、硫化物等。 MnO2[4]、NiO[5]、Co3O4[6]、NiCo2O4[7]等过渡金属氧化物,由于导电性较低,限制了其在赝电容方面的应用。而过渡金属硫化物具有电子电导率高、成本低、低毒性等优点,被广泛应用于锂离子电池、超级电容器、染料敏化太阳能电池等领域[8]。Zhu[9]用牺牲模板法成功合成了 NiS 空心球,并作为超级电容器电极材料,在电流密度分别为4.08、10.2A/g条件下分别具有 927、583 F/g 比电容。Dai[10]利用牺牲模板法合成了NiS2空心棱柱,在电流密度为5 A/g条件下具有1 725 F/g比电容,且在20 A/g电流密度下具有优异的循环稳定性。
笔者以硫纳米球作为自牺牲模板,通过直接沉淀法在其表面包覆一层 Ni(OH)2制备 S@Ni(OH)2前驱体,前驱体在低温煅烧去除模板的同时,硫作为硫源将 Ni(OH)2部分转化为 NiS2,得到多孔的NiS2/Ni(OH)2复合纳米空心球,并研究了其循环伏安、恒流放电等电化学电容性能。
1 实验部分
1.1 材料制备
1.1.1 硫纳米球的制备
向100 mL 0.04 mol/L的NaS2O3+质量分数为0.02%的PVP(聚乙烯吡咯烷酮)溶液中加入0.8 mL 10 mol/L的HCl溶液,磁力搅拌2 h,用去离子水离心洗涤数次,得到硫纳米球,将硫纳米球分散到100 mL质量分数为0.05%的PVP水溶液中[11]。
1.1.2 S@Ni(OH)2前驱体的制备
向硫纳米球分散液中加入50 mL 0.01 mol/L的Ni(NO3)2·6H2O(0.146 g)水溶液,搅拌30 min,加入0.291 g六亚甲基四胺,继续搅拌30 min,移入三口烧瓶中加热至90℃保持6 h,反应结束后用去离子水对产物离心洗涤数次,在60℃烘箱中干燥12 h,得到 S@Ni(OH)2前驱体。
1.1.3 NiS2/Ni(OH)2纳米空心球的制备
将 S@Ni(OH)2置于管式炉中,在 Ar气氛下以2℃/min的升温速率升温至250℃保持1 h,然后以5℃/min的降温速率降温至200℃保持4 h,自然冷却至室温得到NiS2/Ni(OH)2纳米空心球。
1.2 产物表征
样品的晶体学特征通过D/max-γB型X射线衍射仪(XRD)和 ESCALAB 220i-XL 能谱仪(XPS)进行分析。样品的结构和形貌通过SU8020场发射扫描电子显微镜(FESEM)和H-800透射电子显微镜(TEM)进行表征。采用NOVA 2200e型比表面和孔径分析仪表征样品的BET比表面积。
1.3 电化学性能测试
使用无水乙醇作为溶剂,将NiS2/Ni(OH)2纳米空心球、乙炔黑、聚四氟乙烯按质量比为8∶1∶1混合,超声1 h,放入80℃烘箱中干燥,使用辊压机将固体混合物压制成片,随后切割成大小均一的小薄片,然后置于80℃真空干燥箱中干燥12 h。称量电极片质量,用辊压机将电极片压入两片泡沫镍中。采用三电极体系,以制成的电极作为工作电极,以铂片作为对电极,选用Hg/HgO电极作为参比电极,以6 mol/L的KOH溶液作为电解液。使用CHI760D型电化学工作站,采用循环伏安法和恒电流充放电法等测试方法,对样品的电化学性能进行表征。
2 结果与讨论
2.1 产物的物相与组成分析
图1 是 NiS2/Ni(OH)2XRD 谱图。 NiS2/Ni(OH)2特征峰与立方晶相NiS2(JCPDS卡片No.11-0099)和六方晶相 Ni(OH)2(JCPDS 卡片 No.14-0117)标准特征峰基本吻合。在2θ为 27.25、31.59、35.31、38.37、45.31、53.65、58.76、61.16°的衍射峰对应 NiS2的(111)(200)(210)(211)(220)(311)(230)(321)晶面,在 2θ为 19.26、33.06、38.54、52.10、59.05、62.72°的衍射峰对应Ni(OH)2的(001)(100)(101)(102)(110)(111)晶面,说明 NiS2/Ni(OH)2纯度较高,基本可以确定组分是 NiS2和 Ni(OH)2。
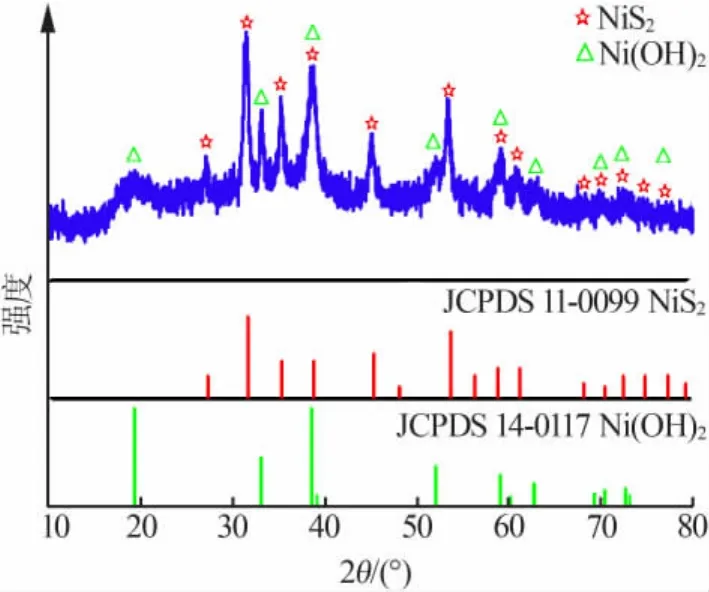
图1 NiS2/Ni(OH)2的 XRD 谱图
图2为 NiS2/Ni(OH)2的 XPS图。 在图 2b中,856.02、873.68 eV 的峰分别代表 Ni 2p3/2、Ni 2p1/2结合能特征峰,表明Ni是以Ni2+形式存在。在图2c中,162.43、163.66 eV 的峰分别代表 S 2p3/2、S 2p1/2结合能特征峰,表明S是以S22-形式存在;168.77 eV的峰代表S—O键,这是因为NiS2暴露在空气中,表面氧化成了SO32-/SO42-。在图2d中,531.50 eV的峰代表O 1s结合能特征峰,表明O是以OH-形式存在。
图3为 NiS2/Ni(OH)2的 EDX(X 射线能谱)图。从图 3 看出,Ni、S、O 原子比接近 1∶1∶1,通过计算可得 NiS2与 Ni(OH)2物质的量比约为 1∶1。
2.2 产物的形貌分析
图4 为 S@Ni(OH)2和 NiS2/Ni(OH)2FESEM 和TEM照片。NiS2/Ni(OH)2是大小均匀纳米球,空腔直径约为500 nm,表面覆盖超薄纳米片,长度约为250nm,整体形如花球,大小约为1μm。说明经过煅烧NiS2/Ni(OH)2形状保持完好,并具有多孔结构。这种结构可使电极材料比表面积增大,继而增大与电解液接触面积,从而加快电子传递可逆法拉第反应,有利于电解质离子进入和迁移,使材料得到充分利用。
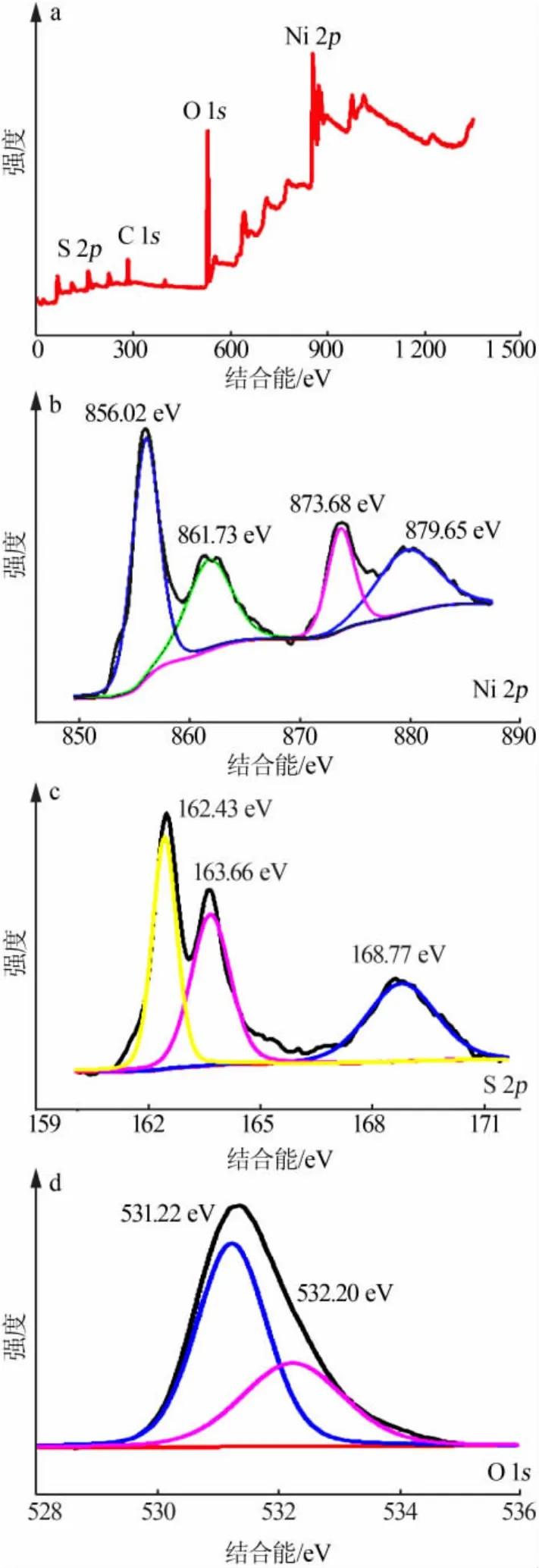
图2 NiS2/Ni(OH)2的 XPS 图
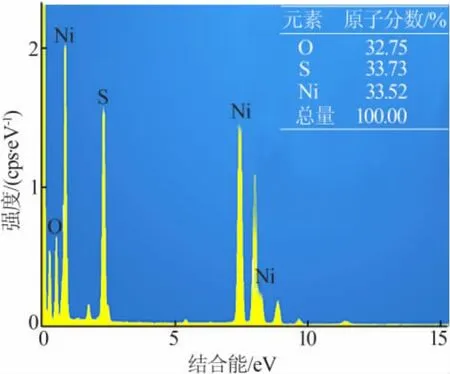
图3 NiS2/Ni(OH)2的 EDX 图

图4 S@Ni(OH)2(a、b)和 NiS2/Ni(OH)2(c、d)的FESEM和TEM照片
图5为 NiS2/Ni(OH)2的氮气吸附-脱附曲线。NiS2/Ni(OH)2的N2吸附-脱附等温曲线出现小的回滞环,属于Ⅳ型等温线。采用多点BET法可得产物的比表面积为87.16 m2/g。
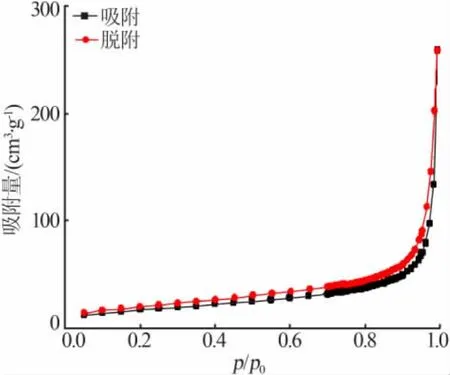
图5 NiS2/Ni(OH)2的氮气吸附-脱附曲线
2.3 电化学性能分析
图6a为不同电压扫速下循环伏安曲线。在电压窗口为0~0.6 V有一对氧化还原峰,证明了样品的赝电容特性。随着电压扫速增加,氧化峰从0.29V位移到0.25V,还原峰从0.38、0.44V极化到0.49V。
图6b为电极材料在不同电流密度下的充放电曲线。可通过公式计算电极材料的比电容Cm=C/m=I·Δt/ΔVm。 式中:ΔVm为放电电压,V;I为充放电电流,A;Δt为放电时间,s。 通过计算可得, 在 1、2、5、10、20A/g电流密度下,NiS2/Ni(OH)2复合纳米空心球的比电容分别为 1446、1335、1208、1100、976F/g。
图6c为不同电流密度下的比电容。随着电流密度增大,比电容略有下降,可见 NiS2/Ni(OH)2在碱性电解液中具有较好的比容量和倍率性能。
图6d为NiS2/Ni(OH)2在电流密度为10 A/g时连续充放电5 000次循环性能图。随着循环次数增加,材料比容量不断衰减,由1 100 F/g降至951 F/g,容量保持率为86.4%,具有良好的循环稳定性。
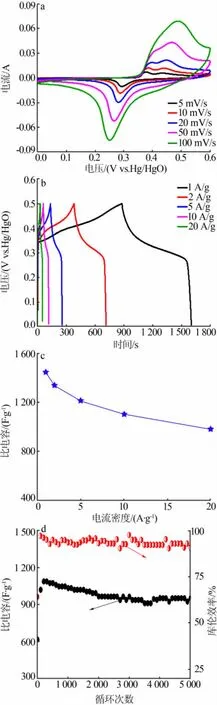
图6 NiS2/Ni(OH)2的电化学性能
3 结论
以硫纳米球为自牺牲模板和硫化硫源,使用直接沉淀法在其表面包覆 Ni(OH)2,在 250℃加热 1 h,获得多孔NiS2/Ni(OH)2复合纳米空心球,用其制备的电极具有良好的电化学性能。在1A/g电流密度下比电容可达到1 446 F/g,在20 A/g电流密度下比电容仍高达976 F/g。在10 F/g电流密度下循环5 000次,其比容量保持率为86.4%。其出色的电化学性能归因于其独特的花球形貌,该形貌有利于离子从电解液中向电极材料表面进行快速有效的扩散、电子的快速转移以及更好地适应充放电过程中材料的体积变化;其次,多孔结构具有更高的比表面积,能够为电化学反应提供更多的活性位点。NiS2/Ni(OH)2电极具有作为高性能超级电容器电极材料的潜能。

