乙型肝炎肝硬化合并肝性脑病的危险因素
王小琴 杨小丽
肝性脑病(HE)是各种原因导致的肝硬化失代偿期和肝病终末期较常见的、严重的并发症之一,在我国导致HE最常见的病因是乙型肝炎肝硬化[1]。HE预后较差,各种并发症较多,临床病死率较高,但至今的发病机制和病理基础尚未完全明了,不同研究的结论差异较大,大多患者在其疾病早期有明显的诱因和出现早期症状,临床早期发现、早期诊断和早期干预,对疾病的转归影响较大[2]。现就近年来的46例乙型肝炎肝硬化合并HE患者的高危因素进行分析,报道如下。
资料与方法
一、一般资料
选择我院感染科2017年1月—2018年10月收治的乙型肝炎肝硬化合并HE患者46例,列入观察组;其中男性25例,女性21例;年龄36~78岁,平均(52.6±5.4)岁。肝炎病史3~24年,平均(8.6±3.5)年;肝硬化病史2~21年,平均(6.5±3.2)年。选择同期住院未发生HE的乙型肝炎肝硬化46例,列入对照组;其中男性26例,女性20例;年龄35~79岁,平均(52.4±5.6)岁。肝炎病史3~25年,平均(8.4±3.6)年;肝硬化病史2~20年,平均(6.4±3.3)年。比较两组一般资料,具可比性(P>0.05)。
二、病例选择
(1)入选标准:所有患者均符合《慢性乙型肝炎防治指南》(2015年版)的诊断标准,有严重的肝病史,存在肝性脑病的可能诱因,出现精神错乱和意识障碍,扑翼样震颤,明显肝功能损害,血氨升高,典型脑电图改变等[3];伦理审核批准。(2)排除标准:肝胆恶性肿瘤,血液性疾病;胃肠瘘、烧伤、严重感染等导致的电解质紊乱和精神异常;原发性心肾功能不全,代谢性疾病。
三、研究方法
(1)对观察组患者按照病情的严重程度进行HE分期,并按照Child-Pugh分级法进行肝功能分期。从患者是否存在劳累、高蛋白饮食、电解质紊乱、合并感染、上消化道出血、肾功能不全、强利尿、放腹水、便秘、创伤、饮酒等方面进行统计,分析引发肝性脑病的各种因素的比例情况。
(2)分别对两组患者的性别、年龄、Child-Pugh评分、血清丙氨酸氨基转移酶(ALT)、白蛋白(Alb)、总胆红素(TBil)、尿素氮(BUN)水平,以及血钠、血氨、凝血酶原活动度(PTA)等指标进行比较,探寻诱发HE可能的危险因素[4]。
四、统计学方法
采用SPSS 20.0软件处理,计量和计数资料分别以和(n,%)表示,组间用t和χ2比较。P<0.05为差异有统计学意义。
结 果
一、肝性脑病的临床资料
在46例乙型肝炎肝硬化合并HE患者中,按照严重程度分期:Ⅰ期6例(13.04%),Ⅱ期16例(34.78%),Ⅲ期14例(30.43%),Ⅳ期10例(21.74%);按照肝功能Child-Pugh分级为B级14例(30.43%),C级32例(69.57%)。
二、肝性脑病各种危险因素的比例
在46例乙型肝炎肝硬化合并HE患者的各种可能诱发因素中,最多的是合并感染15例(32.61%),其次是上消化道出血9例(19.57%)、电解质紊乱7例(15.22%)和放腹水5例(10.87%),是乙型肝炎肝硬化患者引发HE的主要原因。其次为高蛋白饮食3例(6.52%)、强利尿3例(6.52%)、肾功能衰竭2例(4.35%)、手术创伤1例(2.17%)和便秘1例(2.17%)等。
三、肝性脑病危险的单因素分析
将两组患者的相关指标进行比较,在性别、年龄、ALT和BUN等方面,无显著差异(P>0.05);在Child-Pugh评分、Alb、TBil、血钠、血氨和PTA等方面,差异显著(P<0.05),可认为是肝性脑病的单因素。见表1。
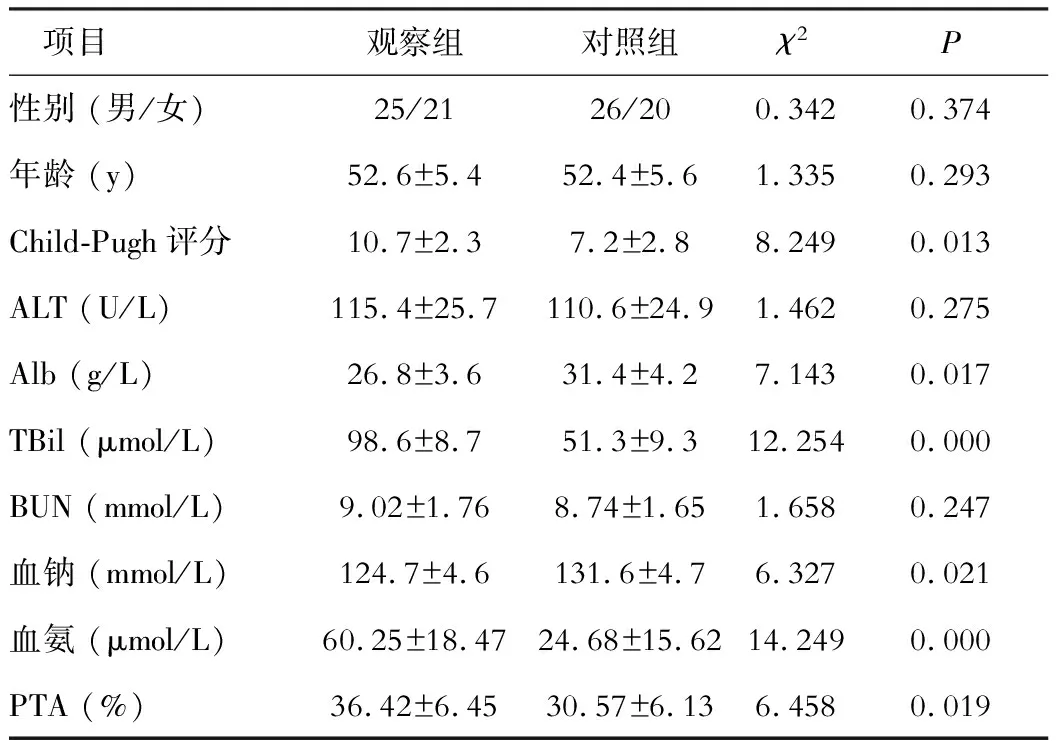
表1 两组单因素相关指标的比较
讨 论
在本研究中,将46例肝炎肝硬化合并HE患者按照疾病严重程度进行分期,最多的是Ⅱ期16例(34.8%),其次是Ⅲ期14例(30.4%);说明大多HE患者在疾病的早中期即可得到初步诊断和有效治疗,部分患者发展到Ⅳ期,疾病预后往往较差。将患者按照Child-Pugh分级进行肝功能评分,最多的是C级25例(54.3%),其次是B级21例(45.7%),并无A级病例发生HE,说明肝炎肝硬化患者的肝功能越差,发生HE的可能性越大。
肝硬化失代偿期患者免疫功能下降,肠道细菌分布异常、肺动静脉和门静脉分流、易致菌群失调,网状内皮细胞对细菌的清除能力下降,加上肝脏对抗菌药物的代谢能力减退,易引发各种感染的发生,炎症因子影响血脑屏障功能,易致脑细胞损伤和功能下降,诱发HE的发生[5]。患者并发上消化道出血后,血容量减少导致红细胞携氧能力下降使脑细胞缺血缺氧;肠道内的蛋白质生产增加,经肠道细菌的分解后,产氨显著增多,易致高氨血症从而诱发HE[6]。电解质紊乱时出现的低钠、低氯、低钾和代谢性碱中毒时,可促进氨的生成,增加机体对氨的吸收,从而导致血氨升高[7]。大量放腹水而白蛋白补充不足时,血浆蛋白质含量降低,电解质紊乱;腹内压突然降低,易使氨和其他有毒物质由肠道吸收;门静脉血管床扩张后,脑和肾脏的血液灌注量降低,引起脑和肾脏缺血缺氧,易致HE发生。本研究中,在可能导致和加重HE的各种诱发因素中,比例较高的分别是合并感染、上消化道出血、电解质紊乱和放腹水,临床上应及时发现这些高危因素的存在及早纠正。
Alb是由肝脏合成,具有运输营养物质、维持血浆胶体渗透压、抗凝血和清除氧自由基等功能,当Alb含量显著下降时,提示肝脏的合成功能和储备功能显著减退,疾病预后不良。肝
脏对血液中的胆红素具有摄取、结合和排泄功能,当肝细胞坏死和肝功能障碍时,TBil水平显著升高,与疾病的严重程度成正比。低钠血症与腹水的形成和严重性有关,反应肾脏对水钠排泄功能下降,抗利尿激素的增加,可致星形细胞水肿,改变多种蛋白和RNA,影响下丘脑结构和大脑功能,易致HE发生[8]。高氨血症干扰脑的能量代谢和神经递质的转运,谷氨酰胺蓄积导致星形细胞损伤和基因表达紊乱,从而导致中枢神经系统功能障碍,诱发HE[9]。凝血酶原和多种凝血因子在肝脏内合成,PTA时反映肝脏凝血功能和储备功能的一个重要指标,当PTA显著降低时,提示肝细胞坏死和肝功能损害的程度较严重。在本研究中,两组患者的Child-Pugh评分、Alb、TBil、血钠、血氨和PTA等指标比较差异显著(P<0.05),可认为是肝性脑病发生和加重的单因素。
综上所述,乙型肝炎肝硬化合并HE患者的疾病分期大多为Ⅱ期和Ⅲ期,多发生在Child-Pugh肝功能C级的患者;引发HE的主要原因为合并感染、上消化道出血电解质紊乱和放腹水等,HE的单因素为Child-Pugh评分、Alb、TBil、血钠、血氨和PTA等指标,在临床工作中应注重这些致病原因和高危因素的存在,及早发现和干预纠正,以改善疾病预后。

