温和条件下氢氧化钠高效异构葡萄糖制备果糖研究
李陆杨,张 怡,李晓璇,关 昕
(承德石油高等专科学校 化学工程系,河北 承德 067000)
将葡萄糖高效异构为果糖是利用生物质资源制备多种平台化合物如5-羟甲基糠醛、乙酰丙酸及乳酸等的重要中间步骤[1]。以果糖为前驱体的制备过程目标产物产量高、反应条件较温和、可简化/减少催化剂的使用。因此,通过异构作用将葡萄糖转化为果糖具有很大的科研和实际意义。目前,最常用的两种葡萄糖异构手段是酶催化法和化学催化法[2],葡萄糖异构酶催化制备果糖的工艺已经在食品和制药领域得到了大规模应用,但酶的生产成本高,对工艺条件环境敏感,容易失活,给酶催化法的使用和发展造成很大的阻碍[3]。化学催化法主要涉及两类催化剂:碱催化剂和Lewis酸催化剂[4]。碱催化剂包括以同相催化起作用的传统碱土金属氢氧化物、有机碱,以及以异相催化起作用的固体碱催化剂如金属氧化物、类水滑石材料等。Lewis酸催化剂则包括一大类Sn-/Ti-beta分子筛材料,以及部分金属卤化物如CrCl3、AlCl3[5]。近期的研究热点主要集中于异相固体催化剂的制备和应用,主要的思路包括有机碱的固载化、水滑石/沸石材料结构的有序调控等。Yang等[6]合成了基于氯甲基树脂和二氧化硅包覆铁氧化物的固定化有机碱,这两种新型固体碱可在120 ℃的反应条件下得到约25%的果糖产率,铁磁材料还具有相当的稳定性和可重复利用性。Chen[7]等通过热解咖啡豆和三聚氰胺的混合物得到一种固体碱生物碳,这种材料在160 ℃时可高效催化葡萄糖异构并得到约14%的果糖产率。Chadwick课题组[8-10]研究了一系列NaY型沸石的改性方法,发现镁盐和碱处理过的沸石有较好的异构作用,反应温度为100 ℃时最大的果糖产率可达35%。固体催化剂在分离和使用过程中具有一定优势,但目前所制备的材料的催化效率都较低,并未体现较好的循坏利用性能,且制备方法大多需要煅烧等耗能过程,原料和辅助溶剂有一定毒性,其实际应用性受到了严重制约。本文利用传统的碱性催化剂氢氧化钠,开发了高效异构葡萄糖制备果糖的温和体系,研究了反应时间、温度、催化剂量、底物浓度等条件的影响。结果表明氢氧化钠在较低温度下(50 ℃)具有比其他催化剂在高温下(80~160 ℃)更好的异构效果,果糖产率和选择性高达40.1%和83.2%,具有很好的应用潜力。
1 实验部分
1.1 实验试剂及仪器
葡萄糖、果糖、氢氧化钠、氢氧化钾、氢氧化钙、氢氧化镁、氢氧化钡等,均为分析纯,上海阿拉丁生化科技有限公司;稀硫酸溶液(0.5M),色谱级流动相,上海麦克林生化科技有限公司。
DSHZ-300A型回旋式水浴恒温振荡器,苏州培英实验设备有限公司;ACQUITY UPLC H class型超高效液相色谱、ACQUITY UPLC TUV型紫外检测器、ACQUITY RI示型差折光检测器,美国沃特世公司;SH-1011型糖类色谱柱,日本昭和电工株式会社。
1.2 实验方法
催化实验在自制具塞玻璃瓶中进行。称取0.18 g葡萄糖溶于20 mL去离子水中,向此溶液中加入0.02 g氢氧化钠。将此混合液迅速转移到预设至不同温度的恒温水浴摇床中,在100 r/min的转速下浸泡相应时间,取出后冰浴降温停止反应,吸取反应液进行分析测定。
1.3 产物分析
葡萄糖转化率、果糖产率及相应中间产物的测定由液相色谱完成,色谱使用条件为:5 mmol/L稀硫酸为流动相,流速为0.5 mL/min。紫外检测器波长设为210 nm,示差检测器流通池温度35 ℃,色谱柱温50 ℃。所有实验结果由三次平行实验平均所得。
葡萄糖转化率、果糖产率、果糖选择性均以含碳量的摩尔百分数表示,具体计算公式如下:



2 结果与讨论
2.1 催化剂的筛选
在之前的工作中我们发现[11],碱金属氢氧化物(Ba(OH)2、NaOH)可以在室温(25 ℃)、厌氧条件下对葡萄糖异构为果糖起到一定的催化作用。但此系统平衡时间较长(48 h),厌氧条件需要复杂的反应装置。为了加速和简化反应过程,提出了以简便的自制玻璃容器为反应装置,在中温、空气气氛进行的反应系统,并对常用碱金属氢氧化物NaOH、KOH、Ca(OH)2、Mg(OH)2、Ba(OH)2的异构效果进行了筛选,结果见表1。
由表1可以看出,在相同OH-浓度的条件下,单价金属氢氧化物在果糖产率和选择性方面均优于二价金属氢氧化物。NaOH的果糖产率和选择性分别可以达到40.1%和83.2%。Mg(OH)2的果糖选择性最高,但其转化葡萄糖并产生果糖的能力很低,这主要受限于其极低的溶解度。二价金属氢氧化物的葡萄糖转化率与单价金属氢氧化物相似,但是果糖产率更低,这主要是由于二价金属离子对果糖进一步转化的催化作用。因此,单价金属氢氧化物更适合于葡萄糖催化异构制备果糖的过程,本文选取NaOH作为后续实验的催化剂。
2.2 时间和温度对反应的影响
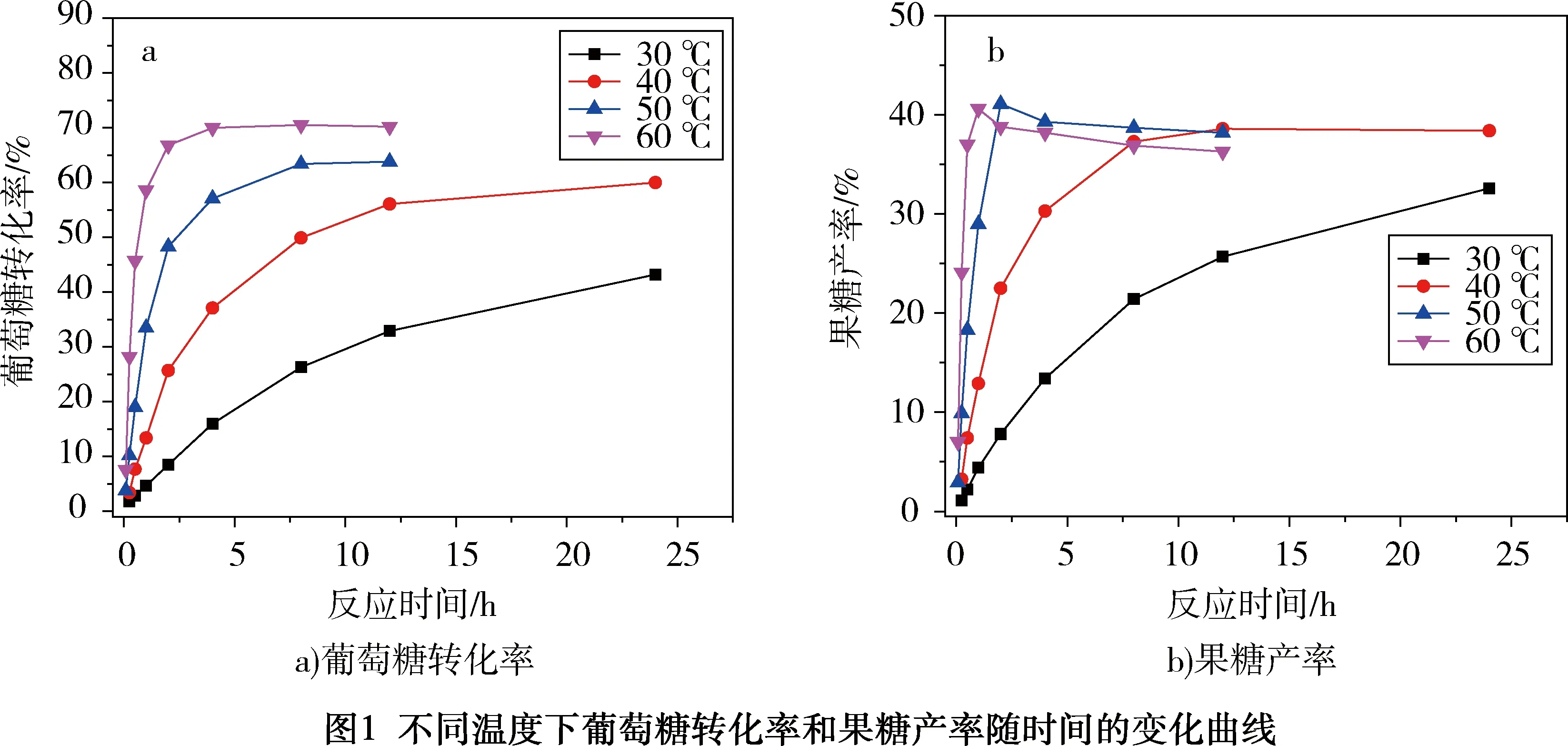
起始反应条件设定为碱/葡萄糖浓度比0.025 mol/L ∶0.05 mol/L,为了加速异构过程并抑制副反应发生,选取较低的温度范围(30 ℃、40 ℃、50 ℃、60 ℃)进行实验。图1显示了不同温度下,葡萄糖转化率和果糖产率随时间的变化曲线。在低温(30 ℃)时,葡萄糖的转化速率极慢,大约需要72 h才
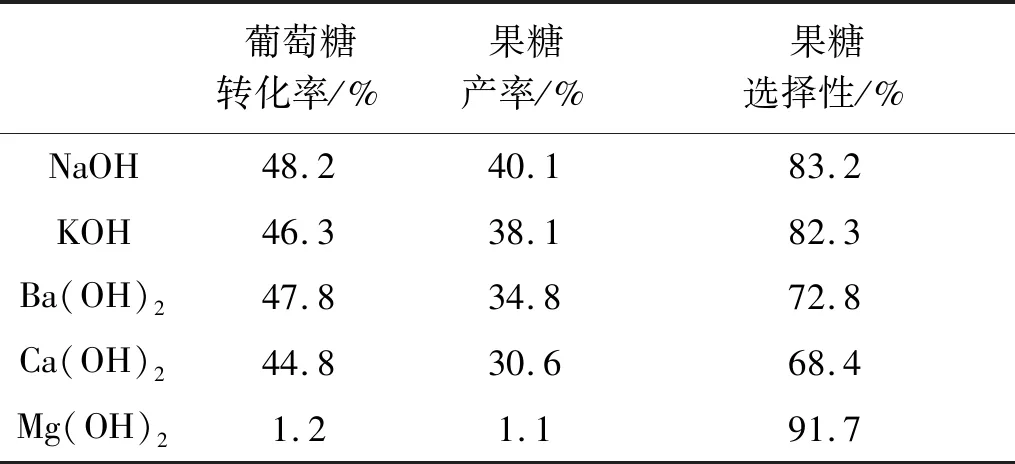
表1 不同碱金属氢氧化物的葡萄糖异构性能
反应条件:50 ℃,0.025 mol/L OH-,0.05 mol/L葡萄糖,2 h
能达到反应平衡。当温度提高到40 ℃时,反应速率加快,平衡时间可被缩短至约48 h。在中温区(50 ℃、60 ℃),葡萄糖转化速率显著加速,平衡时间可分别减小至8 h和4 h。此外,温度的变化对葡萄糖转化率的最终值影响不大,均在60%~70%,高温时转化率稍高一些。从这一结果看,温度的提高可以极大加速葡萄糖转化速率,提高体系的实际应用性能。
不同温度下果糖选择性随温度的变化趋势如图2所示。由结果可知,在反应温度为30 ℃、40 ℃和50 ℃时,所有曲线都在约1.5 h处产生转折,较高的温度下出现拐点的时间会提前,而60 ℃下的曲线则呈现连续的下降趋势。这表明高温加速了果糖的进一步分解,且在异构过程中必然存在一个最优的时间条件,满足高效制备果糖的需要。60 ℃条件下混合物的颜色随时间延长有明显的改变(见图3),着色物为糖类脱水、缩合等过程的副产物,这一现象不利于果糖的积累。根据上述实验结果,本系统最优条件组合为50 ℃下反应2 h。


2.3 碱添加量和葡萄糖浓度的影响
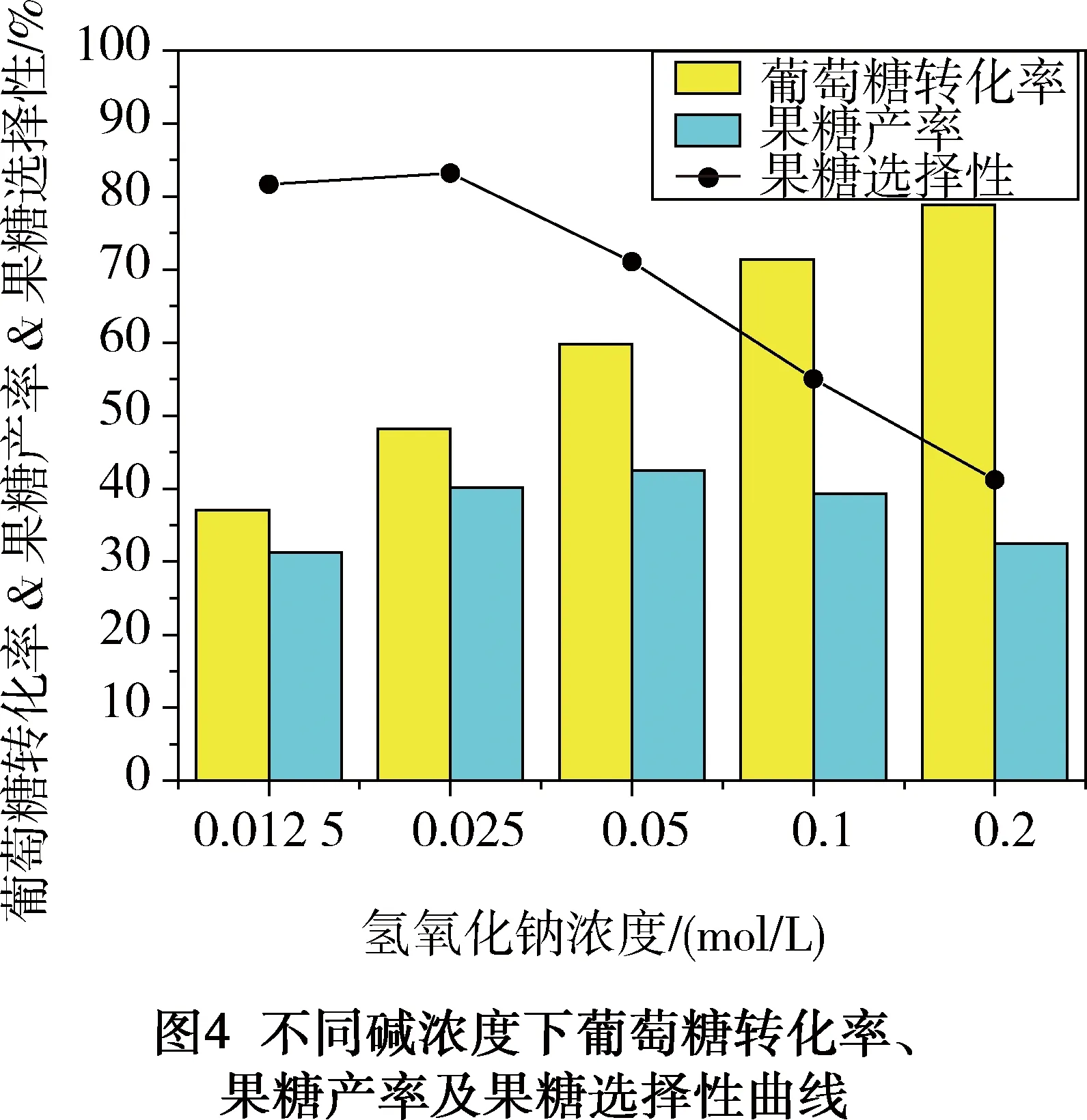
不同碱添加量对葡萄糖的异构作用如图4所示。从图4可以看出,葡萄糖转化率随碱浓度的增加而增加,低浓度(0.0125 mol/L)的氢氧化钠仅能转化约35%的葡萄糖,而高浓度(0.2 mol/L)时葡萄糖转化率可达80%以上。果糖产率在碱浓度为0.05 mol/L时达到最大值42.5%,并随着碱浓度的增加而降低。果糖选择性受碱浓度影响较大,当碱浓度大于0.025 mol/L后,其曲线呈明显的下降趋势。实验结果表明,最佳碱浓度为0.025 mol/L,其葡萄糖转化率为48.2%,果糖产率为40.1%,果糖选择性为83.2%。
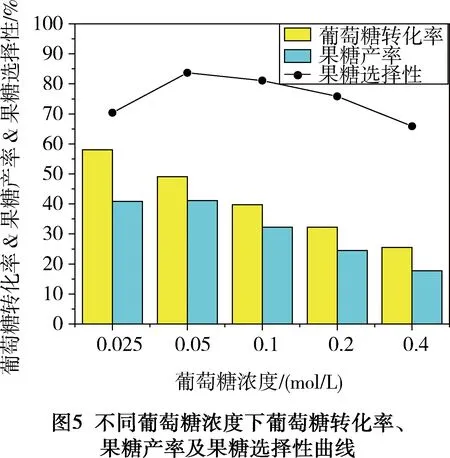
葡萄糖浓度对异构作用的影响如图5所示。随着葡萄糖浓度的增加,其转化率逐渐降低,较低的葡萄糖浓度有利于异构的发生以及果糖的积累。当起始葡萄糖浓度低于0.05 mol/L时,果糖产率可达40%以上。果糖选择性则呈现先增加后降低的趋势。对于较低的起始葡萄糖浓度,葡萄糖转化率和果糖的分解率均较高,过多的果糖分解导致最终选择性的下降。高浓度的葡萄糖则限制了催化剂的催化作用,而使异构效果不佳。综合考虑,碱/葡萄糖最佳配比为0.025 mol/L ∶0.05 mol/L。
2.4 碱催化剂应用展望
以氢氧化钠为催化剂的葡萄糖异构体系显示出了很大的简便性及高效性。相比于其他需要经过复杂途径制备的催化剂,氢氧化钠具有更高的效率,更简便的操作体系,不需要耗能、有污染的制备过程。表2总结了目前文献报道的多种固体催化剂的异构效果。从表2中不难看出,本体系采用的方法具有操作温度低、异构效率高、果糖产率大等特点,同时避免了煅烧、浸泡等处理步骤,有很大优势。
此外,本体系终产物混合液成分主要包含葡萄糖和果糖,其组成与传统酶法催化制备的果葡糖浆相似,利用膜分离、吸附法以及色谱分离纯化等方法即可得到较纯净的产品。
3 结论
利用氢氧化钠作为催化剂可以在温和条件下高效异构葡萄糖制备果糖,当碱/葡萄糖比为0.025 mol/L ∶0.05 mol/L,反应温度为50 ℃,反应2 h时,果糖产率可达40.1%,选择性为83.2%。与其他固体催化剂相比,氢氧化钠无需复杂合成过程,无能耗,且催化效率高,具有较大优势。本体系结构简单,产物组成与酶法制得的果葡糖浆类似,具有实际应用前景。
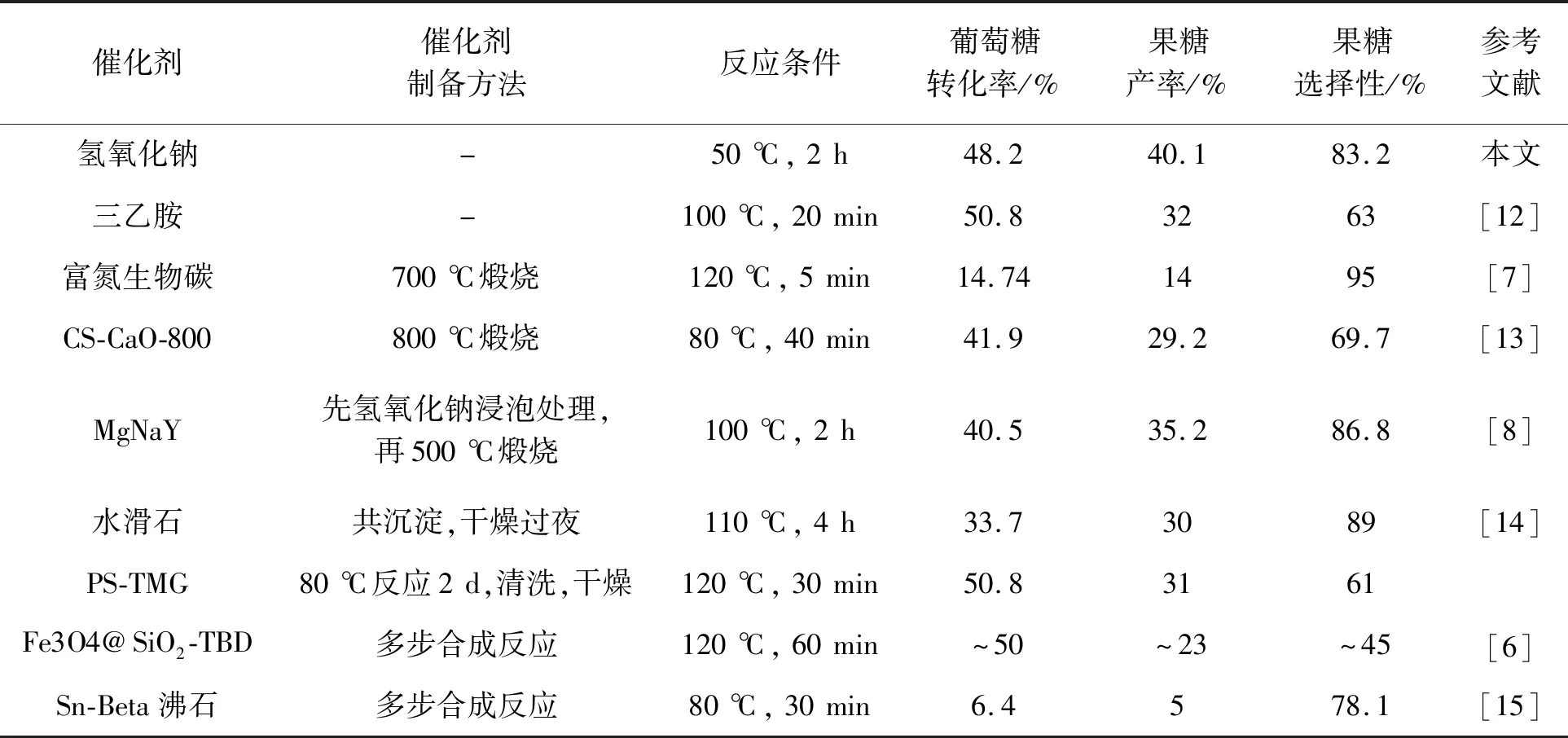
表2 不同催化剂的制备及异构效果

