内生和根际细菌对棉花防御酶活性诱导和黄萎病防治作用
李雪艳,党文芳,杨红梅,3,楚敏,3,高雁,曾军,霍向东,张涛,林青,欧提库尔,李玉国,娄恺,史应武,3*
(1.新疆农业科学院微生物应用研究所/ 新疆特殊环境微生物实验室,乌鲁木齐830091;2.新疆大学生命科学与技术学院,乌鲁木齐830052;3.农业农村部西北绿洲农业环境重点实验室,乌鲁木齐830091)
棉花黄萎病严重影响棉花产量和纤维品质,是限制棉花生产最主要病害之一[1-2]。拮抗细菌诱导抗性防治棉花黄萎病的研究尚处于初级阶段[3],探索拮抗菌对棉花诱导抗性对该土传病害防治具有重要指导价值和理论意义。
在我国,棉花黄萎病是由大丽轮枝菌引起的土传病害,目前还未攻克其防治技术的原因主要是大丽轮枝菌无明显的寄主专化性、致病机理复杂、传播途径多、高抗品种抗性丧失快、微菌核能长期存活等[4]。棉花黄萎病防治一直是棉花种植业关注的热点问题,目前常见的防治方法包括农业防治、化学药剂防治和生物防治。生物防治由于绿色、安全等特点已成为学者优先选择的研究对象。植物诱导抗性是生物防治黄萎病的途径之一。植物诱导抗性又称植物免疫或系统获得抗性,是指植物受到外界刺激后,既快又强地提高自身免疫防御酶[包括过氧化氢酶(Catalase)、过氧化物酶(Peroxidase)、超氧化物歧化酶(Superoxide dismutase)、苯丙氨酸解氨酶(Phenylalanine ammonia lyase)、 多酚氧化酶 (Polyphenol oxidase)]活性和抗菌性植保素、酚类、丙二醛等含量,形成自我保护的天然屏障,阻碍病原菌的侵染。在众多的生防菌中,枯草芽孢杆菌(Bacillus subtilis)凭借分布范围广、易培养、抗逆性强、广谱抑菌等优点而受到青睐[5-6]。有很多报道表明,芽孢杆菌能激发植株诱导抗性达到抑制病原菌生长、繁殖、侵染的目的,例如:Akram 等发现芽孢杆菌菌株在分根系统和田间条件下能诱导番茄对枯萎病的抗性[7];乔俊卿等发现枯草芽孢杆菌PTS-394 能诱导番茄对灰霉病产生抗性[8];赵玉华等报道枯草芽孢杆菌EBS05 产生的surfactin诱导烟草对花叶病毒(Tobacco mosaic virus)产生抗性[9],张亮等也发现芽孢杆菌对番茄诱导抗性是其防治番茄枯萎病的机理[10],张涛等发现芽孢杆菌防治棉花黄萎病机理与诱导抗性有关[11],周京龙等也发现棉花内生蜡状芽孢杆菌YUPP-10能诱导植物防御反应来抵抗病原菌的侵染和扩展[12]。综上,利用拮抗菌对植株的诱导抗性是防治棉花黄萎病的有效途径之一。
本实验室从新疆棉花植株根际及体内分离筛选出4 株芽孢杆菌属拮抗菌,但其防治棉花黄萎病的机理与棉花诱导抗性相关的防御酶是否相关还不清楚。因此,本研究通过平板培养检测4株芽孢杆菌的拮抗性,通过温室盆栽试验统计其对棉花黄萎病的防治效果,并检测棉花叶片中防御酶活性变化,为生物防治棉花黄萎病提供新途径及科学依据。
1 材料与方法
1.1 主要材料
供试棉花品种:新陆早36 号。
供试菌株:由本实验室从新疆棉花植株根际及体内分离筛选,鉴定为Bacillus vanilleaSMT-24(根际),B.velezensisBHZ-29(内生),B.subtilisSHT-15(根际),B.atrophaeusSHZ-24(内生 ),GenBank 登录号分别为:MG470750、MG470759、MG470679、MG470659。大丽轮枝菌由新疆农业科学院植物保护研究所刘海洋提供。
盆栽土壤:新疆农业科学院实验基地提供。
培养基:营养肉汤(Nutrient broth,NB)培养基,营养琼脂(Nutrient agar,NA)培养基,查比克(Czapek)培养基,马铃薯葡萄糖琼脂(Potato dextrose agar,PDA)培养基。
1.2 方法
1.2.1供试细菌及大丽轮枝菌发酵液制备。采用划线法分离拮抗菌单菌落,用竹签挑取单菌落接种至NB 液体培养基,500 mL 三角瓶装液量为50 mL,30 ℃、180 r·min-1振荡培养 2 d 后作为发酵液,将发酵液按照3%体积量接入NB 培养基,NB 培养基每500 mL 三角瓶装液量为200 mL,30 ℃、180 r·min-1振荡培养 6 d 即为拮抗菌发酵液(活菌含量 108mL-1)。将 4 ℃保存的大丽轮枝菌竹签挑取少许菌块倒贴接种到PDA 固体平板培养基上,25 ℃恒温培养15 d 后,用打孔法制备直径6 mm 的小菌饼。查比克培养基每个500 mL 三角瓶装液量为200 mL,每瓶接种15个菌饼,28 ℃、150 r·min-1振荡培养 7 d 即为大丽轮枝菌培养液。
1.2.2供试菌株拮抗性检测。将大丽轮枝菌发酵原液(孢子含量 107mL-1)稀释至 10-2,震荡均匀,用移液器取 100 μL 于 PDA 平板培养基,混匀涂布,用直径6.00 mm 的打孔器打孔,挑去孔内PDA,将100 μL 拮抗菌发酵液加入孔内,放置于28 ℃恒温培养箱培养4 d,拍照记录结果。
1.2.3棉苗盆栽种植。将180 ℃灭菌3 h 的无菌土装至种植棉花卡槽的2/3 处放置托盘中,灌水至托盘,表层土壤湿润后将颗粒饱满的棉种每槽种植2 粒,覆土3 cm,抚平轻压表层土壤,放置于智能培养箱出苗,播种后常规温室管理,昼/ 夜光照时间与温度分别为13 h/11 h、26 ℃/24 ℃,相对湿度60%,光照强度6 万lx。
1.2.4大丽轮枝菌伤根法接种。打开种植棉花的塑料卡槽,将长至两叶一心的棉苗距根底部2~3 cm 处用剪刀人工伤根,每卡槽棉株伤根处灌溉大丽轮枝菌培养液 (孢子含量 105mL-1)10 mL,合紧卡槽放置托盘,全部标记为VD,在智能培养箱继续培养。
1.2.5接种拮抗菌。接种大丽轮枝菌6 d 后,将SMT-24、BHZ-29、SHT-15、SHZ-24 菌 株 发 酵 液(活菌含量 108mL-1) 均以每槽 10 mL 均匀灌溉棉苗根部表层土壤,每种拮抗菌各灌溉3 盆作为3 个平行试验(每盆 4 列 7 行,共计 28 个卡槽)。标记处理组编号为(VD+SMT-24,VD+BHZ-29,VD+SHT-15,VD+SHZ-24),对照 VD 接种同体积灭菌NB 培养基,继续放置于智能培养箱培养,拮抗菌发酵液分3 次灌溉,每次间隔6 d。
1.2.6拮抗菌在根部土壤中的定植量。第3 次接种拮抗菌2 d 后,每处理每个平行试验取1 行卡槽中棉苗,取苗后将根部土壤抖落收集,混匀,自然风干,称量5 g 于250 mL 三角瓶,加入灭菌生理盐水 45 mL,25 ℃、180 r·min-1振荡 2 h,取10-4、10-5稀释梯度在 NA 固体培养基上涂布,放置在30 ℃恒温箱培养2 d,根据4 株拮抗菌的菌落形态进行菌落计数,菌落数在30~300 之间的平板作为菌落计数标准,5 d 取样1 次,共计数5 次。
1.2.7棉株生物量测量。将1.2.6 步骤中的棉苗根部冲洗干净,随机选择每处理组及对照组4~7株棉苗,统计棉苗的株高、根毛数、叶片数、根长。
1.2.8叶片保护酶活性的测定。参照Mahunu等[13]的方法处理1.2.5 得到的棉苗叶片,提取粗酶液,用于检测 POD、PPO、CAT、SOD 活性,其中用硼酸盐缓冲液(pH 8.8)代替磷酸钠缓冲液,其余操作不变,上清液用于检测PAL 活性。以OD值变化 0.01 为 1 个酶活力单位(U),POD、PPO、CAT 的OD值 10 s 记录 1 次,共计 1 min,PAL记录30 min 内OD值变化,活性以每克新鲜组织质量(U·g-1)表示。
POD 活性测定:参照文献[14]的方法配制溶液及测定,加入试剂依次为0.1 mL 粗酶液,0.03 mL 质量分数0.3%的愈创木酚、2.84 mL 磷酸缓冲液(50 mmol·L-1,pH 6.4),混匀后于 30 ℃水浴中保温 5 min,加入 0.03 mL 质量分数 0.3%的H2O2(50 mmol·L-1,pH 6.4 磷酸钠制备),以加入0.03 mL 蒸馏水作对照,调零后立即在470 nm 波长处测量吸光度值。
PPO 活性测定: 依次加入1.9 mL 磷酸缓冲液 (0.05 mol·L-1,pH 6.8) 和 1 mL 0.02 mol·L-1邻苯二苯酚溶液,混匀后于30 ℃水浴中保温5 min 后加入0.1 mL 粗酶液,以蒸馏水代替粗酶液作对照调零,立即在398 nm 波长处测定。
CAT 活性测定:反应混合物由2.87 mL 磷酸钠 缓 冲 液 (50 mmol·L-1,pH 7.0),0.1 mL 40 mmol·L-1H2O2和 0.03 mL 粗酶液组成,以蒸馏水代替酶液作对照调零,记录240 nm 波长处吸光度下降值。
PAL 活性测定: 反应混合物由2.7 mL 硼酸缓冲液 (0.1 mol·L-1,pH 8.8),0.2 mL 的 L- 苯丙氨酸(0.02 mol·L-1,用硼酸缓冲液配制),0.1 mL粗酶液组成,混匀后在290 nm 处立即测定初始值,放置30 ℃下反应30 min 后立即取出,在290 nm 波长下测定吸光值。
SOD 活性测定:参照 Wang 等[15]的测定方法微修改为光照强度60 万lx,光照时间为2 min。
1.2.9病情调查和统计[16]。第3 次接种拮抗菌株后2 d 时,调查病情指数,统计每盆后3 行棉苗。以株为单位,统计发病叶片数与每株总叶片数,发病等级=(患病叶片数/每株总叶片数)×4。分级按照 5 级分类标准:0 级,无病植株;1 级,(0,25%]叶片发病的植株;2 级,(25%,50%]叶片发病的植株;3 级,(50%,75%]叶片发病的植株;4级,75%以上叶片发病的植株。按照下列公式计算病情指数: 病情指数=(∑各级病株数×相应病级)/(总株数×最高病级)×100。
2 结果与分析
2.1 供试菌株在平皿中对大丽轮枝菌的抑菌作用
由图1 可知,4 株拮抗菌均表现出良好的抑制大丽轮枝菌的作用。从抑菌现象看,SMT-24 菌株抑菌效果最好,其次为BHZ-29 菌株,SHT-15与SHZ-24 效果较差。从拮抗结果看,4 株菌株均可作为潜在的黄萎病生防菌。
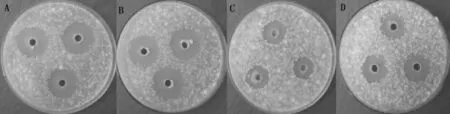
图1 平皿检测4 株菌对大丽轮枝菌的抑菌作用Fig.1 Plate detection of four strains of bacteria against Verticillium dahliae
2.2 棉苗根部拮抗菌定植数量
棉苗根部拮抗菌定植数量结果(图2)显示,菌株BHZ-29 和 SHZ-24 在土壤中的适应性良好,定植量较高,菌株SMT-24 次之,菌株SHT-15定植量较低。菌株 SMT-24、BHZ-29、SHZ-24 在接种后2~7 d 内定植量均下降,接种后7~22 d,菌株 SMT-24、SHZ-24 定植数量逐渐增加,而BHZ-29 菌株在接菌后7~17 d 逐渐增加,17~22 d 又下降。菌株 SHT-15 在接菌后 2~7 d 数量减少较快,7~22 d 数量变化小。在接菌后 2~22 d,SMT-24、BHZ-29、SHZ-24 的定植数量与 SHT-15差异显著。
2.3 拮抗菌对棉株的促生作用

图2 4 株拮抗菌在棉苗根部的定植数量随时间变化的动态Fig.2 Dynamics of colonization of four strains of antagonistic bacteria in cotton seedling roots with time
由图3 趋势可知,拮抗菌接种后2~22 d,处理组株高、叶片数和根毛数与对照组相比均有一定程度的升高,但根长处理组与对照组相比无明显的升高。VD+SMT-24、VD+BHZ-29 处理组中平均株高在2~17 d 时间段呈现增长趋势,VD+SMT-24、VD+SHT-15 处理组平均叶片数及平均根毛数在2~17 d 时间段也呈现增长趋势,其他处理组无明显规律。由多重比较结果可知,株高除 VD+SHT-15 接种后 7 d、VD+SMT-24 接种后 2 d,VD+BHZ-29 接种后 2 d、7 d 和 VD+SHZ-24 接种后 2 d、12 d 外,其他时间点处理组均显著高于对照组;根毛数除VD+SMT-24 接种后2 d 和VD+SHZ-24 接种后17 d 外,其余时间点处理组均和对照差异显著; 根长除VD+SMT-24 接种后 22 d、VD+SHZ-15 接种后 12 d和VD+BHZ-29 接种后17 d 外,其他时间点处理组与对照组差异均不显著;4 株拮抗菌处理组的叶片数均显著高于对照组。上述结果表明,4 株拮抗菌处理提高了棉株株高、 叶片数和根毛数,能促进棉株生长。

图3 拮抗细菌接种后对棉株株高、根长、叶片数和根毛数的影响Fig.3 Effect of antagonistic bacteria on plant height, root length, number of leaves and number of root hairs of cotton plants after inoculation
2.4 防御酶活性测定
由图4 可知,接种后 SMT-24、BHZ-29、SHT-15、SHZ-24 菌株在一定时间内可提高棉叶CAT、SOD、POD、PAL 活性。CAT 活性除 VD+SMT-24接种后 17 d 和 22 d、VD+BHZ-29 接种后 17 d和 22 d、VD+SHT-15 接种后 7 d 和 22 d、VD+SHZ-24 接种后 2 d、17 d 外,其余时间点处理组与对照组 (VD) 差异均显著; 除接种后7 d 外,VD+SMT-24、VD+BHZ-29、VD+SHT-15 处理组其余时间点SOD 活性均高于对照组,VD+SHZ-24 处理组在接种后12~22 d 内 SOD 活性高于对照组; 在接种后 17~22 d,VD+SMT-24、VD+BHZ-29 和 VD+SHZ-24 的处理组 PAL 活性均高于对照组; 菌株处理组棉叶POD 活性在接种后12~22 d,均高于对照组;而PPO 活性在接种后2 d 时,处理组和对照组差异显著,其中仅VD+BHZ-29 高于对照组,7~17 d 之间处理组与对照组无明显差异,在接种后22 d 时,仅VD+BHZ-29、VD+SHT-15 与对照组差异显著,且高于对照组。

图4 拮抗菌对系统诱导酶活性的影响Fig.4 Effect of antagonistic bacteria on system-induced enzyme activity
2.5 拮抗菌对棉花黄萎病的防治效果测定
测定4 株菌株对棉花黄萎病的防治效果,结果如图5A 所示,对照组与处理组棉苗已经出现感病症状,子叶部分感病。由图5B 病情统计结果可知,对照组棉苗病情指数达15.08,与处理组差异显著。处理组中,SMT-24、SHT-15 菌株病情指数较低,分别为 3.88 和 3.44;BHZ-29 菌株病情指数较高,SHZ-24 菌株病情指数最高,分别为4.17、5.49。从病情指数结果得出,4 株拮抗菌均能在一定程度上控制棉花黄萎病,其中SHT-15防治效果最好,SMT-24、BHZ-29 次之,SHZ-24较差。
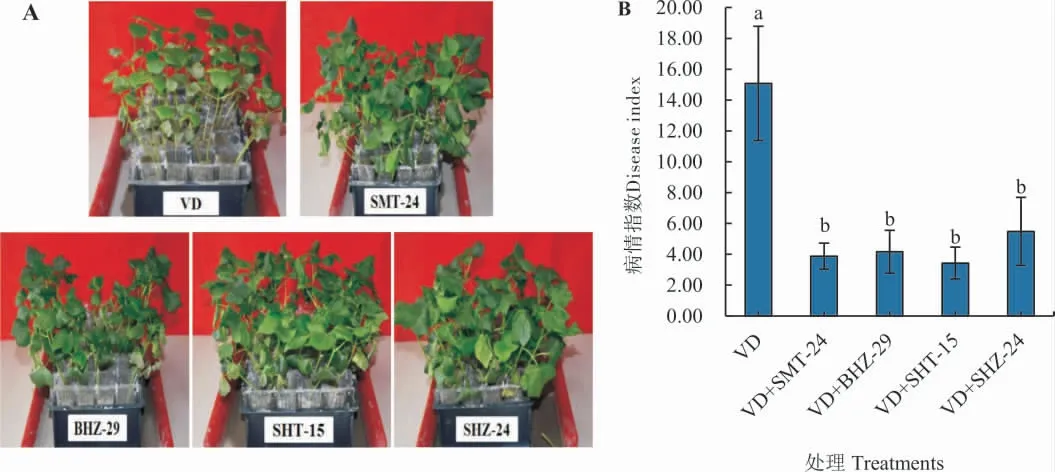
图5 棉花黄萎病发病程度与病情指数统计分析Fig.5 The degree and statistical analysis of disease index of cotton Verticillium wilt of each treatment
3 讨论
3.1 拮抗菌株SMT-24、BHZ-29、SHT-15、SHZ-24对棉花防御酶系的诱导作用
本研究选用新疆本土芽孢杆菌菌株研究其对棉花防御酶系的诱导作用,为更科学防治当地棉花黄萎病提供理论支撑,并为棉花黄萎病的防治提供物质储备。平皿试验结果说明,4 株拮抗菌均可以抑制大丽轮枝菌的生长繁殖。接种后,SMT-24、BHZ-29、SHZ-24 在根系土壤中的活菌数出现先下降再上升的趋势,SHT-15 菌株定植数量随着时间减少,说明4 株拮抗菌均可在根系土壤定植,占领根系生态位,并且 SMT-24、BHZ-29、SHZ-24 菌株比 SHT-15 更加适应土壤的环境。加入4 株拮抗菌一定程度上提高了棉苗的株高、根毛数、叶片数,说明4 株拮抗菌能不同程度促进棉苗的生长。刘玉涛等也报道了相似研究结果:2 株链霉菌D74 和Act12 提高防御酶活性的同时促进植株的生长[17]。
防御酶 CAT、SOD、PAL、PPO、POD 是植物体内抵制病原侵染的有关物质,其活性的变化通常作为衡量植物体内防卫反应的重要指标[5]。CAT 在植物细胞内清除H2O2和维持其在正常水平,减轻活性氧所造成的损伤[18];POD 能够防止活性氧引起伤害,调控细胞内自由基水平[19];SOD是植物体内的抗氧化剂,将O2-转化成诱导植物产生抗病性的起始激发分子H2O2;PAL 调控酚类物质、木质素合成[20]。本研究中,接种拮抗菌在一定时间范围内能提高棉花CAT、SOD、PAL、POD活性,说明接种4 株拮抗菌能刺激棉花体内部分防御酶活性在一段时间内提高,并不是持续诱导提高防御酶活性。
3.2 防治效果及不足
温室盆栽试验表明,4 株拮抗菌均可显著降低棉花黄萎病的病情指数,并表现出良好的土壤环境适应能力,但拮抗菌还是会受大田地域、气候条件、土壤理化性质等影响,应用大田后是否能达到预期防治效果,是否能稳定持久,还需长时间、多地域的田间试验验证[21-22]。
4 结论
在温室中,4 株芽孢杆菌属细菌均可抑制大丽轮枝菌生长,定植于棉花根系土壤中,提高棉株株高、叶片数、根毛数,并显著降低棉花黄萎病病情指数,通过在一定时间内提高棉花防御酶CAT、SOD、PAL、POD 活性,增强棉花抗病性。

