基于新药研发能力培养的药理学实验教学探索
高越颖, 刘 蕾, 任怡琳, 耿 燕
(江南大学 药学院, 江苏 无锡 214122)
0 引 言
制药工程专业是培养具有新药研究与开发的基本能力、有较扎实的制药工程设计基础知识、并具有一定的研究、解决制药工程实际问题能力的人才。我校制药工程专业作为教育部特色专业、江苏省品牌专业,在人才培养过程中,尤其注重学生综合能力的培养。从人才培养方案、教学大纲及教学过程都突出了制药企业对学生的实际需要,从新药研发实际出发强化学生开放性思维的培养。药理学作为专业核心课程之一,在江苏省精品课程建设理念的基础上,形成了“基础-综合-开放创新”层次鲜明的开放式实验课程体系,药理学设计性实验主要目的是培养学生的科学研究能力和创新能力[1-3]。
以前期课程(如药物化学实验)中合成的产品或学院科研团队研究成果为研究对象,设置了药效学评价、药代动力学研究及毒性评价等研究方向,学生根据自己的擅长和兴趣自愿组合,4或5人1组,查阅文献、确定研究方向、设计实验方案,老师组织学生对各组的实验方案进行科学性及可行性的论证,每个同学都参与讨论。最后,根据实验设计的水平和实验室实际条件进行筛选整合,形成1或2个可实施的设计性实验。实验结束后各小组整理实验结果,进行汇报分享,每个同学都要按国家标准论文格式写一篇论文。通过开展设计性实验,不仅能培养学生的创新思维,综合运用理论知识及新药研发能力[4-6],也能够为教师科研工作中开展药物合成或工艺的改进提供实验依据。
1 实验原理
药食用真菌是世界公认的具有良好疗效的药食同源物质,灵芝发酵菌丝体粉(以下简称灵芝菌粉)是学院较成熟的科研成果,有抗氧化、抗毒性以及免疫调节的功效[7],为探究其安全范围,设计了急性毒性实验,为促进其合理开发利用提供科学依据。
急性毒性是指动物一次或24 h内多次接受一定剂量的受试物,动物在短期内出现的毒性反应。传统的急性毒性以动物死亡为判断指标,与动物保护的“3R”原则严重冲突,而且对于毒性较低的受试物为求出LD50动物使用量大、死亡率高,故本研究应用固定剂量法,对其毒性表现进行观察[8-10]。通过实验学生能够直观观察到不同剂量下灵芝菌粉是否存在毒性表现,还可通过血清生化指标、主要器官的病理切片验证其毒性。
2 试剂及仪器
药品与试剂:灵芝菌粉为灵芝发酵的菌丝体经喷雾干燥后得到的粉末。其余试剂均为国产分析纯。
实验动物:健康ICR小鼠,SPF级,40只,体重(20±2)g,由扬州大学实验动物中心提供。饲养温度25 ℃,相对湿度55%。
仪器:艾本德5810R离心机,德国Eppendorf 公司;科华卓越310全自动生化分析仪,上海科华生物工程股份有限公司;KD-BM生物组织包埋机,浙江金华市科迪仪器设备有限公司;KD-BL包埋冷冻台,浙江金华市科迪仪器设备有限公司;YT-6C生物组织摊烤片机,湖北孝感市亚光医用电子技术有限公司;LEICA RM2135切片机,德国LEICA 公司;Olympus BX41生物显微摄影系统,日本Olympus公司。
3 实验方法
3.1 实验动物分组及给药
小鼠随机分成灵芝菌粉4个剂量(50、500、2 000、5 000 mg/kg)组[11],另设对照组,每组8只,雌雄各半且分笼饲养。灵芝菌粉各组一次性灌胃(ig)给予相应药物水溶液,给药前禁食4 h,自由饮水,给药体积10 mL/kg。对照组小鼠ig等体积蒸馏水。
3.2 一般状态观察
给药后观察小鼠的外观,包括皮毛、呼吸、鼻眼、口腔有无异常分泌物等,观察小鼠的精神状态,大、小便等情况;各剂量组小鼠观察不以死亡为指标,而以明显的毒性反应为指标。详细观察给药后4 h内小鼠反应情况,然后每天上午、下午各观察一次,连续观察14天[12-13]。
3.3 指标测定
小鼠给药后14天后颈椎脱臼法处死小鼠,摘眼球取血,进行大体解剖肉眼观察有无明显病变,并取脑、胸腺、心、肝、脾、肾等脏器称质量,计算脏体比,脏体比=器官重/小鼠体重 ×100%。血液室温静置1 h后,3 000~4 000 r/min离心,取上清,-20℃保存,用于生化指标测定。血清AST,ALT采用全自动生化分析仪进行分析[14-15]。
3.4 重要脏器形态学观察
小鼠给药后14天,脱颈致死,速取心、脑、肺、肝、脾、肾新鲜组织,于10%福尔马林固定,常规浸蜡包埋5 μm切片,切片脱水脱蜡,苏木素-伊红(Hematoxylin- Eosin,HE)染色[16]。
3.5 统计学分析
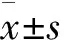
4 实验结果
4.1 各剂量组小鼠一般观察
给药后各剂量组小鼠体型正常,背不弓起,行动迅速,被毛浓密有光泽,呼吸正常,食欲良好,粪便颜色、质地正常。外观形态与对照组无区别。
4.2 小鼠脏体比
灵芝菌粉一次性给药14天后,各剂量组各器官外观颜色、大小均正常,未见明显萎缩、水肿、渗出、增生等病变。各剂量器官指数与对照组比较均无显著差异(见表1)。
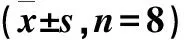
表1 灵芝菌粉对小鼠器官指数的影响
4.3 小鼠血清生化指标
天冬氨酸转氨酶(AST或GOT)和丙氨酸氨基氨酶(ALT或GPT)合称转氨基酶,肝受损后,内源性转氨酶释放到细胞外,使得血清中的转氨酶水平成为肝脏损伤的重要指标[12]。与对照组相比,给药后低剂量组小鼠血清AST、ALT均未出现显著差异(见表2)。可见灵芝菌粉对小鼠血液生化指标无明显影响。
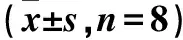
表2 灵芝菌粉对小鼠组织血清生化指标的影响
4.4 主要脏器病理学检查
对照组的心肌细胞正常,肝细胞轮廓清晰,可见核仁,中央静脉完整,肺被膜完好,肺泡间隔内有少量淋巴细胞浸润,肾组织结构完整,脑组织皮层可见典型的椎体细胞,胶质细胞排列整齐,高剂量组5 000 mg/kg小鼠的心、肝、肺、肾、脑切片染色后光镜检查结果也未见任何特异性病理改变。
综上,灵芝菌粉在最高剂量5 000 mg/kg给药时,小鼠生长良好,脏体比、血清生化指标与对照组比均无显著差异(P>0.05),主要器官病理组织学检查结果也表明灵芝菌粉对受检脏器无明显损害,因此有着良好的口服安全性。
5 结 语
灵芝孢子粉的急性毒性试验是学生十分感兴趣的选题,激发了学生的求知欲,从实验设计到结果分析学生感到有较大的挑战性,实验技能得到了提高。通过文献调研,学生对药物急性毒性研究的基本概念、基本原则和主要研究内容和实验方法,有了较全面的学习;实验实施过程中,小鼠灌胃、取血、解剖取材等实验动物基本技能操作得到了复习巩固,此外学生还接触了血清生化测定、病理切片染色等多门学科综合实验技术技能,培养了动手实践能力、创新意识及科研兴趣。
当然在设计性实验过程中也发现了一些问题,例如:设计实验方案时,很多学生没有考虑到药食用菌的低(无)毒,设计了LD50这个指标;取血经验不够,导致有些小鼠取血量偏少;取材过程中未将器官取完整造成实验误差,另外统计技能的缺乏也是学生进行数据处理的主要障碍。尽管本实验还有一些不尽如人意的地方,但是通过实践与摸索,该实验将不断完善。

