超高液相色谱-高分辨质谱联用测定苦玄参的化学成分
陈 晖,丘 琴
(广西中医药大学药学院,广西 南宁 530200)
苦玄参,又名蛇总管、鱼胆草、落地小金钱、四环素草,为玄参科植物苦玄参Picria felterrae Lour.的干燥全草,分布于广西、广东、贵州和云南南部等地,具有清热解毒、消肿止痛之功效。临床常用于风热感冒、咽喉肿痛、喉痹、痄腮、脘腹疼痛、痢疾、跌打损伤、疖肿、毒蛇咬伤。电喷雾离子源质谱具有灵敏度高、操作简便、分子离子峰丰度高等优点,本实验采用超高效液相色谱-高分辨质谱(UPLC-Triple TOF-MS)联用技术初步分析苦玄参的化学成分,为苦玄参的临床应用提供理论参考。
1 实验材料
1.1 仪器 色谱仪器为岛津LC-30A 超高液相色谱系统:包括二元高压梯度泵、自动进样器、柱温箱、二极管阵列检测器(DAD);质谱仪器为AB Sciex Triple TOF 5600+,XEVO G2-S QTOF∕MS质谱系统和Masslynx 4.1质谱工作站;SQP电子天平[赛多利斯科学仪器(北京)有限公司];优普Ulupure 实验室超纯水仪(上海优普实业有限公司)。
1.2 试药与试剂 实验用苦玄参全草1批,2018年11月采自广西梧州,经广西一心医药马利飞副主任中药师鉴定为玄参科植物苦玄参Picria felterrae Lour.的干燥全草。甲醇(默克股份两合公司,批号:JB034007);乙腈(色谱纯,批号:JA034131)和甲酸(色谱纯,批号:JC034117)均为默克股份两合公司产品;95%乙醇(分析纯,批号:170505)为西陇化工股份有限公司产品;甲醇(分析纯,批号:20170920)为国药集团化学试剂有限公司产品;水为纯净水。
2 方法和结果
2.1 供试品的制备 称取苦玄参全草1 g,精密称定,加入70%乙醇在90 ℃恒温水浴中加热回流1 h,过滤,滤液置于水浴锅上蒸干,残渣用甲醇溶解,转移至2 ml 的容量瓶中,用甲醇定容至刻度线,摇匀,将溶液转移到离心管,高速离心10 min(13 000 r∕min),将上清液过0.22 μm微孔滤膜,备用。将样品放入4 ℃冰箱保存,保存时间不超过24 h。
2.2 色谱条件 色谱柱为C18(1.8 μm,2.1 mm×100 mm);柱温40 ℃;流速为0.3 ml∕min;进样量为2 μl;流动相采用乙腈(B)-0.2%甲酸(A)水溶液的梯度洗脱:0 min(5%B),0.1~37 min(5%~30%B),37.1~40 min(30%~5%B)。
2.3 质谱条件 离子化模式为电喷雾正离子模式,离子源电压分别为5 500 V,离子源温度为600 ℃,去簇电压(DP)分别为100 V,碰撞能量(CE)分别为35 eV,碰撞能量扩展(CES)分别为15 eV。雾化气体为氮气,辅助气1为60 PSI,辅助气2 为50 PSI,气帘气为40 PSI。一级质谱母离子扫描范围为50~1 000,IDA 设置响应值超过100 cps 的6 个最高峰进行二级质谱扫描,子离子扫描范围为50~1 000,开启动态背景扣除(DBS)。
离子化模式为电喷雾负离子模式,离子源电压分别为-4 500 V,离子源温度为500 ℃,去簇电压(DP)为100 V,碰撞能量(CE)为-35 eV,碰撞能量扩展(CES)为15 eV。雾化气体为氮气,辅助气1 为60 PSI,辅助气2 为50 PSI,气帘气为40 PSI。一级质谱母离子扫描范围为50~1 000,IDA 设置响应值超过100 cps 的6 个最高峰进行二级质谱扫描,子离子扫描范围为50~1 000,开启动态背景扣除(DBS)。
3 结果与讨论
3.1 苦玄参供试品溶液的总离子流图 在ESI正离子模式下,苦玄参供试品溶液的总离子流图见图1;在ESI 负离子模式下,苦玄参供试品溶液的总离子流图见图2。
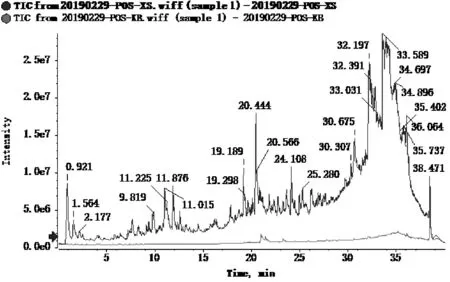
图1 正离子模式下苦玄参提取物的总离子流图

图2 负离子模式下苦玄参提取物的总离子流图
3.2 数据分析 采用高分辨质谱对数据库中的活性成分匹配,定性分析苦玄参中药活性成分。苦玄参醇提取液在正负离子模式下共检测到33种中药活性成分,其中响应强度大于10 000的中药活性成分共有19种,其中推测出10种成分。见表1。
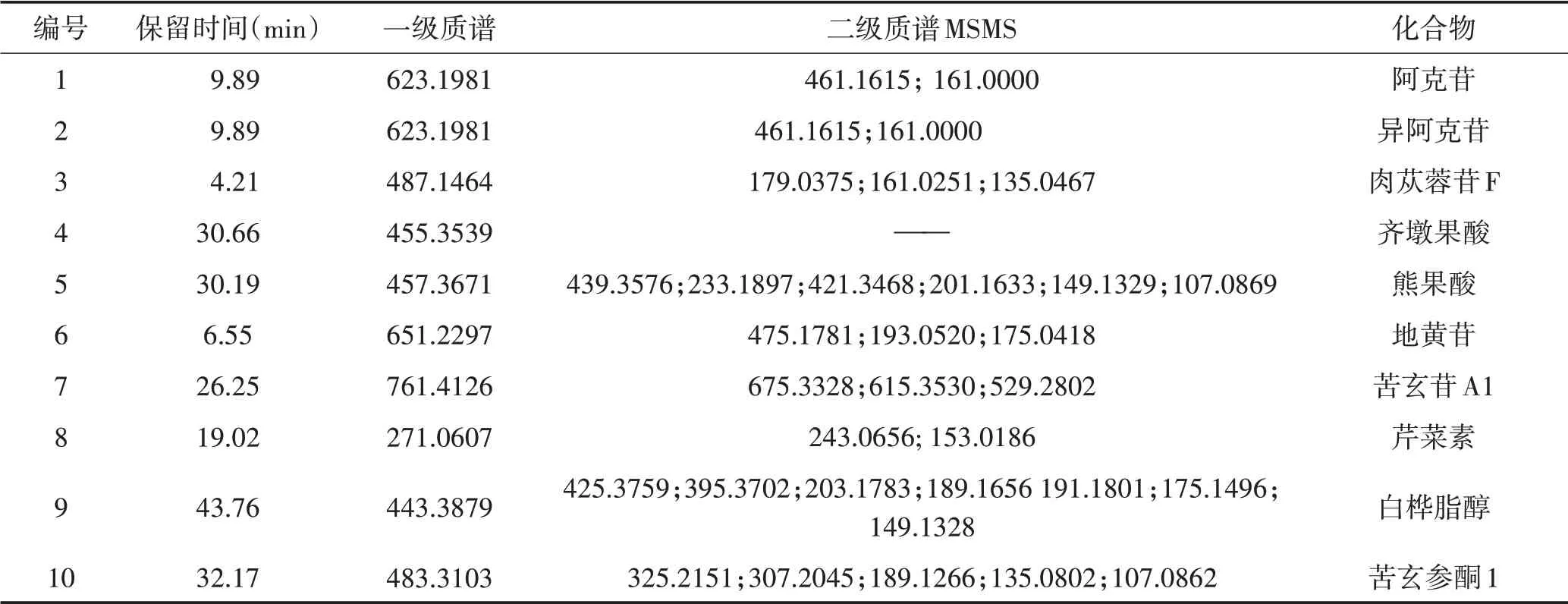
表1 苦玄参的化学成分分析结果
化合物1:一级质谱图中存在离子峰[M-H]-(m∕z 623.1981),理论计算值为623.1975(calcd for C29H35O15),高分辨质谱实测获得的精确质量与理论计算值高度一致,得出此化合物的分子式为C29H36O15;其二级质谱中检测到主要碎片离子峰(m∕z 461.1615),(m∕z 161.0000),推测(m∕z 461.1615)离子是化合物丢失一个162Da 的咖啡酰基产生的,m∕z161.0000 是咖啡酸负离子脱水的产物,因此推测化合物结构有咖啡酰基,结合文献[1-2],推测该化合物是阿克苷。
化合物2:在提取离子流图中tR=9.89 min 处还有一个强度很大的离子峰,对应的一级质谱基峰为[M-H]-(m∕z 623.1981),其理论计算值为623.1975(calcd for C29H35O15),此化合物的二级质谱裂解的碎片离子与化合物1完全一致,显示有咖啡酰基的信号,即化合物2 和化合物1 为同分异构体。据文献报道,含有不饱和芳香酰基的顺反异构体在混合溶液中会互相转化而达到平衡[1],故推测该化合物可能为一对顺反异构体,结合文献[1],推测该化合物是异阿克苷。
化合物3:一级质谱中存在较强的离子峰[M-H]-(m∕z 487.1464),在负离子模式下,高分辨质谱实测获得的精确质量与理论计算值高度一致,得出此化合物的分子式为C21H28O13,该化合物在二级质谱下裂解的主要碎片离子峰有(m∕z 179.0375),该碎片离子为咖啡酸脱去一个H+得到,(m∕z 161.0251)为咖啡酸脱去一份子水得到,(m∕z 135.0467)该碎片离子为咖啡酸脱去H-CO2所得,结合文献[3-4],推测该化合物为肉苁蓉苷F。
化合物4:在提取离子流图中tR=30.66 min峰对应的一级质谱基峰为m∕z 455.3539,在负离子模式下该化合物的[M-H]-离子理论值质荷比为(m∕z 455.3531),与实验测量值仅相差0.00353 Da,根据元素组成和参考文献,推测该化合物分子式为C30H48O3,该化合物在负离子模式下比较稳定,没有裂解的二级质谱,故推测该化合物为齐墩果酸[5]。根据文献[3]可知齐墩果酸广泛存在于玄参科多种植物中。
化合物5:该化合物是在正离子模式下裂解,化合物一级质谱图存在正离子[M+H]+(m∕z 457.3671),因此计算出分子式为C30H48O3,根据文献[5],该化合物在正离子模式下不稳定,极易发生裂解,主要碎片离子有m∕z 439.3576,m∕z 233.1897,m∕z 421.3468,m∕z 201.1633,m∕z 149.1329 等。其二级质谱中丰度较大的碎片离子(m∕z 439.3576),是由准分子离子(m∕z 457.3671)失去一分子水形成。结合文献[6],推测该化合物是熊果酸,是齐墩果酸的同分异构体,该化合物广泛存在于玄参科多种植物中。
化合物6:该化合物在负离子模式下发生裂解,其一级质谱图存在较强离子峰[M-H]-(m∕z 651.2297),其理论计算值为651.2288(calcd forC31H40O15),与实验测量值仅相差0.0009 Da。二级质谱中检测到的碎片离子峰(m∕z 475.1781)[M-H-Feruloyl]-为化合物脱掉阿魏酸所得,(m∕z 193.0520)[M-H-HMP]-,(m∕z 175.0418)[M-HHMP-H2O]-,这些碎片离子峰与文献[10]报道一致,故推测该化合物是地黄苷,地黄苷广泛存在于玄参科多种植物中[11]。
化合物7:该化合物在负离子模式下裂解,一级质谱中存在负离子[M-H]-(m∕z 761.4126),因此计算出分子式为C41H62O13,化合物的二级质谱中存在碎片离子(m∕z 675.3328)、(m∕z 615.3530)、(m∕z 529.2802),其中碎片离子(m∕z 615.3530)[M-146-H]-提示分子中存在一个鼠李糖,以上数据与文献中报道苦玄苷A1 的MS 的数据一致[1],故推测该化合物为苦玄苷A1。苦玄苷A1 是苦玄参重要的有效成分[7]。
化合物8:该化合物在正离子模式下发生裂解,其一级质谱图中存在较强离子峰[M+H]+(m∕z 271.0607),其理论值(m∕z 271.1348),高分辨质谱实测获得的精确质量与理论计算值高度一致,因此得出此化合物的分子式为C15H10O5,其二级质谱中检测到碎片离子(m∕z 243.0656)、(m∕z 153.0186)与文献报道的数据一致[1],故推测该化合物为芹菜素,据文献报道,芹菜素是苦玄参中的主要成分之一,能在苦玄参的醇提液中检测到该化合物[2,7]。
化合物9:该化合物在正离子模式下发生裂解,一级质谱中存在离子峰[M+H]+(m∕z 443.3879),其理论值(m∕z 443.3884),实验测得值与理论值高度一致,故该化合物的分子式为C30H50O2,在二级质谱检测到重要碎片离子(m∕z 425.3759)[M+H-H2O]+;(m∕z 203.1783)[M+H-C15H26OH2O]+与文献[8]报道的相关数据一致,故推测该化合物为白桦脂醇。白桦脂醇是苦玄参种子的成分之一[9]。
化合物10:该化合物在正离子模式下发生裂解,其一级质谱中存在较强离子峰[M+H]+(m∕z 483.3103),计算出其分子式为C30H42O5,二级质谱中检测到的碎片离子峰(m ∕z 325.2151)为[M+H-C8H11O2-H2O]+所 得,(m ∕z 307.2045)为[M+H-C8H11O2-H2O-CH3-H]+所得,(m∕z 189.1266)为[M+H-C17H26O4]+所得,上述碎片离子峰与文献[12]报道一致,故推测该物质为苦玄参酮1。
4 小 结
本实验采用液质联用技术,对苦玄参的醇提物进行初步研究,发现提取物中含有三萜类、黄酮类、环烯醚萜苷类和多种苯丙酸(如肉桂酸、咖啡酸等),以及葡萄糖、鼠李糖等缩合成苷化合物,因而同系物较多。通过主要离子峰和碎片离子峰信息,推测出其中10种化合物。
本实验鉴定的化合物大多数源于对已知化合物的筛查,对未知化合物进行结构确认仍较为困难,尤其是同分异构体及同系物,需要结合C谱、H谱等技术进一步分析,以获得化合物的准确结构。本实验可为苦玄参的化学成分研究提供依据,也可为苦玄参的临床应用提供参考。
——碳正离子的产生及稳定性比较

