利用小鼠骨骼肌细胞持续表达单链胰岛素类似物进行1型糖尿病模型鼠的长效基因治疗
杨平,苏若珂,邓璐,杨月瑶,王刚
(四川大学生物材料工程研究中心,成都610064)
1型糖尿病是由于过度免疫反应导致胰岛β细胞被破坏,致使胰岛素缺乏,进而引起高血糖和一系列威胁生命的并发症。该类患者需要每日注射胰岛素来维持体内血糖的正常水平,这给患者带来许多的麻烦、痛苦和风险。基因治疗以其简便、经济、来源充足、疗效持久等优势引起大众关注,且以腺病毒、逆转录病毒、腺相关病毒、裸质粒等作为临床试验中的代表(Yoon &Jun,2002;Handorfetal.,2015)。然而,前三者来源于病毒,存在感染性、容量有限、操作复杂等局限性,而相对安全的裸质粒却有严重的体内转染效率低下问题。骨骼肌作为基因治疗的重要平台之一,有以下特点:(1)是重要的糖代谢组织,在全身分布广泛,且肌纤维的使用寿命较长、再生能力较强,即使受损后也能继续发挥生物学功能(Blaverietal.,1999);(2)一些哺乳动物的组织,尤其是骨骼肌,能够自发地吸收不与脂质络合的外来质粒(Konetal.,1999);(3)高度血管化的肌肉允许重新合成的蛋白质分泌到体循环中(Kessleretal.,1996;Olfertetal.,2001)。因此,骨骼肌是利用裸质粒作为基因治疗载体进行胰岛素异位分泌的潜在平台之一。然而,肌肉、肝脏等组织由于缺乏β细胞特定反应酶而无法直接利用胰岛素基因表达出高活性成熟胰岛素。因此,本研究首先将胰岛素基因序列中的C肽换成灵活的柔性肽linker(GGGGS)3(Kuferetal.,1997),再使用Pluronic L64-电脉冲体系来提高裸质粒的体内传递效率(Liuetal.,2014),旨在通过这套外源胰岛素基因在骨骼肌原位高效传递的系统来提高1型糖尿病小鼠的体内基因治疗效果,以实现胰岛素长期、有效的分泌,进而能为减少患者每日注射胰岛素的身心痛苦提供一定的实验依据。
1 材料和方法
1.1 实验动物
从成都达硕实验动物有限公司[实验动物生产许可证号:SYXK(川)2015-030]预订足量6~8周龄雄性BALB/c小鼠,适应性喂养1周,每笼放置6~8只小鼠,并且在湿度45%~65%、21 ℃的环境中饲养,动物房规范提供12 h日照和12 h黑夜环境。所有实验均得到相关伦理委员会认可,并且按照规定和制度操作[实验动物使用许可证号:SYXK(川)2013-07]。所有实验分为4个组:(1)正常小鼠(NC)组;(2)以pcDNA3.1(+)空质粒为对照的糖尿病小鼠,并且进行Pluronic L64-电脉冲治疗,即L/E-pcDNA3.1(+)组;(3)仅使用含单链胰岛素类似物基因的裸质粒治疗组,即pcDNA-INS组;(4)以含单链胰岛素类似物基因的pcDNA-INS质粒和Pluronic L64-电脉冲进行联合治疗的糖尿病小鼠,即L/E-pcDNA-INS组。空腹血糖水平与生存率最初检测时以每组12只进行实验,在单次治疗后的4周内进行观察和检测,其余指标为每次每组4只进行取样检测。
1.2 试剂及仪器
相关试剂材料主要包括:质粒小量提取试剂盒(Omega)、限制性内切酶及相关试剂(Fermentas)、胶回收试剂盒(Omega)、连接酶及相关试剂(Invitrogen)、质粒大量提取试剂盒(Invitrogen)、BCA蛋白含量检测试剂盒(Thermo)、胰岛素ELISA试剂盒(mlbio)、链脲佐菌素(STZ)(Sigma)、血糖检测试纸(罗氏)、Pluronic L64(Sigma-Aldrich)、相关抗体和染色剂(Cloud-Clone Corp和Abcam)、pcDNA3.1(+)质粒为实验室前期购买并且保存、含有胰岛素类似物基因的质粒PUC57由成都擎科梓熙生物技术有限公司合成并提供。相关仪器主要包括:凝胶成像系统(ChemiDocTM XRS+,Bio-Rad),NanoDrop2000(Thermo)、SDZ-Ⅴ型电脉冲治疗仪(华佗)、多功能酶标仪(Varioskan Flash,Thermo)、血糖检测仪(罗氏)、数码三目摄像显微镜(BA400Digital)。
1.3 实验方法
1.3.1 质粒的制备与鉴定从NCBI上找到所需胰岛素基因序列(NM_008386.4),分析信号肽、胰岛素B链、胰岛素A链、胰岛素C肽等各部分的序列,将C肽的序列删除,替换成柔性肽序列(GGGGS)3,并在两端加上酶切位点(EcoRⅠ和BamHⅠ),送成都擎科梓熙生物技术有限公司合成,并构建到PUC57载体上。将空载体pcDNA3.1(+)或PUC57质粒(含胰岛素类似物基因)在含氨苄抗生素的平板上活化,进行质粒小提鉴定,再根据设计的酶切位点进行双酶切,按照说明书步骤进行胶回收、连接反应等操作,构建好含胰岛素的载体pcDNA-INS后,将其进行酶切鉴定后测序,确认无误后对质粒进行大量提取。将所需质粒浓度调至约5 000 ng·μL-1进行分装,-20 ℃(短期)或-80 ℃(长期)保存。
1.3.2 模型建立及治疗STZ放在低温、干燥、避光环境中保存,按照要求配制1%枸橼酸缓冲液(pH4.2~4.5),4 ℃预冷。将小鼠禁食不禁水喂养过夜,并以180~250 mg每公斤体质量一次性腹腔注射STZ溶液,对照组以同样方式注射不含STZ的等量1%枸橼酸缓冲液。注射后第3天开始检测小鼠血糖值,大于16.7 mmol·L-1并且稳定7~14 d则视为糖尿病模型构建成功。治疗时,NC组注射等体积的生理盐水。质粒配制及Pluronic L64-电脉冲体系的使用:以生理盐水稀释终浓度0.1%L64与60 μL质粒形成治疗混合物,室温放置5 min,并将小鼠两侧的胫骨前肌脱毛,在两侧等量注射治疗混合物,1 h后对小鼠2条腿的胫骨前肌进行电脉冲治疗(参数设置为5 Hz,3 min),单点单次注射,观察4周左右。
1.3.3 血糖和体质量的检测采用电子天平和血糖检测仪分别对小鼠体质量与血糖进行检测,每次测量血糖之前都将小鼠禁食不禁水过夜处理,次日用罗氏血糖采集针扎出小鼠尾巴的血滴或者用剪尾法采集小鼠血滴。每周至少检测1次血糖水平。
1.3.4 生存率检测及小鼠形体观察从治疗当天开始,每日观察小鼠的外形和生存情况等,记录每次死亡的小鼠,于第4周实验结束时对各组小鼠进行拍照记录。
1.3.5 胰岛素检测(1)胰岛素含量检测:使用眼球摘除术收集小鼠血样,4 ℃ 3 000 r·min-1离心20 min,仔细收集上清,4 ℃临时保存,-20 ℃短期保存,-80 ℃长期保存,按照说明书进行胰岛素ELISA检测。(2)胰岛素免疫组化检测:将小鼠引颈法处死后,用解剖剪小心取出胰腺、肌肉等组织器官,用4%多聚甲醛固定液处理后脱水、包埋再切片,切片放入染色缸染色,并且进行抗体孵育,再使用显色试剂盒处理,洗涤后用苏木精轻度复染,再封片。最后将制好的样品在室温下保存,并且用BA400Digital显微摄像系统进行结果观察和图片采集。
1.3.6 苏木精-伊红(HE)染色病理检测将小鼠引颈法处死后,用解剖剪小心取出心脏、肝脏、脾脏、肾脏、胰腺及肌肉等所需的组织器官,并将其用预冷后的1×磷酸缓冲液(PBS)洗涤后放入15 mL离心管中,再注入4%多聚甲醛固定液,4 ℃备用。脱水、包埋后切片,将切片放入染色缸进行苏木精染色,充分洗涤后再用伊红染液染色,再充分洗涤并且使用中性树胶封片。最后将制好的样品在室温下保存,并且用BA400Digital显微摄像系统观察结果和采集图片。
1.4 统计学分析
使用GraphPad Prism 5.0对数据进行统计学分析,采用Two-Way ANOVA或t检验进行分析,以P<0.05表示数据差异具有统计学意义。
2 结果
2.1 含胰岛素类似物基因的载体(pcDNA-INS)构建及结果分析
1.5%琼脂糖凝胶电泳将构建好的pcDNA-INS质粒进行酶切鉴定,其片段大小为250~500 bp,且完整的pcDNA-INS质粒、pcDNA3.1(+)质粒以及酶切后的pcDNA-INS载体大小和相对位置较为准确(图1:A)。质粒测序结果显示其基因序列正确,可以用于后续实验操作(图1:B)。
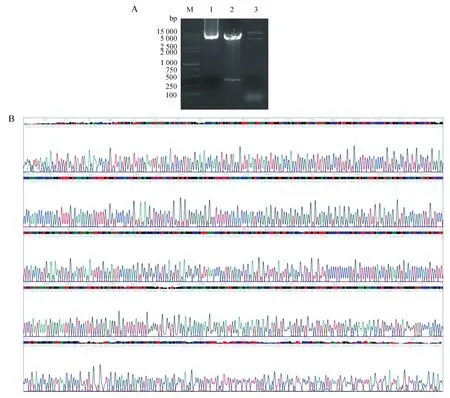
图1 质粒鉴定及胰岛素类似物基因测序Fig.1 Plasmids identification and gene sequence of insulin analogueA.质粒鉴定的电泳结果:M.Marker,1.构建完成的pcDNA-INS质粒载体(未酶切),2.pcDNA-INS质粒载体双酶切鉴定,3.pcDNA3.1(+)空载体;B.pcDNA-INS质粒载体上胰岛素类似物基因的测序结果A.plasmid identification:M.Marker,1.complete pcDNA-INS plasmid,2.pcDNA-INS plasmid identified by double enzyme digestion,3.pcDNA3.1(+)plasmid;B.gene sequence of insulin analogue on pcDNA-INS plasmid vector
2.2 糖尿病小鼠模型的建立
糖尿病小鼠血糖水平为(24.3±5.74)mmol·L-1,而正常小鼠血糖水平为(4.8±1.01)mmol·L-1,2组间的差异具有统计学意义(t=14.266,P<0.05)。此外,糖尿病小鼠的体质量显著降低,为(18.67±4.22)g,而正常小鼠的体质量为(22.42±3.06)g,2组间的差异具有统计学意义(t=3.445,P<0.05)。胰腺组织HE染色结果显示,糖尿病小鼠的胰岛细胞遭到了严重损害,模型构建结果可靠(图2)。
2.3 各组小鼠的血糖水平变化
在治疗后第3天开始检测每组小鼠的血糖水平,结果显示,NC组小鼠保持正常的血糖水平(约5 mmol·L-1);L/E-pcDNA3.1(+)组小鼠的血糖水平较高,与NC组之间的差异有统计学意义(P<0.05);pcDNA-INS组小鼠的血糖水平波动较大,与NC组之间的差异有统计学意义(P<0.05);L/E-pcDNA-INS组的小鼠血糖水平明显下降,且在第1周后与NC组接近,与其他2组的差异均有统计学意义(P<0.05)(图3)。
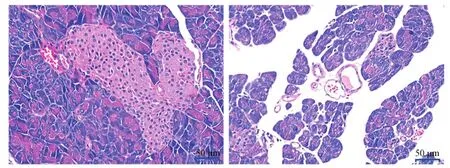
图2 正常小鼠(左)与链脲佐菌素诱导小鼠(右)的胰腺苏木精-伊红染色结果Fig.2 Hematoxylin-eosin staining pancrea results of normal (left)and streptozotocin-induced mice (right)
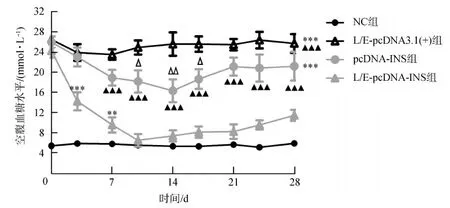
图3 各组小鼠治疗后的血糖变化Fig.3 Blood glucose trends of mice in different groups after treatments与NC组相比,** P<0.01,*** P<0.001;与L/E-pcDNA-INS组相比,▲▲▲ P<0.001;与L/E-pcDNA3.1(+)组相比,△ P<0.05,△△ P<0.01;下同Compared with normal control group,** P<0.01,*** P<0.001;compared with L/E-pcDNA-INS group,▲▲▲ P<0.001;compared withL/E-pcDNA3.1(+)group,△ P<0.05,△△ P<0.01,△△△ P<0.001;the same below
2.4 各组小鼠的血清胰岛素含量变化
实验开始前,3组糖尿病小鼠血清胰岛素水平间的差异无统计学意义(P>0.05),但是显著低于NC组(P<0.05)。在治疗后第2周,pcDNA-INS组的胰岛素水平明显升高,并且显著高于L/E-pcDNA3.1(+)组(P<0.05),与NC组和L/E-pcDNA-INS组之间的差异有统计学意义(P<0.05),而 L/E-pcDNA-INS组与NC组间的差异无统计学意义(P>0.05)。在治疗后第4周,L/E-pcDNA-INS组的胰岛素水平虽然降低了一些,但与NC组间的差异无统计学意义(P>0.05),且与pcDNA-INS组、L/E-pcDNA3.1(+)组间的差异均有统计学意义(P<0.05)。pcDNA-INS组在治疗4周后显著低于 NC组和L/E-pcDNA-INS组,差异均有统计学意义(P<0.05)(图4)。

图4 各组小鼠治疗后的血清胰岛素变化Fig.4 Serum insulin contents of mice in different groups after treatments
2.5 糖尿病小鼠生存率情况及免疫组化结果
治疗4周内,NC组和L/E-pcDNA-INS组(12/12)的生存率均为100%,L/E-pcDNA3.1(+)组、pcDNA-INS组的生存率分别为50%(6/12)、67%(8/12),2组间的差异无统计学意义(P>0.05)。其中,L/E-pcDNA3.1(+)组与NC组或L/E-pcDNA-INS组间的差异均有统计学意义(P<0.05)(图5:A)。在第4周时,取4组小鼠的胰腺和肌肉组织进行免疫组化检测,发现糖尿病小鼠胰腺均处于受损状态,且胰腺胰岛素含量显著少于正常小鼠(图5:B),而L/E-pcDNA-INS组小鼠骨骼肌胰岛素含量明显高于其他3组(图5:C)。

图5 各组小鼠治疗后的生存情况(A)及胰腺(B)和肌肉(C)的免疫组化结果Fig.5 Survival condition (A)and immunohistochemical results of pancreas (B)and muscle (C)A:与L/E-pcDNA3.1(+)组相比,☆ NC组,P<0.05,★ L/E-pcDNA-INS组,P<0.05;B,C:1~4.NC组,L/E-pcDNA3.1(+)组,pcDNA-INS组,L/E-pcDNA-INS组;下同A:compared with L/E-pcDNA3.1(+)group,☆ NC group,P<0.05,★ L/E-pcDNA-INS group,P<0.05;B,C:1-4.NC group,L/E-pcDNA3.1(+)group,pcDNA-INS group,L/E-pcDNA-INS group;the same below
2.6 各组小鼠的形体变化及病理检查结果
治疗4周后,L/E-pcDNA-INS组毛色虽有一定暗淡、粗糙现象出现,但脱毛现象较轻,且其整体形态与正常小鼠较为接近(图6:A1)。L/E-pcDNA3.1(+)组和pcDNA-INS组则有明显的脱毛现象,且毛色更加粗糙,整体形态更小,肌肉有不同程度的萎缩,且皮肤血管较为明显(图6:A2~A4)。此外,HE染色结果显示,L/E-pcDNA3.1(+)组和pcDNA-INS组小鼠各部位有不同程度的病变,如脾脏组织出现中心淋巴细胞减少且细胞变性坏死现象,肺组织有肺炎及肺泡萎陷现象、肌肉组织发生变性坏死等,而L/E-pcDNA-INS组的组织病变情况明显较轻,其组织炎症较少,且肌肉组织没有明显坏死,更接近NC组的情况(图6:B)。

图6 各组小鼠治疗后的形体特征(A)及HE染色结果(B)Fig.6 Appearances (A)and HE staining results (B)of mice after treatment
3 讨论
随着社会、经济的发展和进步,人们的生活方式和饮食习惯发生了较大变化,导致全球糖尿病患者逐渐增加,预计到2030年,全球糖尿病人数约达到5.22亿(Navarro-Gonzalez &Mara-Fernandez,2008;Whitingetal.,2011)。1型糖尿病患者需要每日注射胰岛素维持体内血糖的正常水平,这给患者带来许多痛苦和风险。基因治疗能为1型糖尿病患者带来长期治疗效果的福音。目前裸质粒治疗虽然安全性较高,但是其体内传递效率较低,因此需要将含有胰岛素基因的外源质粒有效导入糖尿病生物体内,才能产生良好的治疗效果。骨骼肌是重要的糖代谢组织之一,对维持体内血糖平衡起着重要作用,且在全身的分布范围较广,比肝脏、胰腺、肾脏等有着更强的操作性和更高的容错率。因此,骨骼肌是人们理想中外源胰岛素基因传递的靶场所之一。在自然条件下,胰岛素基因转录翻译出的C肽对胰岛素的折叠和构象起着至关重要的作用,但其结构冗长且刚性较大,影响胰岛素活性的发挥(Abaietal.,1999;Huaetal.,2008)。因此,胰岛素原需要在胰岛β细胞中经过特定的酶切掉C肽后形成成熟胰岛素,进而发挥生理作用。这意味着当外源胰岛素基因试图在非β细胞(如肝脏和肌肉组织)中进行表达时,很难得到高活性的成熟胰岛素(Fukazawaetal.,2006;Hanetal.,2011)。为了解决这一难题,可以使用柔性肽linker(GGGGS)3(Kuferetal.,1997)取代C肽,实现胰岛素A、B链的连接及不需要酶切掉连接区域的双重目标。
从20世纪开始,人们将电脉冲法应用到与细胞膜通透性改变的相关实验中,并且取得了一定成效(Coster,1965)。在电脉冲领域的研究中,高、低2种电压联用的方法效果较佳。在这种方法中,短时高压脉冲会促进细胞膜通透性的提升,而相对作用时间较长的低电压则会使DNA发生电泳现象从而加快入胞速度(Bureauetal.,2000),但高压电脉冲可能会对组织造成不可修复的损伤和功能缺陷,而降低电压则会降低基因传递效率(Hartikkaetal.,2001)。因此,人们在不断探索合适的替代方案来改变细胞膜的通透性,并且抵消高电压的作用和伤害,普朗尼克非离子型电中性的生物材料,是一类由两端聚氧乙烯(PEO)组成的亲水链和中间聚氧丙烯(PPO)组成的亲油链共同组成的两亲性三嵌段共聚物(Kabanovetal.,2002)。在普朗尼克浓度超过临界胶束浓度时,其PPO部分可以与亲油性材料或药物结合形成内核部分,而外部的PEO亲水链部分则可以形成外壳。这时,普朗尼克的结构能够起到保护内部材料或药物以及提高整体溶解度的作用(Batrakova &Kabanov,2008)。因此,普朗尼克是一种生物安全性较高、生物相容性较好的生物材料,常用作药物传递载体、药物乳化剂、缓释材料等(Alakhovetal.,2001)。
本实验室的前期研究工作已经构建了一套以L64-电脉冲体系介导的骨骼肌基因传递系统。Liu等(2014)在其研究工作中指出L64的加入可以使电脉冲作用下的裸质粒传递效率得到显著提升。He等(2019)将L64-电脉冲体系分别与聚乙烯亚胺(PEI)、表没食子儿茶素没食子酸酯(EGCG)等生物材料联用,使得裸质粒体内基因传递的效率得到进一步提升。Chen等(2015)以细胞系为模型研究了不同浓度L64及L64加入的先后顺序对基因传递效率的影响机制,并且发现L64主要是具有与细胞膜相似的结构从而扰动细胞膜,提高细胞膜的通透性,促进外源基因的入胞。本实验室由L64独特结构对生物膜的影响联想到了从仿生学角度构建新型三嵌段分子——类磷脂双分子层结构和反磷脂双分子层结构,并且研究了2种共聚物的结构和功能特点,以及其对骨骼肌细胞基因传递效率的影响和机制(Puetal.,2014)。在外源质粒注射小鼠肌肉组织后,Pluronic L64-电脉冲系统能有效提高外源胰岛素基因的有效表达。因此,在成功建立了1型糖尿病小鼠模型后,使用Pluronic L64-电脉冲体系和pcDNA-INS进行联合治疗,糖尿病小鼠血糖得到了有效控制并且其他相关病症和指标得到了最大的缓解。此外,免疫组化结果显示,治疗4周后,3组糖尿病小鼠的胰腺组织依然受损严重,且胰岛素表达量较少,而L/E-pcDNA-INS组的肌肉组织含量相对较高,这说明L/E-pcDNA-INS组病症的缓解并不是由于其被破坏β细胞的重生引起,而确实为外源基因治疗效果。HE染色结果表明,长期高血糖对机体的伤害很严重,经过治疗后的小鼠相对症状较轻,尤其以L/E-pcDNA-INS治疗方案为代表,在极大程度上缓解了1型糖尿病小鼠的病症,并且与正常小鼠相比,Pluronic L64-电脉冲体系和pcDNA-INS联合治疗对小鼠的机体没有明显毒副作用,是一种较为安全、可靠的、具有潜力的治疗方法。
综上所述,本研究基于实验室前期工作提供了一套安全、高效的以裸质粒和Pluronic L64-电脉冲体系为基础的1型糖尿病骨骼肌基因治疗系统,为实现胰岛素的长期、有效分泌提供了一定实验依据。
——一道江苏高考题的奥秘解读和拓展

