黑花生与红花生果实各部分硒含量的研究
徐 聪,杨 柱
(陕西省安康市农业科学研究所,陕西 安康 725021)
硒是一种多功能的生命元素,是人体必需的微量元素[1],但是又不能自制,且无机硒不仅不易吸收,还易对人体造成毒害。因此通过植物将无机硒转化成有机硒进入食物链,是人类和动物摄入硒的重要来源,所以研究植物对硒的生物富集特点具有重要意义。
花生是我国主要的油料作物,营养价值比粮食高,含有大量蛋白质和脂肪,有“长生果”之称。花生果实各部分都是宝,果仁可食用,包衣和果壳均有药理作用[2]。为此,我们选择了花生为研究对象,采用微波消解-氢化物-原子荧光光谱法对样品进行测定,得出硒在不同品种的花生果实各部分的含量,为进一步的研究提供参考。
1 材料与方法
1.1 仪器与试剂
全能型微波化学工作平台:TOPEX+(上海屹尧仪器科技发展有限公司),智能控温电加热器:G-400(上海屹尧仪器科技发展有限公司);原子荧光光度计:AFS-8220(北京吉天仪器公司),硒编码特种空心阴极灯。硒标准溶液[GBW(E)080215]:100 μg·mL-1(国家标准物质中心);硝酸:优级纯(成都科龙化工试剂厂);盐酸:优级纯(洛阳昊华化学试剂有限公司);30% 双氧水:分析纯(天津市科密欧化学试剂有限公司);实验用水为优普纯水机制备的超纯水;器皿使用前用10% HNO3浸泡24 h,超纯水冲洗备用。
1.2 样品来源
黑花生和红花生均为陕西安康市农业科学研究所3号试验田所产。
1.3 实验方法
1.3.1 样品前处理 样品首先用清水冲洗去除泥沙,依次用纯水洗涤3次,超纯水冲洗2次,沥干;再将样品放置恒温干燥箱100℃烘至恒重,烘好后,取出放在干燥器中自然冷却;最后将样品分离为壳、花生仁、包衣三部分,分别研磨成粉末保存在干燥器中备用。
1.3.2 样品制备 称取0.2 ~0.5 g(精确到0.001 g)样品放入消解罐中,然后加入5 mL浓硝酸摇匀,放入G-400加热器中120 ℃预消解30 min后,取出冷却至室温加入1 mL 30%双氧水混匀,盖好密封盖放入微波化学工作平台中。根据样品选择合适的反应条件进行微波消解。降温至60 ℃取出消解罐转移到G-400加热器中120 ℃进行赶酸,约剩1 mL液体时取出冷却至室温,然后加入5 mL 6 moL·L-1的盐酸溶液,混匀后再放入G-400加热器中120 ℃进行还原反应,待黄烟散完出现白烟取出冷却至室温。用超纯水冲洗罐壁将内容物无损失的转入10 mL容量瓶中,定容、混匀待测。以同样步骤制备试剂空白[3]。
1.3.3 标准溶液的配制 分别准确吸取1 000 μg·L-1硒标准使用液0.2、0.4、0.6、0.8、1.0、2.0、3.0 mL置于100 mL的容量瓶中,用10% 盐酸溶液定容,配制成浓度为2.0、4.0、6.0、8.0、10.0、20.0、30.0 μg·L-1的梯度标液,绘制标准系列,见表1。

表1 标准系列测定
1.3.4 仪器工作条件 主要有:
(1)微波化学工作平台设置。选择梯度升温法消解法。室温升到100 ℃保温3 min,再升到130 ℃保温3 min,再升到160 ℃保温3 min,最后升到200 ℃保温25 min。
(2)原子荧光光度计工作条件设置。负高压270 V;总电流80 mA;辅阴极电流40 mA;载气流量300 mL·min-1,屏蔽气流量800 mL·min-1;原子化器高度8 mm;测定方式:校准曲线;读数方式:Peak Area;测量方式:Std. Curve; 读数时间10 s,延迟时间1 s,重复次数2次;进样方式为手动进样[4~5]。
1.3.5 标准曲线的绘制 按1.3.4(2)中设定的仪器工作条件,将原子荧光分光光度计调到最佳状态,用2%硼氢化钾-0.5%氢氧化钾溶液(现配现用)作为还原剂,首先连续对10%的盐酸载液测定获得稳定的标准空白值,再测定梯度标液自动扣除标准空白值以获得相应的荧光强度。系统自动绘制标准曲线(见图1),并算出回归方程式和相关系数。线性回归方程为y=93.018x+10.635,相关系数R2=1。
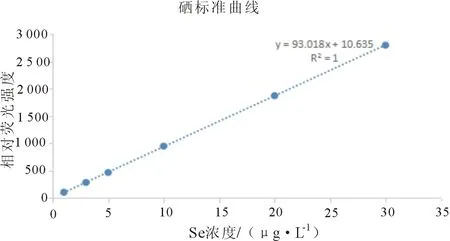
图1 硒的标准曲线
1.3.6 测定方法 按照仪器操作条件2%硼氢化钾-0.5%氢氧化钾溶液(现配现用)作为还原剂,10%盐酸做为载液,将样品溶液导入原子荧光光度计,测其荧光强度,由上面的线性回归方程及样品配制倍数计算出样品中硒的含量。
2 结果讨论
2.1 重复性实验
为了验证本实验方法的可靠性,用黑花生果仁和黑花生壳按1.3.2方法处理,按1.3.6方法重复测定5次,计算RSD值,结果见表2。
2.2 精密性实验
为了验证测量方法的可靠性,分别对黑花生果仁和黑花生壳测量了5次,计算RSD值,结果见表3。
2.3 回收率实验
分别对样品中微量元素Se进行加标回收,称取样品后加入硒标准溶液,按1.3.2方法处理,按1.3.6方法测定,测得加标回收率,结果见表4。

表2 重复性实验结果

表3 精密性实验

表4 加标回收结果
2.4 花生果实各部分硒含量测定
结果见表5。

表5 红花生、黑花生果实各部分硒含量
3 结论
3.1 实验方法的讨论
采用微波消解-氢化物发生-原子荧光光谱法的方法测定花生各部分中微量元素硒的含量,重复性实验结果RSD值在6%以内,仪器精密性测试RSD值在2%以内,回收率为97%~108%。此方法具有操作简单易行、干扰少、灵敏度高、回收率好的特点。应该注意的是硒的熔点只有217 ℃,沸点为685 ℃,因此在实验过程中要严格控制温度,避免实验过程中造成硒的损失,导致实验结果偏低,赶酸温度和还原温度控制到120 ℃为宜。
3.2 实验结果的讨论
(1)从结果可以看出,不管是红花生还是黑花生,各部分的总硒含量顺序一致,都是果仁>壳>包衣。
(2)相对于红花生,黑花生的硒含量更高。黑花生的壳含量大概是红花生壳的1.3倍,黑花生的果仁含量大概是红花生果仁的1.5倍,黑花生的包衣含量大概是红花生包衣的1.8倍。由于在同一块试验田里生长,生长大环境相同,所以从结果可以看出黑花生的聚硒能力更好。

