姜黄素联合美沙拉嗪治疗轻中度溃疡性结肠炎的临床观察*
朱立伟, 朱达坚
广东医科大学顺德妇女儿童医院(广东佛山 528300)
溃疡性结肠炎(ulcerative colitis,UC)是一种慢性疾病,其特征在于结肠和直肠黏膜的弥漫性炎症。由于近年来发病率的增加和预后不良,UC的治疗已成为临床的挑战。UC的发病机制是多因素共同参与的,如基因易感性、黏膜屏障破坏、免疫机制失衡和肠道菌群比例失调等。UC病变起始部位为直肠,由近端以连续的方式延伸至部分或整个结肠,主要侵犯的是肠壁浅层结构黏膜层及黏膜下层。UC最突出的表现是血性腹泻,其他症状有腹痛、消瘦、直肠紧迫感、里急后重等。还可伴有关节病变、眼部病变、皮肤病变和肝胆病变等肠外表现以及消化道出血、缺铁性贫血、周围性神经病等全身症状。尽管UC通常不会对生命构成直接威胁,但它常常导致焦虑和生活质量下降,从而导致不可预测和危险的并发症。
1 资料与方法
1.1 一般资料 随机纳入佛山市顺德妇女儿童医院自2018年1月起至2019年1月诊断为轻度至中度UC的门诊及住院患者。本研究纳入对象的诊断标准是基于2012年发布的关于UC诊断与治疗的共识意见[1]制定的。纳入标准:(1)18~65岁轻、中度的活动期UC患者,男女不限;(2)通过放射学、内镜检查以及组织学标准诊断为UC的患者,且从肛缘起病变范围超过25 cm;(3)Mayo评分在3~10分,并稳定4周以上;(4)曾使用皮质类固醇(>20 mg/d,泼尼松龙)或替代药物的患者需达到缓解,并已成功停止类固醇治疗;(5)血红蛋白>9 g/dL;(6)患者知情同意,志愿参加本次临床试验,并通过医院伦理委员会审核。排除标准:(1)不符合纳入标准者;(2)患有基础病如肾或肝脏疾病、慢性胰腺炎、糖尿病或胆结石;(3)严重的心血管疾病;(4)感染、败血症或肺炎的患者;(5)孕妇或哺乳期妇女;(6)既往有酒精及药物滥用史的患者;(7)实验室异常指示贫血(血红蛋白<9 g/dL),白细胞减少,血小板减少症或凝血异常;(8)敏感体质或对本次研究所使用药物过敏的患者;(9)接受免疫调节剂、生物制剂、抗生素、益生菌以及其他可能对试验影响的药物治疗的患者。
1.2 方法
1.2.1 分组方法 根据SPSS软件生成的随机数事先进行分组。在研究开始前,按照门诊、住院患者的先后就诊顺序,受试者根据相应的随机数被随机分配到不同的治疗组。
1.2.2 治疗方案 对照组(单药美沙拉嗪方案):口服美沙拉嗪[美沙拉嗪肠溶片(惠迪),葵花药业集团佳木斯鹿灵制药有限公司,国药准字H19980148,规格:0.25 g/片]活动期:1 g/次,4次/d,维持治疗:0.5 g/次,3次/d。疗程为4周。观察组(姜黄素联合美沙拉嗪方案):在对照组用药基础上,加用姜黄素制剂[降脂通络软胶囊(旨可平),神威药业集团有限公司,国药准字Z20040032,每粒含姜黄素化合物50 mg],100 mg/次,3次/d。疗程为4周。观察组药物选择理由:(1)姜黄素治疗UC的临床研究表明[2],姜黄素对于UC是有效的;(2)本药品为国药准字,主要成分为姜黄素,在临床试验中未出现明显的毒副作用,说明降脂通络软胶囊用于临床研究是安全的[3-5]。
1.2.3 疗效评定和不良反应观察
1.2.3.1 疗效评定 依据《共识意见》中疗效评定标准[1]设定本研究疗效标准。UC的疾病活动度使用UCDAI标准进行评分。UCDAI评分由同一门诊医生或住院部医生针对4个参数(大便次数、直肠出血、内镜评分和医师针对其严重程度的评分)进行个体评分计算。其中直肠出血和大便频率评分通过询问患者过去7 d的症状来评估。(1)主要结局指标:有效定义为在4周结束时UCDAI相比基线评分降幅≥30%以及下降超过3分(含3分),而且便血部分评分≤1分或者便血评分降幅至少1分。显效定义为在4周结束进行评价时患者UCDAI评分及便血分项评分下降但未达到有效的诊断标准,即UCDAI相比基线评分降幅<30%或下降<3分,便血部分的分项评分>1分且评分未下降。无效则定义为在4周结束时评定为UCDAI评分及便血分项评分无降低甚至升高。临床应答率=有效率+显效率。(2)次要结局指标:获得内镜下疾病活动度改善的患者比例。内镜应答定义为在第4周的内镜亚组评分至少下降1分。黏膜愈合定义为在第4周的内镜亚组评分为0分或者1分。
1.2.3.2 实验室结果指标变化 白细胞计数(WBC)、血红蛋白(Hb)、血小板计数(PLT)、血沉(ESR)、血清白蛋白(ALB)。
1.2.3.3 安全性评估 详细的询问患者主观感受;并进行体格检查及实验室检查如生物化学和血常规、凝血功能、肾功能、肝功能分析;记录研究期间发生的任何不良事件,详细记录不良事件的表现、发生时间、频次、持续时间,并记录干预方案和两组用药期间的不良反应结局。
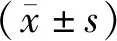
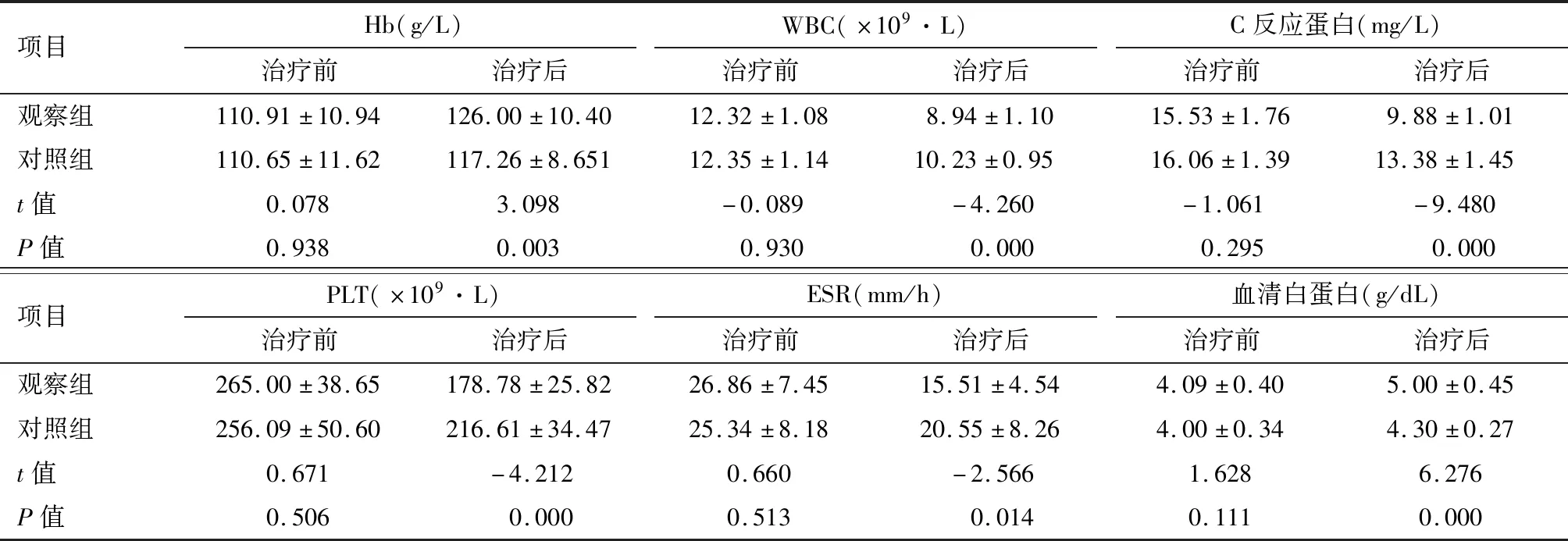
2 结果
2.1 两组治疗前基线数据的比较 对两组患者的一般情况[性别、年龄及体质指数(BMI)等]和入组时病情(病程长短、病情程度、内镜评分及病变范围等)以及实验室指标(炎症反应指标、安全性指标等)各方面进行基线分析对比,两组患者各方面差异无统计学意义(P>0.05),有可比性,见表1。


项目例数性别(例)男女年龄[(x±s)岁]身高(m)体重(kg)BMI(kg/m2)病程(d)观察组23121141.43±12.9781.69±0.0666.35±9.1023.13±2.1723.70±3.50对照组23101342.13±11.071.66±0.0665.04±6.0823.70±2.2224.26±3.33P值0.5550.3270.0810.5710.3810.578项目例数病情程度(例)病变范围(例)轻度中度左半结肠全结肠炎治疗前Mayo评分治疗前内镜亚组评分2分3分观察组2381510137.13±2.03185对照组2391413107.04±2.21167P值0.7600.3760.9110.502
2.2 临床疗效评定
2.2.1 两组Mayo积分差值 观察组与对照组两组Mayo积分治疗前后差值经正态检验提示不符合正态分布,采用秩和检验进行统计学分析,Z=-3.684,P<0.05,两组患者Mayo积分治疗前后差值差异无统计学意义,具有可比性。结合调整后的均数可知,与对照组相比观察组积分降低更明显,观察组优于对照组,治疗效果差异有统计学意义(P<0.05)。见表2。


组别 例数治疗前积分治疗后积分治疗前后差值Z值P值观察组237.13±2.034.17±2.422.96±1.02-3.6840.000对照组237.04±2.215.30±2.421.74±1.10
2.2.2 临床疗效 观察组和对照组的治疗有效率差异有统计学意义(F=12.667,P=0.002),见表3。

表3 两组用药后临床应答比较 例(%)

表4 两组用药后内镜应答比较 例(%)

表5 两组用药后粘膜愈合比较 例(%)
2.3 两组患者治疗前后实验室数据比较 治疗前两组患者血清Hb、WBC、PLT、C反应蛋白、ESR、血清白蛋白水平差异无统计学意义(P>0.05)。治疗后观察组Hb、白蛋白升高显著高于对照组,而WBC、PLT、ESR、C反应蛋白显著低于对照组,差异有统计学意义(P<0.05)。见表6。

项目Hb(g/L)WBC(×109·L)C反应蛋白(mg/L)治疗前治疗后治疗前治疗后治疗前治疗后观察组110.91±10.94126.00±10.4012.32±1.088.94±1.1015.53±1.769.88±1.01对照组110.65±11.62117.26±8.65112.35±1.1410.23±0.9516.06±1.3913.38±1.45t值0.0783.098-0.089-4.260-1.061-9.480P值0.9380.0030.9300.0000.2950.000项目PLT(×109·L)ESR(mm/h)血清白蛋白(g/dL)治疗前治疗后治疗前治疗后治疗前治疗后观察组265.00±38.65178.78±25.8226.86±7.4515.51±4.544.09±0.405.00±0.45对照组256.09±50.60216.61±34.4725.34±8.1820.55±8.264.00±0.344.30±0.27t值0.671-4.2120.660-2.5661.6286.276P值0.5060.0000.5130.0140.1110.000
2.4 安全性评定 观察组与对照组患者均未出现肝肾功能、凝血功能受损,也并未出现过敏等症状。临床研究过程中仅出现轻微恶心、食欲减退、头痛头晕不适。观察组1 例患者出现恶心,1例患者食欲减退;对照组有1例头痛、头晕,2例患者食欲减退、1例患者恶心。上述患者及时给予相应简单处理后症状缓解,未干扰研究进行。两组不良反应比较差异无统计学意义(P>0.05)。见表7。
2.5 依从性评定 在为期4周的治疗过程中,观察组与对照组患者无患者退出研究。所有患者均按照预先规定的治疗方案进行治疗,两组患者也未出现漏服、擅自增减药物剂量的情况。
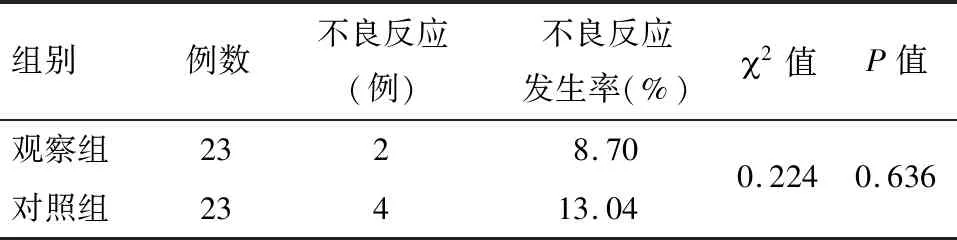
表7 两组不良反应比较
3 讨论
UC治疗的短期目标是诱导缓解,而长期目标是维持缓解并防止复发、疾病进展。为患者提供更好的生活质量,减少对糖皮质激素的长期依赖,并将出血、穿孔癌变的风险降至最低是每一个消化疾病医师奋斗的目标。对于专科医师而言,我们必须根据患者病情、病变特点个体化制定治疗方案,需向患者仔细分析各方法的优缺点,更需要结合患者的情况及其个人意愿,患者的经济情况也是我们需要考虑的方面,在与患者充分交流沟通后,最终制定治疗方案,此时患者有更好的依从性,往往能取得更好的疗效。UC的病程长,患者的生活质量不佳,有复发和癌变的风险。在传统药物治疗不能满足现代医学的要求时,我们可以选择中医药发挥其独特的特色及优势。
姜黄素的病理生理效应,已经在动物模型中进行了评估。研究表明[6],姜黄素能够通过抑制TLR-4受体和MyD88的途径对实验动物结肠炎产生抑制作用。Zhang等[7]发现姜黄素能够通过激活PPAR-γ途径抑制TNBS诱导的溃疡性结肠炎,从而提高患病大鼠的长期存活率,促进体重的恢复,降低结肠炎的宏观评分。姜黄素可抑制p38MAPK及其上下游信号通路的表达,减少肿瘤坏死因子-α等促炎细胞因子的释放,减少中性粒细胞浸润,从而减轻炎症损伤,在UC治疗中发挥作用[8]。姜黄素可抑制NF-κB的活化,阻断IKB蛋白的降解,抑制结肠黏膜中促炎细胞因子的转录,从而防止炎症级联反应和结肠黏膜损伤[9]。Sanchez-Munoz等[10]的研究表明,姜黄素通过降低各种免疫细胞分泌的白细胞介素的过度表达,引起炎症反应的减少,减轻大鼠结肠炎症。姜黄素可抑制肠组织TNF-α的表达水平,从而抑制肠上皮细胞的凋亡[11]。姜黄素可抑制TRPV1的磷酸化及随后的膜转位,有效减轻葡聚糖硫酸钠诱导的结肠炎大鼠的内脏痛觉过敏[12]。
通过46例患者的初步研究发现在4周治疗后,在Mayo评分下降、临床应答、黏膜愈合、实验室指标调节等各方面,美沙拉嗪联合口服姜黄素类制剂均优于单药美沙拉嗪。从安全性角度出发,应用姜黄素类制剂,患者不良反应并未增加,患者依从性好。说明在应用口服姜黄素制剂联合美沙拉嗪治疗轻、中度UC时,在产生更好的临床疗效时却不增加毒副作用的发生,该治疗方案是安全有效的。
综上所述,姜黄素作为一种食品衍生的药物,在人类保健和防治各种疾病方面发挥着重要作用。鉴于目前UC传统治疗药物的局限性,使用姜黄素类制剂可以作为补充药物有效地减轻UC患者的临床症状和促进患者的结肠黏膜愈合。相信在不久的将来,通过对姜黄素的研究,能为UC的治疗和缓解提供新的方向。

