猪早期胚胎发育中SOX2基因启动子活性分析
赵剑超,柴壮,郭诗萌,刘忠华
研究报告
猪早期胚胎发育中基因启动子活性分析
赵剑超,柴壮,郭诗萌,刘忠华
东北农业大学生命科学学院,哈尔滨 150030
转录因子SOX2 (sex determining region Y-box2)在早期胚胎发育第一次谱系分化以及内细胞团多能性维持等方面具有重要的作用。但是目前有关基因启动子的系统研究较少,尤其是在猪()中尚无相关报道。为系统分析猪基因启动子在早期胚胎中的活性,本研究通过优化显微注射体系中绿色荧光蛋白表达载体种类和注射时间,构建了适合猪基因启动子活性分析的参照体系和显微注射体系;对猪基因翻译起始位点上游5000 bp区域进行转录因子结合位点的预测,发现该区域存在4个转录因子结合位点簇;针对上述区域设计并构建相应的缺失型基因启动子报告载体,利用建立的显微注射体系将其导入胚胎,通过mCherry荧光强度以及qRT-PCR定量分析基因启动子中不同转录因子结合位点簇对启动子活性的影响。结果表明,与全长基因启动子相比,基因翻译起始位点上游2254~2442 bp区域缺失后,猪4-细胞和8-细胞胚胎中基因启动子活性下降至17.8%,该缺失区域中仅包含两个NF-AT(nuclear factor of activated T cells)转录因子结合位点。因此,本研究结果推测猪基因启动子中NF-AT转录因子结合位点是影响猪早期胚胎基因启动子活性的关键位点。本研究为揭示猪早期胚胎发育中基因表达调控机制提供了数据支持。
基因;启动子活性;猪
SOX2蛋白作为重要的转录因子,广泛表达于胚胎、原始生殖细胞、神经元等多种组织与细胞中。在胚胎发育过程中,基因的表达是大脑皮层形成和发育所必需的,同时也参与指导食道与前胃的形成[1]。此外,基因在多种癌细胞与肿瘤干细胞中广泛表达[2~4]。近年来,SOX2转录因子在早期胚胎发育和维持干细胞多能性方面的作用受到广泛关注[5~7]。
在哺乳动物早期胚胎发育中,第一次谱系分化发生在囊胚腔形成时期,胚胎由全能性的卵裂球分化形成多潜能性的滋养层细胞(trophectoderm, TE)和内细胞团细胞(inner cell mass, ICM)。然而,关于第一次谱系分化形成滋养层和内细胞团细胞的机制目前尚不清楚。SOX2蛋白作为核心多能性转录因子之一,在早期胚胎发育中第一次谱系分化以及内细胞团多能性维持等方面具有重要的作用[8,9]。2003年,Avilion等[10]证实小鼠()基因敲除的囊胚中仍存在ICM,但导致其丧失多能性,同时失去产生胚胎干细胞的能力。2014年,Wicklow等[11]发现小鼠中基因的表达不受CDX2蛋白调控,且基因在内细胞团中特异性表达并具有重要功能。在猪早期胚胎发育中,SOX2转录因子备受关注。2015年,Liu等[12]研究表明,虽然基因在猪内细胞团中特异性表达,但表达模式与小鼠不同:(1)在早期囊胚内细胞团前体细胞中即出现基因特异性表达,但此时基因尚未表达;(2)在囊胚期,滋养层细胞中基因表达沉默先于极化的发生,而小鼠中由于细胞的极化导致滋养层细胞中基因表达沉默。表达模式的差异暗示猪基因表达上游调控机制不同于小鼠。此外,在猪诱导性多能性干细胞(induced pluripotent stem cells, iPSC)的建系研究中,利用SOX2蛋白在内的经典4因子对体细胞重编程,虽然可以获得具有一定多能性的iPS细胞系[13~16],但猪iPSC同时具有内源基因不激活、外源基因不沉默以及不具嵌合能力等问题[17]。同时,参考小鼠和人胚胎干细胞系建系的经验,至今仍无法获得猪胚胎干细胞系[18,19]。上述研究表明,猪与小鼠、人等多能性调控网络存在差异,建立猪多能性相关调控网络机制具有重要的科学意义。
其次,用户端向传感器端发送验证传感器的身份的请求。用户端的计算公式为(9)—(10),其中R1是随机数是时间戳:
本研究通过检测基因启动子介导的报告基因表达水平评价其启动活性,预测了启动子区域转录因子结合位点,分析了各区域对基因启动子活性的影响,进而揭示猪早期胚胎发育中基因表达调控关键因子,为进一步研究猪早期胚胎第一次谱系分化以及多能性干细胞建立提供理论基础[20]。
1 材料与方法
1.1 质粒载体构建
本研究所用的质粒包括:pEGFP-C1 (Clontech,美国),pRL-TK (Promega E2241,美国),FUGW (Addgene 14883,美国)和pLV-mCherry (Addgene 36084,美国)。载体构建中片段克隆所用的DNA聚合酶为PrimeSTAR®Max DNA Polymerase (TaKaRa R045A,日本),反应体系为25 μL,反应条件中退火温度设定为58℃,时间15 s;DNA片段连接所用的试剂盒为NEBuilder®高保真 DNA 组装克隆试剂盒(NEB E2621S,美国),引物重复序列长度25 bp,20 μL反应体系中共加入0.2 pmol DNA片段总量,反应时间15 min。PCR和qRT-PCR所用全部引物信息见表1。
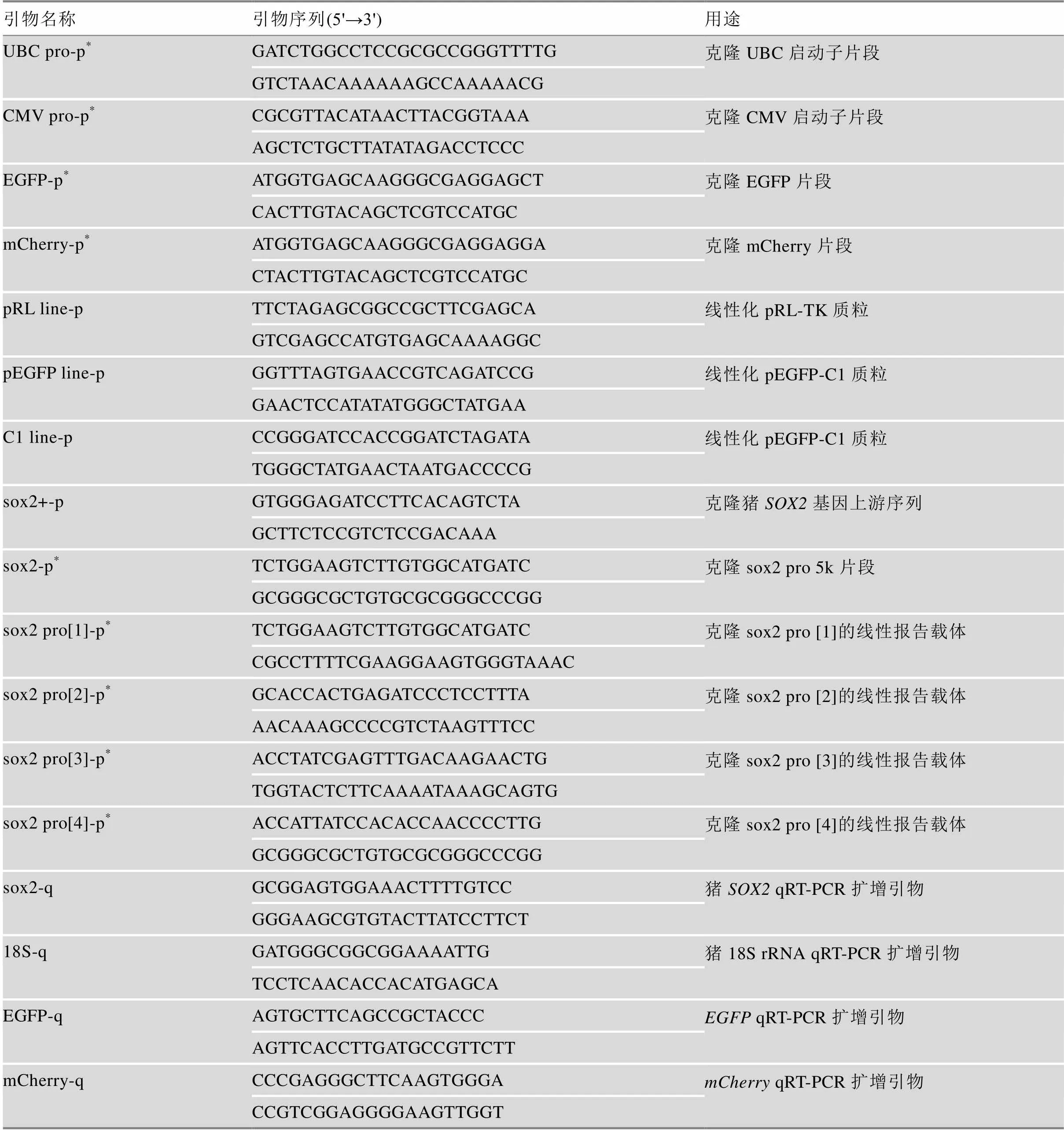
表1 引物信息
*引物序列中未标出用于无缝克隆的重复序列。
将质粒Sp0、Sp1、Sp2、Sp3、Sp4与内参质粒pEGFP-C1以4∶1的比例混合,终浓度为100 ng/μL。对猪胚胎进行注射并培养72 h,以检测mCherry以及EGFP蛋白的表达情况(图5 A)。结果显示,与Sp0注射组相比,Sp1注射组胚胎无法检测到mCherry蛋白信号;Sp3与Sp4注射组mCherry蛋白信号显著下降;而Sp2注射组胚胎mCherry蛋白水平与Sp0注射组无显著差异(图5 B)。进一步利用qRT-PCR对各组胚胎的基因相对表达量进行定量分析。结果显示,相对于Sp0注射组胚胎,各组胚胎基因相对表达量均有不同程度的下降,但与荧光检测结果不同的是,Sp3注射组胚胎基因的mRNA表达水平最低,仅为Sp0注射组的0.18(±0.0034) (图5 C)。据此推断,Sp3质粒中缺失的转录因子结合位点簇d3可能为基因启动子活性关键区域。根据转录因子结合位点预测结果,d3中仅包含两个NF-AT转录因子结合位点,推测NF-AT转录因子家族是调节猪早期胚胎中基因表达的关键转录因子。
显微操作系统为倒置显微镜(Nikon TS-100,日本)、显微注射系统(Nikon IM-9A,日本)及Femtojet Express定量注射系统(Eppendorf,德国)。取100 μL胚胎操作液(MAN)于平皿中央,并用石蜡油覆盖后放置于显微操作仪39℃恒温工作台上,向MAN液滴中加入卵母细胞准备注射。将5 μL质粒溶液通过微量上样枪头加至注射针内进行注射操作。注射系统相关参数为:注射压力(Pi)100 hPa、注射时间(Ti)0.5 s和补偿压力(Pc)40 hPa。显微镜下对猪卵母细胞进行胞质注射,注射量约为30 pL/枚。
(1)For high power semiconductor lasers,working current Iop is usually much larger than the threshold current Ith,so in formula(5)Ith has relatively small effect.
以Sp0质粒为模板,分别以sox2 pro[1]-p、sox2 pro[2]-p、sox2 pro[3]-p和sox2 pro[4]-p为引物进行克隆,将得到的克隆产物直接自连,分别获得质粒Sp1、Sp2、Sp3和Sp4,其特点为:分别缺失相应结合位点簇的基因启动子介导的mCherry表达载体。
以猪基因组为模板,利用引物sox2+-p进行克隆;再以克隆产物为模板,利用引物sox2-p克隆得到翻译起始位点上游5000 bp片段,即本研究中基因全长启动子,命名为sox2 pro 5k。以pLV-mCherry质粒为模板,利用引物mCherry-p克隆得到mCherry片段;以pEGFP-C1质粒为载体骨架,利用引物C1 line-p克隆得到线性化的载体骨架;将sox2 pro 5k片段、mCherry片段和线性化的载体骨架连接,获得质粒Sp0,其特点为:以pEGFP-C1质粒为基础骨架的5000 bp基因启动子介导的mCherry表达载体。
构建完成的质粒去内毒素提取后–20℃保存。
本工作提出的改进的模型预测直接转矩控制方法,通过优化矢量选择器得到需要进行价值函数优化控制的3个电压矢量,可有效降低模型预测直接转矩控制的优化计算量.对于控制延时对系统性能的影响,延时补偿控制能够显著减小由控制延时引起的电流纹波和转矩脉动.通过在MPDTC的价值函数中加入开关切换次数的约束,增大开关频率的权重因子可降低逆变器的开关频率,但同时会使得电流畸变率有所增加.仿真和实验结果表明,由全阶磁链观测器得到的磁链能够准确地跟踪其给定值,改进的MPDTC具有良好的动、静态性能,并且可以有效降低逆变器的开关频率.
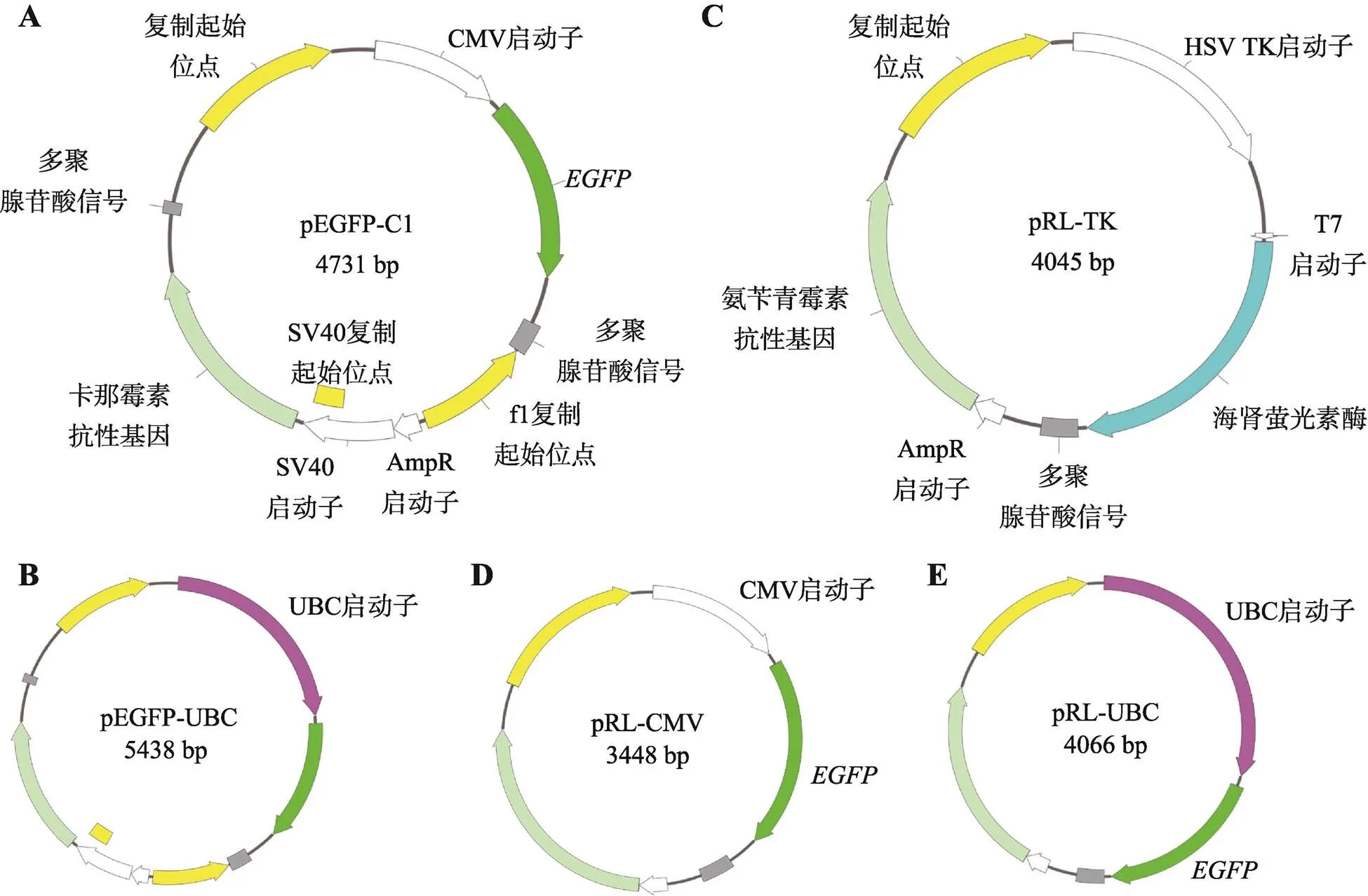
图1 报告质粒图谱
A, B:报告质粒pEGFP-C1和pEGFP-UBC构建图谱;C~E:pRL-TK质粒和pRL-CMV、pRL-UBC报告质粒构建图谱。
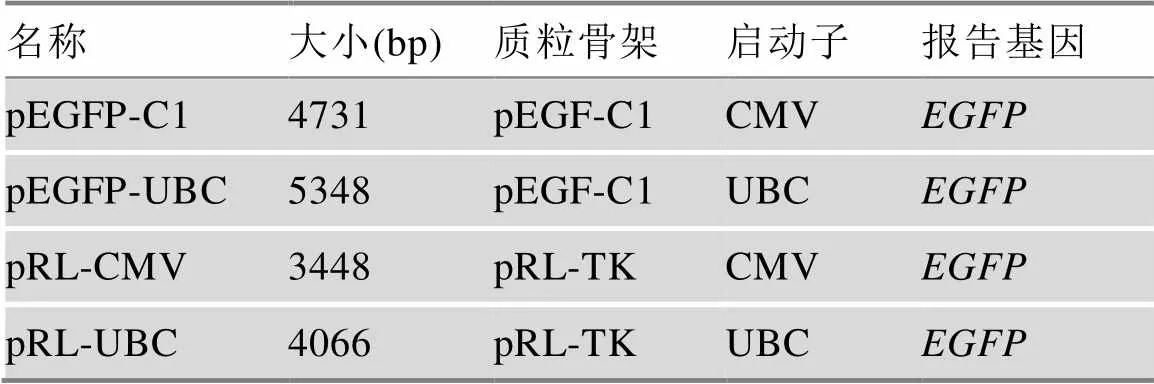
表2 报告质粒信息对比
1.2 胚胎培养与显微注射
2.1.1 报告载体的筛选
以pEGFP-C1质粒为模板,利用引物CMV pro-p和EGFP-p分别克隆得到CMV启动子片段和增强绿色荧光蛋白(enhanced green fluorescence protein, EGFP)片段;以pRL-TK质粒为基础载体,利用引物pRL line-p克隆得到线性化的pRL-TK质粒载体;将CMV启动子片段、EGFP片段和线性化的pRL-TK质粒载体连接,获得pRL-CMV质粒,将UBC启动子片段、EGFP片段和线性化的pRL-TK质粒载体连接,获得pRL-UBC质粒。其特点为:以pRL-TK质粒为基础骨架的CMV或UBC启动子介导的EGFP表达载体(图1,C~E;表2)。
1.3 启动子信息获取与预测
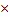
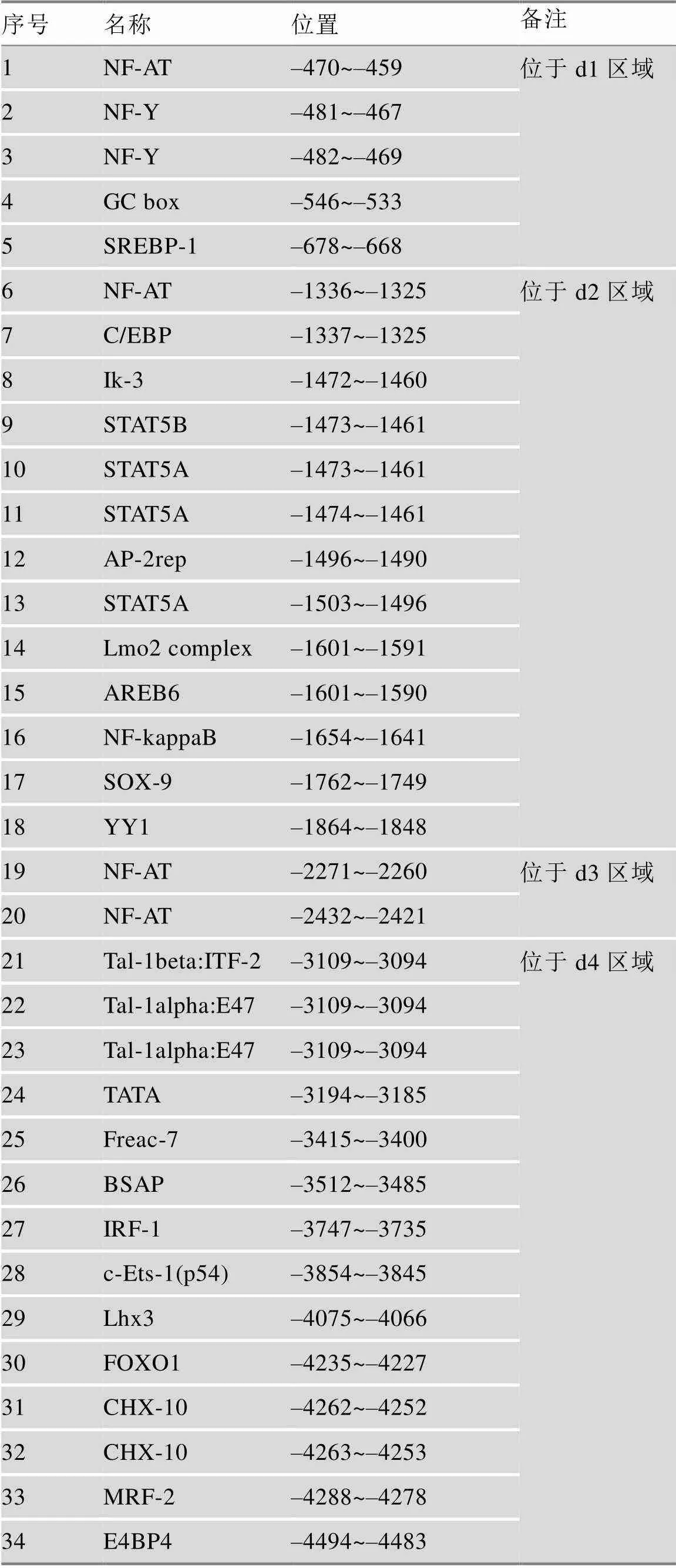
表3 sox2pro 5k片段中预测的转录因子结合位点
1.4 启动子活性分析
2.1.2 注射时间选择
2 结果与分析
2.1 猪胚胎显微注射体系的建立
从屠宰场收集猪卵巢,在37℃生理盐水中抽取直径2~8 mm卵泡。将获得的卵泡液静置,弃上清,并用HEPES缓冲液清洗稀释后,在39℃恒温工作台上借助显微镜挑出有3层以上卵丘细胞包裹的卵母细胞,50枚一组培养在500 μL预平衡的成熟培养液(MAT)中,条件为39℃、5%CO2的饱和湿度环境。避光静置培养42 h后,将卵母细胞置于0.5%透明质酸酶中震荡去除卵丘细胞,在39℃恒温工作台上借助显微镜挑出具有第一极体的MII期卵母细胞。将获得的MII期卵母细胞置于细胞融合液(FM)中排成一列,附加两次120 V/mm、30 μs的矩形脉冲以完成孤雌激活,之后50枚一组培养在500 μL预平衡的胚胎培养液(PZM-3),条件为39℃、5% CO2的饱和湿度环境中。
对猪胚胎显微注射体系中报告载体的类型进行筛选,以获得高效表达外源报告基因的载体。选择两种载体骨架以及两种广谱型启动子共计4种载体作为备选报告载体,分别是pEGFP-C1、pEGFP-UBC、pRL-CMV和pRL-UBC (图1)。孤雌激活后4 h用上述4种质粒对胚胎进行显微注射,注射质粒浓度为20 ng/μL。观察EGFP蛋白表达情况以及胚胎发育情况(图2,A和B)。结果表明,注射pEGFP-C1质粒的胚胎EGFP阳性率为39.33% (±1.76%),显著高于其他组(图2,C和D)。由于早期胚胎发育会受外源DNA浓度的影响,因此又分别选择20 ng/μL与100 ng/μL浓度的pEGFP-C1进行显微注射。经观察发现,当注射浓度提高至100 ng/μL时,注射胚胎发育情况与20 ng/μL浓度组无显著差异(图2B),但EGFP表达效果更好(图2,C和D)。因此,在后续研究中选择pEGFP-C1质粒为内参和基本载体骨架,质粒总浓度为100 ng/μL。
纸飞机飞得很远,再慢慢滑翔下去,安安静静地扎在街心花园的草丛里。阮小棉看着它,久久地久久地看,真想自己也和它一样,那么轻那么轻,可以滑翔,坠地的时候没有一点声响。
为了确定猪胚胎显微注射体系中最佳注射时间,分别针对孤雌前卵母细胞(–0 h)与孤雌激活0 h、2 h、4 h、6 h、8 h、10 h以及11 h后胚胎显微注射pEGFP-C1质粒,观察各组胚胎发育与EGFP蛋白表达情况(图3)。结果表明,不同注射时间对于胚胎发育与EGFP蛋白表达影响较大。其中–0 h组对胚胎发育影响最小,但EGFP蛋白表达水平最低;而2 h、4 h与6 h组对胚胎发育影响较小,同时EGFP蛋白高水平表达(图3,A和B)。综合胚胎发育情况及EGFP蛋白表达水平,选择孤雌后2~6 h作为最佳注射时间。此外,观察发现胚胎在4-细胞期开始表达EGFP蛋白,在8-细胞期EGFP蛋白表达阳性胚胎比例达到最高。因此,在后续基因启动子活性检测研究中选择孤雌后72 h收集4-细胞和8-细胞胚胎进行检测(图3 C)。
2.2 启动子结构预测分析与报告载体构建
本研究对猪基因翻译起始位点上游5000 bp序列进行转录因子结合位点预测分析。结果发现,该区域中转录因子结合位点成簇分布于4个区域,以与翻译起始位点的距离分别命名d1~d4(图4 A,表3)。针对4个结合位点簇分别设计并构建相应缺失的基因启动子报告载体,将构建的启动子片段分别命名为sox2 pro [1~4],构建的质粒分别命名为Sp1~4 (图4,B和C)。同时针对猪基因翻译起始位点上游5000 bp序列,与小鼠进行相似性比对分析,结果显示,序列相似点的排布近似斜率为1的直线,相似性为71% (图4 D)。因此,小鼠的相关研究结果在猪中具有一定参考价值。
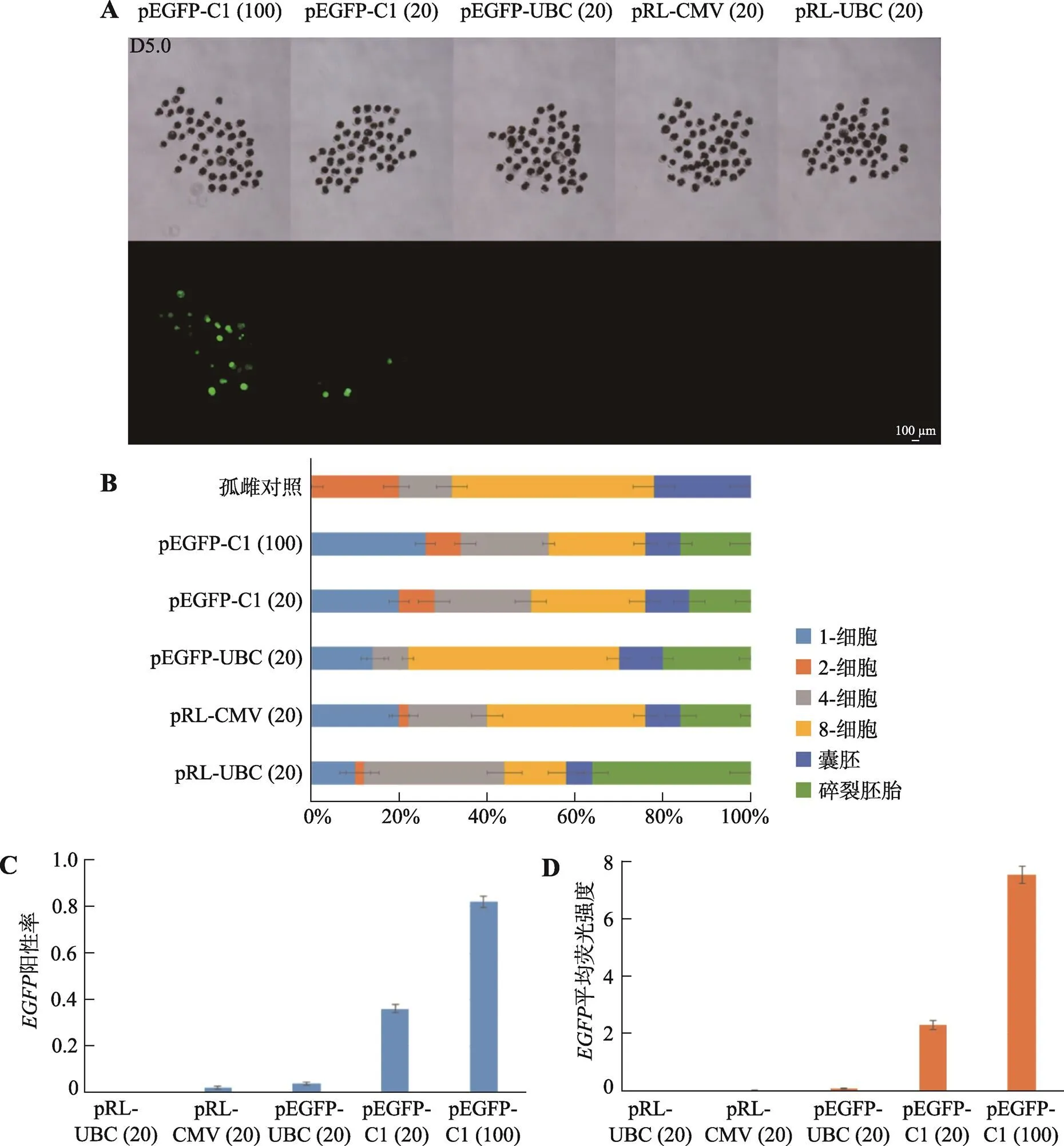
图2 4种质粒对胚胎荧光标记的效果
A:用4种质粒分别对孤雌激活4 h后的胚胎进行注射,培养5 d后荧光镜下观察基因表达情况;B:以孤雌胚胎为对照,各注射组培养5 d内胚胎各阶段发育情况统计;C:各注射组在培养5 d后胚胎基因表达阳性率;D:各注射组在培养5 d后胚胎EGFP平均荧光强度。括号中20和100分别代表质粒浓度为20 ng/μL和100 ng/μL。
2.3 启动子活性检测
以FUGW质粒为模板,利用引物UBC pro-p克隆得到泛素C (ubiquitin-C, UBC)启动子片段;以pEGFP-C1质粒为基础载体,利用引物pEGFP line-p克隆得到线性化的pEGFP-C1质粒载体;将UBC启动子片段和线性化的pEGFP-C1质粒载体连接,获得pEGFP-UBC质粒。pEGFP-C1和pEGFP-UBC质粒特点:以pEGFP-C1质粒为基础骨架的CMV (cytomegalovirus)或UBC启动子介导的EGFP表达载体(图1,A和B;表2)。
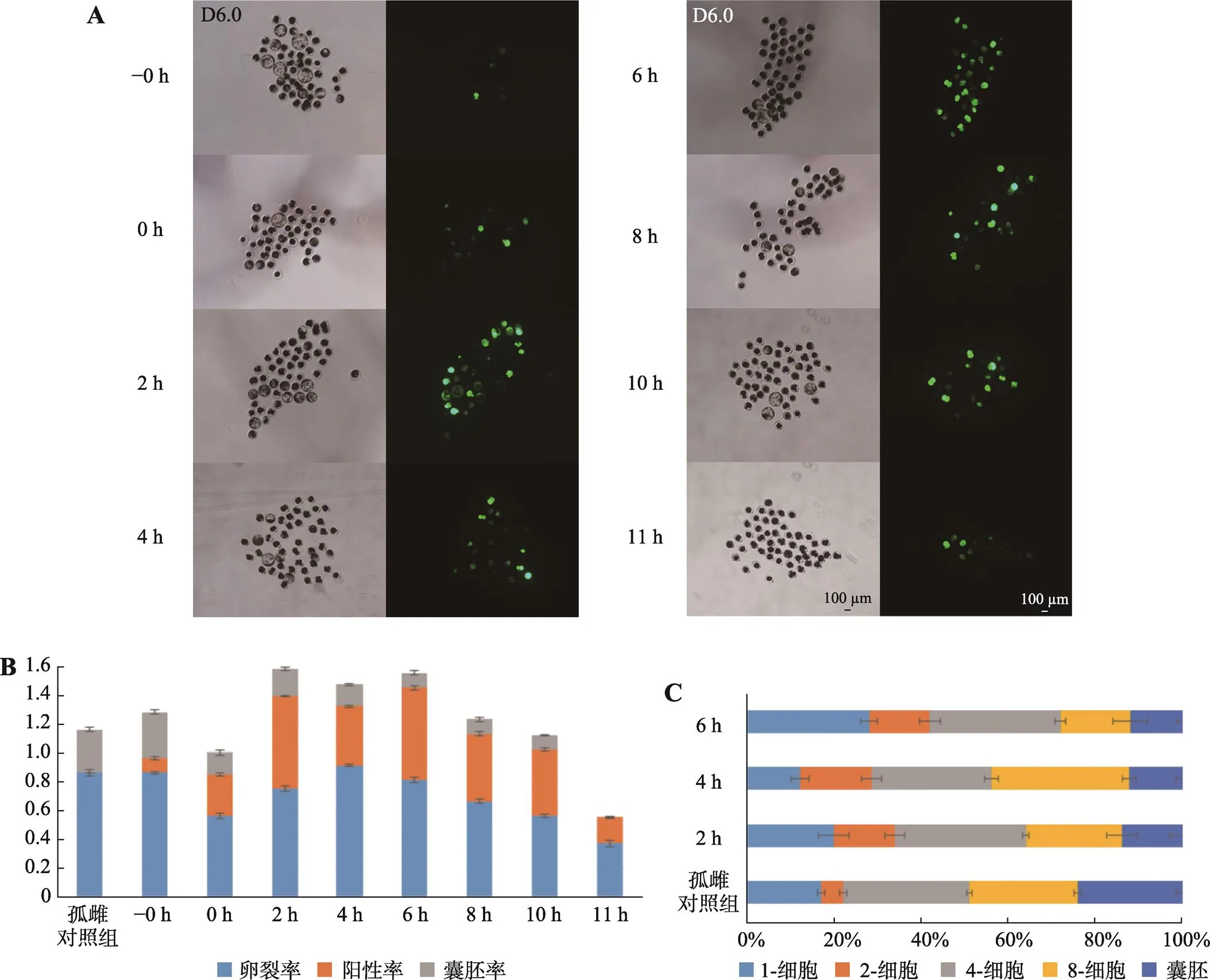
图3 孤雌激活前后不同注射时间的荧光标记效果
A:分别在孤雌前(–0 h)和孤雌后0 h、2 h、4 h、6 h、8 h、10 h、11 h注射pEGFP-C1质粒,培养6 d后观察基因表达情况;B:各注射组胚胎基因表达阳性率及发育率统计;C:2 h、4 h和6 h注射组在培养6 d时间内胚胎各阶段发育情况统计。
3 讨论
SOX2蛋白是哺乳动物早期胚胎发育中关键转录因子之一,对于基因上游调控网络的研究可以揭示早期胚胎发育中细胞命运决定、胚胎干细胞多能性维持等相关分子机制[21]。本研究通过对猪早期胚胎中基因启动子活性分析,发现NF-AT转录因子结合位点是4-细胞与8-细胞胚胎中调控基因表达的关键顺式调控元件。NF-AT是一个钙离子敏感的转录因子家族,在内皮细胞、骨骼肌细胞、平滑肌细胞和神经元等多种细胞中广泛表达[22]。但是NF-AT转录因子在早期胚胎发育中的作用功能尚不明确,同时NF-AT蛋白调控基因表达的相关研究尚未报道。因此,研究NF-AT转录因子对于猪早期胚胎发育的调控功能具有重要意义。
对Sp1注射组的报告基因检测时发现,其蛋白水平与mRNA水平并不一致。在小鼠中,基因启动子无“TATA box”核心启动元件,而上游约60 bp处存在倒转的“CCAAT box”元件[23,24],该元件作为基因启动子的核心启动元件,转录因子NF-Y (nuclear factor-Y)可识别、结合“CCAAT box”并募集RNA聚合酶复合体,启动基因的转 录[25~27]。而Sp1质粒中sox2 pro [1]启动子片段缺失区域d1上存在预测的NF-Y结合位点,且与翻译起始位点的距离同小鼠类似,因此推测d1中包含核心启动元件以及转录起始位点。然而本研究结果显示,Sp1注射组中可以检测到报告基因的mRNA表达。据此推断,在基因启动子的其他区域中存在第二转录起始位点,由于sox2 pro[1]中并未破坏第二转录起始位点,导致该组中检测到报告基因的mRNA表达,但由于移码突变产生的无义蛋白不具有荧光特性,因此无法检测到报告基因蛋白。预测分析结果显示d2区域包括C/EBP (CCAAT-enhancer-binding protein)结合位点,而C/EBP转录因子家族具有募集RNA聚合酶复合体、启动转录的能力[28~30],因此推测第二转录起始位点位于d2中。在后续研究中,本课题组将针对这两个潜在的转录起始位点进行分析,明确猪基因转录起始位点特性。
这几年,城市就像气球,不断膨胀。老城之外,又衍生出新城。车多了,人也多了,老城的路跟不上时代了,城市的机关单位就得挪出去,搬到城市的外围。路修得宽宽的,向北京的长安街看齐,生怕再过几年又落后了。嗅觉灵敏的开发商早瞅准时机,在新城的四周竖起一幢又一幢楼盘。
2007年,为提高服务业整体发展水平和国际竞争力,更好发挥标准化对服务业发展的促进作用,国家标准委积极探索服务业标准有效实施的途径,创新服务业标准化工作的机制和模式,与国家发展和改革委员会等六部委联合下发《关于推进服务标准化试点工作的意见》[1],在全国范围内,全面启动了服务标准化试点建设工作,涉及旅游、物流、金融、运输、社区、餐饮、商贸及家政等领域。
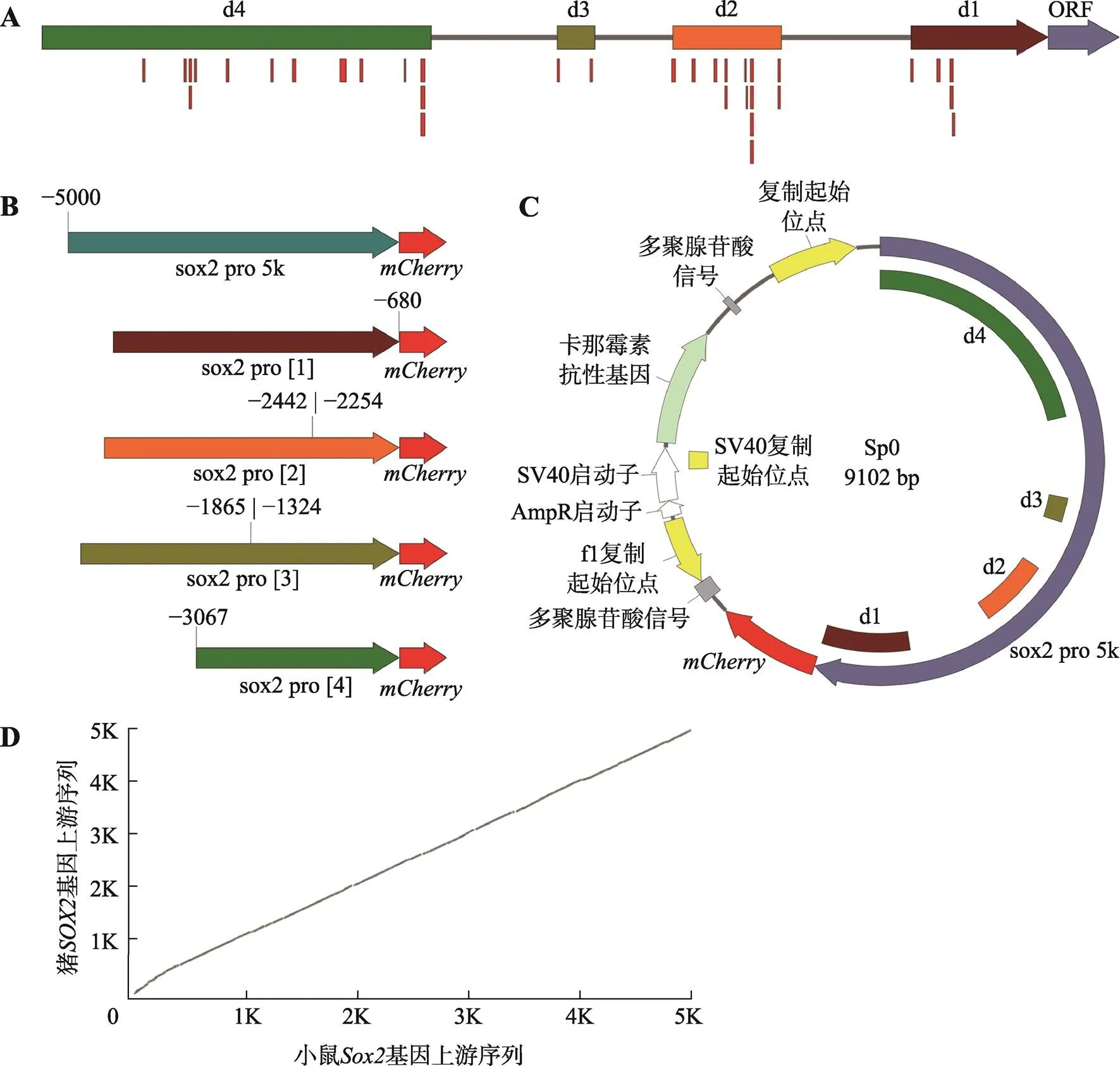
图4 猪SOX2翻译起始位点上游5000 bp序列结构分析
A:猪基因翻译起始位点上游5000 bp序列预测的转录因子结合位点(红色条)以及4个转录因子结合位点成簇分布的区域d1~d4;B:猪基因翻译起始位点上游5000 bp全长启动子、4个转录因子结合位点成簇分布的区域d1~d4和构建的各区域缺失型启动子sox2 pro [1~4];C:基因启动子报告载体图谱;D:猪翻译起始位点上游5000 bp序列与小鼠对应序列相似性比较。
根据上述结果以及相关分析,可以确定调控基因启动子的潜在关键因子包括NF-AT[31]、NF-Y[32]、C/EBP[33]和AP-2 rep (Krueppel-like factor 12) 4种转录因子[34]。Cao等[35]对猪早期胚胎发育表达模式进行分析,发现上述4种转录因子在早期胚胎发育中都有表达。其中,NF-Y和C/EBP转录因子可能与猪基因的转录起始相关;NF-AT转录因子可以增强基因启动子的启动活性;而AP-2 rep转录因子或对NF-AT转录因子的功能产生影响[36,37]。因此推断这4类转录因子是潜在调节基因表达的关键因子。
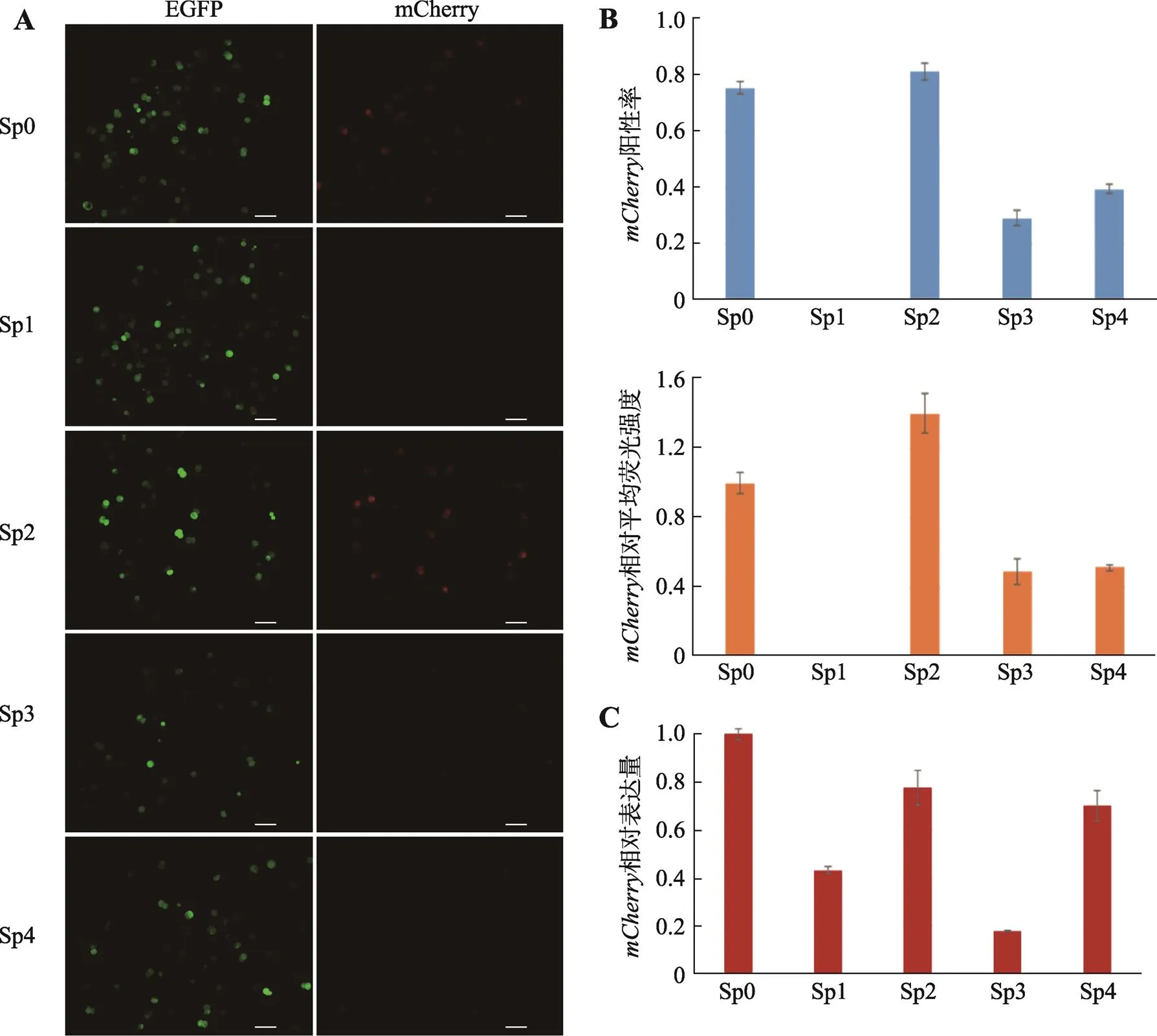
图5 各启动子片段的活性分析
A:孤雌胚胎分别注射Sp0~4各组质粒并培养72 h后在荧光镜下观察和基因表达情况(Bar=100 μm);B:孤雌胚胎注射并培养72 h后各注射组基因表达统计;C:孤雌胚胎注射并培养72 h后qRT-PCR检测相对表达量。
双萤光素酶检测系统[38]虽然是启动子活性检测的常规技术[39],然而受到早期胚胎样品收集困难以及细胞数低的制约,本研究无法采用双萤光素酶检测系统进行基因启动子活性评价。因此选择报告基因表达水平检测的方式评价启动子活性[40]。通过qRT-PCR检测报告基因mRNA的相对表达水平,避免蛋白降解周期对结果的干扰;利用内参质粒的表达水平检测,排除显微注射体系的系统误差;利用内源基因的表达水平检测,排除各组间因胚胎状态差异导致的误差,通过计算获得报告基因相对表达水平可以最高程度地体现相应启动子的转录活性。同时,本研究对胚胎显微注射条件进行探索,最终确定孤雌激活2~6 h进行显微注射可以在保证报告基因表达的前提下最小限度地影响胚胎发育。本研究技术体系可以更广泛地应用于猪早期胚胎中启动子活性的研究,筛选分析猪早期胚胎中相关基因调控元件,揭示猪早期胚胎发育特点。
从H在2017年工资与福利发放表中可以查出H 2017计提工资薪金2 026 830 003.08元,实际发放只有1 918 170 240.84元。两者之间差了108 659 762.2元。只能扣除在规定限额内的实际发放的工资和薪金,其余均不能扣除。所以,在最终环节,计算最终应纳税费的税基时,H应先对多计提并计入相关成本费用的部分进行相应的调增。调增数额为108 659 762.2元,还需补缴税款 108 659 762.2×25%=27 164 940.55 元。 所以在筹划时应尽量缩小实发与计提之间的差额。
综上所述,本研究利用报告基因表达检测的方法,以pEGFP-C1质粒为内参和启动子报告载体骨架,对孤雌后2~4 h胚胎注射,并在72 h后检测报告基因表达水平,评估启动子活性。分析猪基因翻译起始位点上游5000 bp,发现4个转录因子结合位点成簇分布的区域,类似于小鼠基因表达调控中超级增强子(super-enhancer)结构[41,42]。通过分析这4个区域对猪基因启动子活性的影响,发现存在NF-TA转录因子结合位点簇的关键区域,该区域的缺失导致基因启动子活性降低。本研究结果为猪基因启动子结构以及上游调控机制的研究提供了数据支持。
[1] Sarkar A, Hochedlinger K. The sox family of transcription factors: versatile regulators of stem and progenitor cell fate., 2013, 12(1): 15–30.
[2] Liang S, Furuhashi M, Nakane R, Nakazawa S, Goudarzi H, Hamada J, Iizasa H. Isolation and characterization of human breast cancer cells with sox2 promoter activity., 2013, 437(2): 205–211.
[3] Zhu F, Qian W, Zhang H, Liang Y, Wu M, Zhang Y, Zhang X, Gao Q, Li Y. Sox2 is a marker for stem-like tumor cells in bladder cancer., 2017, 9(2): 429–437.
[4] Stolzenburg S, Rots MG, Beltran AS, Rivenbark AG, Yuan X, Qian H, Strahl BD, Blancafort P. Targeted silencing of the oncogenic transcription factor sox2 in breast cancer., 2012, 40(14): 6725–6740.
[5] Wang Z, Oron E, Nelson B, Razis S, Ivanova N. Distinct lineage specification roles for nanog, oct4, and sox2 in human embryonic stem cells., 2012, 10(4): 440–454.
[6] Arnold K, Sarkar A, Yram MA, Polo JM, Bronson R, Sengupta S, Seandel M, Geijsen N, Hochedlinger K. Sox2(+) adult stem and progenitor cells are important for tissue regeneration and survival of mice., 2011, 9(4): 317–329.
[7] Hu Y H, Yao JH. Progress on pluripotency factors in zebrafish., 2012, 34(9): 1097–1107.胡雨, 姚纪花. 斑马鱼多能性因子的研究进展. 遗传, 2012, 34(9): 1097–1107.
[8] Rizzino A, Wuebben EL. Sox2/oct4: a delicately balanced partnership in pluripotent stem cells and embryogenesis., 2016, 1859(6): 780–791.
[9] White MD, Angiolini JF, Alvarez YD, Kaur G, Zhao ZW, Mocskos E, Bruno L, Bissiere S, Levi V, Plachta N. Long-lived binding of sox2 to DNA predicts cell fate in the four-cell mouse embryo., 2016, 165(1): 75–87.
[10] Avilion AA, Nicolis SK, Pevny LH, Perez L, Vivian N, Lovell-Badge R. Multipotent cell lineages in early mouse development depend on sox2 function., 2003, 17(1): 126–140.
[11] Wicklow E, Blij S, Frum T, Hirate Y, Lang RA, Sasaki H, Ralston A. Hippo pathway members restrict sox2 to the inner cell mass where it promotes icm fates in the mouse blastocyst., 2014, 10(10): e1004618.
[12] Liu S, Bou G, Sun R, Guo S, Xue B, Wei R, Cooney AJ, Liu Z. Sox2 is the faithful marker for pluripotency in pig: evidence from embryonic studies., 2015, 244(4): 619–627.
[13] Wu Z, Chen J, Ren J, Bao L, Liao J, Cui C, Rao L, Li H, Gu Y, Dai H, Zhu H, Teng X, Cheng L, Xiao L. Generation of pig induced pluripotent stem cells with a drug-inducible system., 2009, 1(1): 46–54.
[14] Gu Q, Hao J, Hai T, Wang J, Jia Y, Kong Q, Wang J, Feng C, Xue B, Xie B, Liu S, Li J, He Y, Sun J, Liu L, Wang L, Liu Z, Zhou Q. Efficient generation of mouse escs-like pig induced pluripotent stem cells., 2014, 5(5): 338–342.
[15] Esteban MA, Xu J, Yang J, Peng M, Qin D, Li W, Jiang Z, Chen J, Deng K, Zhong M, Cai J, Lai L, Pei D. Generation of induced pluripotent stem cell lines from tibetan miniature pig., 2009, 284(26): 17634–17640.
[16] West FD, Uhl EW, Liu Y, Stowe H, Lu Y, Yu P, Gallegos-Cardenas A, Pratt SL, Stice SL. Brief report: chimeric pigs produced from induced pluripotent stem cells demonstrate germline transmission and no evidence of tumor formation in young pigs., 2011, 29(10): 1640–1643.
[17] Fan N, Chen J, Shang Z, Dou H, Ji G, Zou Q, Wu L, He L, Wang F, Liu K, Liu N, Han J, Zhou Q, Pan D, Yang D, Zhao B, Ouyang Z, Liu Z, Zhao Y, Lin L, Zhong C, Wang Q, Wang S, Xu Y, Luan J, Liang Y, Yang Z, Li J, Lu C, Vajta G, Li Z, Ouyang H, Wang H, Wang Y, Yang Y, Liu Z, Wei H, Luan Z, Esteban MA, Deng H, Yang H, Pei D, Li N, Pei G, Liu L, Du Y, Xiao L, Lai L. Piglets cloned from induced pluripotent stem cells., 2013, 23(1): 162–166.
[18] Brevini T, Pennarossa G, Maffei S, Gandolfi F. Pluripotency network in porcine embryos and derived cell lines., 2012, 47(Suppl. 4): 86–91.
[19] Roberts RM, Yuan Y, Genovese N, Ezashi T. Livestock models for exploiting the promise of pluripotent stem cells., 2015, 56(1): 74–82.
[20] Goolam M, Scialdone A, Graham SJL, Macaulay IC, Jedrusik A, Hupalowska A, Voet T, Marioni JC, Zernicka- Goetz M. Heterogeneity in oct4 and sox2 targets biases cell fate in 4-cell mouse embryos., 2016, 165(1): 61–74.
[21] Yang N, Wang Y, Hui L, Li X, Jiang X. Silencing sox2 expression by rna interference inhibits proliferation, invasion and metastasis, and induces apoptosis through map4k4/jnk signaling pathway in human laryngeal cancer tu212 cells., 2015, 63(9): 721–733.
[22] Rinne A, Banach K, Blatter LA. Regulation of nuclear factor of activated t cells (nfat) in vascular endothelial cells., 2009, 47(3): 400–410.
[23] Wiebe MS, Wilder PJ, Kelly D, Rizzino A. Isolation, characterization, and differential expression of the murine sox-2 promoter., 2000, 246(1–2): 383–393.
[24] Lis M, Walther D. The orientation of transcription factor binding site motifs in gene promoter regions: does it matter?, 2016, 17: 185.
[25] Sikorska M, Sandhu JK, Deb-Rinker P, Jezierski A, Leblanc J, Charlebois C, Ribecco-Lutkiewicz M, Bani-Yaghoub M, Walker PR. Epigenetic modifications of sox2 enhancers, srr1 and srr2, correlate with in vitro neural differentiation., 2008, 86(8): 1680– 1693.
[26] Mojsin M, Topalovic V, Marjanovic Vicentic J, Stevanovic M. Transcription factor nf-y inhibits cell growth and decreases sox2 expression in human embryonal carcinoma cell line nt2/d1., 2015, 80(2): 202– 207.
[27] Wiebe MS, Wilder PJ, Kelly D, Rizzino A. Isolation, characterization, and differential expression of the murine sox-2 promoter., 2000, 246(1–2): 383–393.
[28] Di Stefano B, Sardina JL, van Oevelen C, Collombet S, Kallin EM, Vicent GP, Lu J, Thieffry D, Beato M, Graf T. C/EBPαpoises b cells for rapid reprogramming into induced pluripotent stem cells., 2014, 506(7487): 235–239.
[29] Bueno C, Sardina JL, Di Stefano B, Romero-Moya D, Muñoz-López A, Ariza L, Chillón MC, Balanzategui A, Castaño J, Herreros A, Fraga MF, Fernández A, Granada I, Quintana-Bustamante O, Segovia JC, Nishimura K, Ohtaka M, Nakanishi M, Graf T, Menendez P. Reprogramming human b cells into induced pluripotent stem cells and its enhancement by c/EBPα., 2016, 30(3): 674–682.
[30] Borrelli S, Fanoni D, Dolfini D, Alotto D, Ravo M, Grober OM, Weisz A, Castagnoli C, Berti E, Vigano MA, Mantovani R. C/EBPδgene targets in human keratinocytes., 2010, 5(11): e13789.
[31] Kel A, Kel-Margoulis O, Babenko V, Wingender E. Recognition of nfatp/ap-1 composite elements within genes induced upon the activation of immune cells., 1999, 288(3): 353–376.
[32] Mantovani R. A survey of 178 nf-y binding ccaat boxes., 1998, 26(5): 1135–1143.
[33] Grange T, Roux J, Rigaud G, Pictet R. Cell-type specific activity of two glucocorticoid responsive units of rat tyrosine aminotransferase gene is associated with multiple binding sites for c/ebp and a novel liver-specific nuclear factor., 1991, 19(1): 131–139.
[34] Roth C, Schuierer M, Günther K, Buettner R. Genomic structure and DNA binding properties of the human zinc finger transcriptional repressor ap-2rep (klf12)., 2000, 63(3): 384–390.
[35] Cao S, Han J, Wu J, Li Q, Liu S, Zhang W, Pei Y, Ruan X, Liu Z, Wang X, Lim B, Li N. Specific gene-regulation networks during the pre-implantation development of the pig embryo as revealed by deep sequencing., 2014, 15: 4.
[36] Hilger-Eversheim K, Moser M, Schorle H, Buettner R. Regulatory roles of ap-2 transcription factors in vertebrate development, apoptosis and cell-cycle control., 2000, 260(1–2): 1–12.
[37] Macián F, López-Rodriguez C, Rao A. Partners in transcription: Nfat and ap-1., 2001, 20(19): 2476–2489.
[38] Ning Ding, Yuan Gao, Wang N, Li H. Functional analysis of the chicken pparγ gene 5′flanking region and c/EBPα mediated gene regulation., 2011, 158(4): 297–303.
[39] Cheng M, Zhang WJ, Xing TY, Yan XH, Li YM, Li H, Wang N. Functional analysis of the upstream regulatory region of chicken mir-17-92 cluster., 2016, 38(8): 724–735.程敏, 张文建, 邢天宇, 闫晓红, 李玉茂, 李辉, 王宁. 鸡miR-17-92基因簇上游调控区功能分析. 遗传, 2016, 38(8): 724–735.
[40] Yu L, Domann FE. Rapid and direct quantitative rt-pcr method to measure promoter activity., 2006, 22(5): 1461–1463.
[41] Zhang S, Magnusson G. Kilham polyomavirus: activation of gene expression and DNA replication in mouse fibroblast cells by an enhancer substitution., 2001, 75(21): 10015–10023.
[42] Whyte WA, Orlando DA, Hnisz D, Abraham BJ, Lin CY, Kagey MH, Rahl PB, Lee TI, Young RA. Master transcription factors and mediator establish super-enhancers at key cell identity genes., 2013, 153(2): 307–319.
Analysis ofgene promoter activity in porcine early embryonic development
Jianchao Zhao, Zhuang Chai, Shimeng Guo, Zhonghua Liu
SOX2 (sex determining region Y-box2) is one of the critical pluripotent factors that play a crucial role in the first lineage differentiation and maintenance of pluripotency in inner cell mass during early embryonic development. However, there are few researches about the regulation of thepromoter, especially in. To analyzed the activity ofpromoter in early porcine embryos, we determined the control system and established the microinjection system for assessingpromoter activity by analyzing the embryonic development and the expression of enhanced green fluorescence protein (EGFP) after micro-injected different EGFP plasmids at different times after activation of the oocytes. Then, we analyzed the structure of 5000 bp upstream of thetranslation initiation site and found there were four transcription factor binding site clusters. Next, we designed and constructed promoter-containing plasmids to analyze the function of each cluster. To detect the activity of different promoters, we assessed the mCherry expression in protein levels and mRNA levels by analyzing the mCherry fluorescence intensity and qRT-PCR after injecting plasmids into embryos. These results showed that the activity of the shorted promoter, with the region from 2254 bp to 2442 bp upstream of translation initiation site deleted, decreased to 17.8% at 4-cell and 8-cell stages compared with the full-length promoter. This region included two NF-AT transcription factor binding sites, which indicated that the NF-AT binding site is a key region to regulate the activity of thepromoter. The results provide important data for determination the mechanism of porcineregulation.
gene; promoter activity; pig
2019-02-21;
2019-06-17
国家自然科学基金面上项目(编号:31872360)资助[Supported by the National Natural Science Foundation of China (No. 31872360)]
赵剑超,硕士研究生,专业方向:发育生物学。E-mail: arabidopsis@yeah.net
刘忠华,教授,博士生导师,研究方向:早期胚胎发育与猪干细胞研究。E-mail: liuzhonghua@neau.edu.cn
10.16288/j.yczz.19-045
2019/7/5 14:07:50
URI: http://kns.cnki.net/kcms/detail/11.1913.R.20190705.1407.002.html
(责任编委: 李明洲)

