液相色谱质谱联用仪测定沙丁胺醇的不确定度评定


摘 要:目的:全面地分析液相色谱-串联质谱法测定沙丁胺醇的不确定度来源与影响不确定度的因素。在测量结果处于临界状态时,对测量结果作出正确判定。方法:通过建立数学模型,依据JJF 1059.1-2012《测量不确定度评定与表示》、JJG 196-2006《常用玻璃量器检定规程》和GB/T 22286-2008《动物源性食品中多种β-受体激动剂残留量的测定 液相色谱串联质谱法》的规定,逐层对测量过程中的不确定度来源进行分析,最后给出合成不确定度和扩展不确定度。结果:按照GB/T 22286-2008《动物源性食品中多种β-受体激动剂残留量的测定 液相色谱串联质谱法》测定沙丁胺醇的不确定度为1.54 μg/kg。
关键词:瘦肉精;沙丁胺醇;液质联用
测量不确定度是表征合理的赋予被测量值的分散性、与测量结果相联系的参数,测量不确定度的大小反映了测量结果的质量高低,完整的测量结果应该包括测量不确定度。从实验过程的数学模型,分析实验过程的不确定度主要来源,对不确定度分量进行计算并评定,使该不确定度为今后改善β-受体激动剂残留量检测的测量程序,提高实验测量精密度和准确性提供理论依据[1]。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
市售猪肉;PCX固相萃取柱(60 mg,3 mL)。
1.1.2 试剂
β-葡萄糖醛苷酸酶、乙酸铵(分析纯)、氨水(分析純,含量:25%~28%)、乙腈(色谱纯)、甲醇(色谱纯)、甲酸(分析纯)与沙丁胺醇标准物质溶液(编号:SB05-201-2008;产品批号:201901;北京坛墨质检科技有限公司;浓度:100 μg/mL)。
1.2 仪器设备与条件
1.2.1 仪器
岛津制作所(日本.京都)串联四级杆液质联用仪LCMS-8045;JJ500电子天平(常熟市双杰测试仪器厂);V6旋涡混合器(广州科桥实验技术设备有限公司);SB-5200DTD型超声仪(宁波新艺超声设备有限公司);DK-S24恒温水浴锅(上海森信实验仪器有限公司);E3115台式微量高速离心机(美国安胜科技有限公司);Fotector-02HT固相萃取装置(睿科仪器有限公司);GM-0.5A真空泵(天津市津腾实验设备有限公司);N150-氮吹仪(广州安胜仪器有限公司)。
1.2.2 色谱条件
色谱柱为Shim-pack GIST C18(50 mm×2.1 mm,2 μm);进样量:10 μL;流速为0.4 mL/min;柱温为30 ℃;流动相为A-0.1%甲酸/水:B-0.1%甲酸/乙腈,梯度洗脱,具体比例见表1。
1.2.3 质谱条件
干燥气为氮气,流速15 L/min,温度350 ℃;雾化气:氮气,3.0 L/min;碰撞气:氩气;DL温度:250 ℃;加热模块温度:400 ℃;电喷雾电离正离子模式ESI(+);离子喷雾电压4 500 V;质谱扫描方式:多反应离子监测(MRM);驻留时间:20 ms;延迟时间:3 ms[2]。
1.3 标准溶液的配制
1.3.1 标准储备液
准确移取沙丁胺醇标准品溶液
1 mL(浓度:100 μg/mL)于50 mL容量瓶中,用甲醇定容至刻度,此溶液浓度为2 μg/mL,于4 ℃冰箱中保存,有效期3个月。
1.3.2 标准工作液
根据需要,将标准储备液配制成适当浓度的标准工作液,标准工作液在使用前配制。
1.4 数学模型
该检测过程中的数学模型见式(1)。
(1)
式(1)中:X-样品中沙丁胺醇含量(μg/kg);c-标准曲线校准后试液中沙丁胺醇的浓度(ng/mL);v-试液定容体积(mL);m-试样质量(g);f-加标回收率。
2 各个分量不确定度的评定
2.1 标准物质及其配制过程引入的不确定度
根据标准物质证书信息,沙丁胺醇标准物质的不确定度为0.05 μg/mL,按正态分布考虑,包含因子为K=3,属于B类评定,故其相对不确定度为U1rel=0.05/3=1.67×10-2。
2.2 标准溶液配制过程引入的不确定度
2.2.1 标准溶液配制过程中玻璃仪器校准引入的不确定度
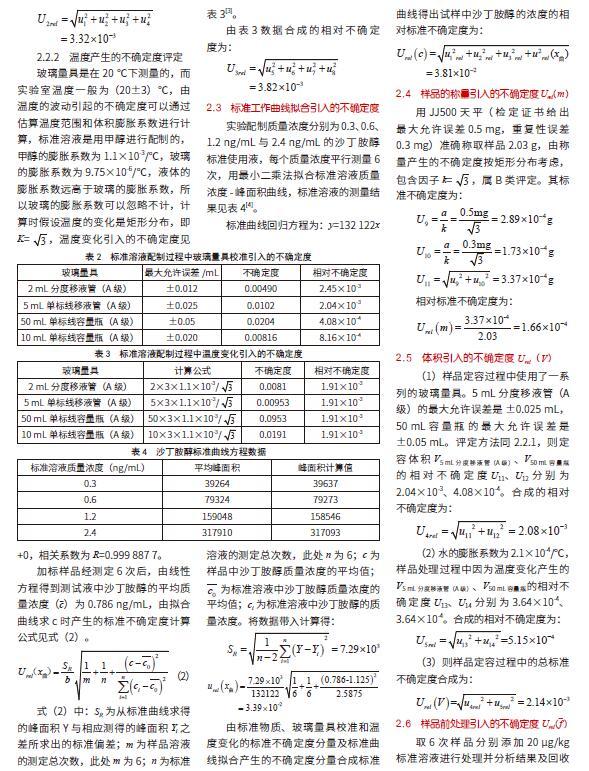
标准溶液在配制过程中使用了一系列的玻璃器具,按照JJG 196-2006《常用玻璃量具检定规程》的要求,均有相应的最大允差。欧洲分析化学中心(EU-RACHEM)认为其服从三角分布,故K=,计算不确定度分量。玻璃量具校准的不确定度见表2。
由表2中的数据合成的相对不确定度为:
2.2.2 温度产生的不确定度评定
玻璃量具是在20 ℃下测量的,而实验室温度一般为(20±3)℃,由温度的波动引起的不确定度可以通过估算温度范围和体积膨胀系数进行计算,标准溶液是用甲醇进行配制的,甲醇的膨胀系数为1.1×10-3/℃,玻璃的膨胀系数为9.75×10-6/℃,液体的膨胀系数远高于玻璃的膨胀系数,所以玻璃的膨胀系数可以忽略不计,计算时假设温度的变化是矩形分布,即K=,温度变化引入的不确定度见表3[3]。
由表3数据合成的相对不确定
度为:
2.3 标准工作曲线拟合引入的不确定度
实验配制质量浓度分别为0.3、0.6、1.2 ng/mL与2.4 ng/mL的沙丁胺醇标准使用液,每个质量浓度平行测量6次,用最小二乘法拟合标准溶液质量浓度-峰面积曲线,标准溶液的测量结果见表4[4]。
标准曲线回归方程为:y=132 122x
+0,相关系数为R=0.999 887 7。
加标样品经测定6次后,由线性方程得到测试液中沙丁胺醇的平均质量浓度(c)为0.786 ng/mL,由拟合曲线求c时产生的标准不确定度计算公式见式(2)。
(2)
式(2)中:SR为从标准曲线求得的峰面积Y与相应测得的峰面积Yi之差所求出的标准偏差;m为样品溶液的测定总次数,此处m为6;n为标准溶液的测定总次数,此处n为6;c为样品中沙丁胺醇质量浓度的平均值;为标准溶液中沙丁胺醇质量浓度的平均值;ci为标准溶液中沙丁胺醇的质量浓度。将数据带入计算得:
由标准物质、玻璃量具校准和温度变化的标准不确定度分量及标准曲线拟合产生的不确定度分量合成标准曲线得出试样中沙丁胺醇的浓度的相对标准不确定度为:
2.4 样品的称量引入的不确定度Urel(m)
用JJ500天平(检定证书给出最大允许误差0.5 mg,重复性误差
0.3 mg)准确称取样品2.03 g,由称量产生的不确定度按矩形分布考虑,包含因子k=,属B类评定。其标准不确定度为:
相对标准不确定度为:
2.5 体积引入的不确定度Urel(V)
(1)样品定容过程中使用了一系列的玻璃量具。5 mL分度移液管(A级)的最大允许误差是±0.025 mL,
50 mL容量瓶的最大允许误差是±0.05 mL。评定方法同2.2.1,则定容体积V5 mL分度移液管(A级)、V50 mL容量瓶
的相对不确定度U11、U12分别为2.04×10-3、4.08×10-4。合成的相对不确定度为:
(2)水的膨胀系数为2.1×10-4/℃,
样品处理过程中因为温度变化产生的V5 mL分度移液管(A级)、V50 mL容量瓶的相对不确定度U13、U14分别为3.64×10-4、3.64×10-4。合成的相对不确定度为:
(3)则样品定容过程中的总标准不确定度合成为:
2.6 样品前处理引入的不确定度Urel(f)
取6次样品分别添加20 μg/kg标准溶液进行处理并分析结果及回收率。6次检测平均值为19.71 μg/kg,回收率测定结果为95.6%、97.8%、99.0%、101.0%、99.4%与96.6%,平均回收率为f=98.2%,标准偏差为Sf=1.96%,标准不确定度采用平均值的标准偏差,标准不确定度和相对标准不确定度分别为:
2.7 合成标准不确定度
将2.1~2.6各分量的不确定度合成得:
2.8 扩展不確定度
扩展标准不确定度:U=kUrel(X)=2×0.039=0.078。
由2.6中6次检测平均值为19.71 μg/kg,则扩展不确定度为:U=19.71 μg/kg×0.078=1.54μg/kg。
3 测量不确定度报告
按照GB/T 22286-2008 《动物源性食品中多种β-受体激动剂残留量的测定 液相色谱串联质谱法》测定猪肉中沙丁胺醇的结果为:C=(19.71±1.54)μg/kg,k=2。
参考文献
[1]国家质量监督检验检疫总局.JJF 1059.1-2012 测量不确定度评定与表示[S].北京:中国标准出版社,2012.
[2]国家质量监督检验检疫总局.GB/T 22286-2008 动物源性食品中多种β-受体激动剂残留量的测定 液相色谱串联质谱法[S].北京:中国标准出版社,2006.
[3]国家质量监督检验检疫总局.JJG 196-2006 常用玻璃量器检定规程[S].北京:中国标准出版社,2006.
[4]陈佳,乔菲,金红宇,等.ICP—MS法测定马钱子中重金属及有害元素含量的不确定度评定[J].药物分析杂志,2013(12):2176-2182.
基金项目:潮州市2018年广东省科技创新战略专项资金专题10:潮州市食品检测公共平台建设(编号:2018SS21)。
作者简介:陈楠瑜(1980—),男,广东潮州人,本科,食品检验工程师。研究方向:食品检验、检验室管理、食品生产企业质量管理体系的建立和生产许可现场核查等。

