阿法替尼治疗非小细胞肺癌患者致严重的药品不良反应影响因素的Logistic回归分析Δ
谭鑫宇,张 欢,张 杰,王怡鑫
(1.遂宁市中心医院药剂科,四川 遂宁 629000; 2.成都市药品不良反应监测中心药品不良事件管理办公室,四川 成都 610042; 3.四川省肿瘤医院/电子科技大学医学院附属肿瘤医院药学部,四川 成都 610041)
肺癌是临床最常见的恶性肿瘤之一,每年约有140余万例患者死于肺癌,占恶性肿瘤总死亡人数的18.2%[1]。非小细胞肺癌(non-small cell lung cancer,NSCLC)占肺癌病理类型的75%~80%,晚期NSCLC患者的5年生存率仅为10%~15%[2]。目前,阿法替尼作为最新型的表皮生长因子受体拮抗剂,用于晚期腺癌的NSCLC患者,预后优于含铂类药物化疗方案,疗效显著[3-5];但该药严重的药品不良反应(adverse drug reaction,ADR)也较多,常见的严重的ADR有腹泻、氨基转移酶升高、肾损伤、皮疹及口腔炎等[4-5]。评价阿法替尼用于NSCLC的安全性,了解其导致严重的ADR的因素,为其临床安全应用提供参考,对减少该药致ADR的发生有重要意义。
1 资料与方法
1.1 资料来源
调取2017年1月至2018年8月四川省肿瘤医院(以下简称“我院”)使用马来酸阿法替尼片(生产厂家:Boehringer Ingelheim PHarman GmbH &Co.KG;批准文号:国药准字J20170028;规格:30或40 mg/粒,)的所有晚期NSCLC患者病历资料,共96份,其中发生严重的ADR的病历共24份。阿法替尼大多数为口服,院外治疗,科室护士常规随访(每周进行1次电话询问,主要询问患者坚持服药情况以及身体基本情况,对于发生ADR的患者评估后给予建议,必要时返院治疗)。发生严重的ADR的界定标准为:患者不能耐受腹泻(不良事件通用术语标准:Ⅲ度)、皮疹/痤疮症状较重需暂停服药或返院治疗,医院监测肝功能,氨基转移酶水平升高>3倍正常值上限,肌酐清除率低于正常值,视为阿法替尼发生严重的ADR病例[6-7]。
1.2 方法
采用回顾性调查分析方法,翻阅患者相关病历资料以及各科室电话随访资料,收集患者药物过敏史、药物服用时间、既往药物治疗情况、体质量指数(BMI)、肝功能、年龄、性别、内科并发症(高血压病、糖尿病等)和阿法替尼服用剂量、服用时间等信息[8-9]。
1.3 统计学方法
以是否发生严重的ADR为因变量,以药物过敏史、性别、年龄、服用剂量和时间、既往治疗情况、BMI及肝功能等因素为自变量,进行单因素分析。年龄和BMI作为计数变量,采用两样本t检验,对发生严重的ADR组和未发生严重的ADR组进行统计学分析;对其余计量变量的因素进行非条件Logistic回归分析[10]。采用SPSS 22.0统计学软件中非条件Logistic回归模块对数据进行回归分析。
2 结果
2.1 患者一般情况
96例患者中,未发生严重ADR患者的平均年龄为(58.06±8.13)岁,发生过敏患者的平均年龄为(59.08±8.48)岁;未发生ADR患者的平均BMI为(22.25±2.02)kg/m2,发生ADR患者的平均BMI为(22.52±2.13)kg/m2;男性患者55例(占57.29%),女性患者41例(占42.71%);仅11例患者有过敏史(占11.46%),其中仅1例患者发生严重的ADR(仅占11例患者的9.09%);阿法替尼服用剂量多以40 mg,1日1次为主,共84例(占87.50%),服用低剂量(30 mg,1日1次)的患者中仅有2例发生严重的ADR;服药时间>3个月的患者共64例(占66.67%),其中发生严重的ADR的患者共19例(占64例患者的29.69%);有内科并发症的患者共24例(占25.00%),其中14例患者发生严重的ADR(占24例患者的58.33%);服药前3个月内接受过化疗的患者共22例(占22.92%),其中13例患者发生严重的ADR(占22例患者的59.09%)。
2.2 阿法替尼致严重的ADR影响因素的单因素分析
把数据分为发生严重的ADR组和未发生严重的ADR组,对可能影响严重的ADR结果的两组计数变量年龄和BMI进行t检验;对可能影响结果的其他计量变量进行χ2检验。t检验结果显示,发生、未发生严重的ADR组患者的年龄、BMI的差异均无统计学意义(P>0.05)。χ2检验结果显示,服用靶向药物时间和是否有内科并发症对严重的ADR的发生有显著影响(P<0.05),其余各变量对严重的ADR的发生无显著影响(P>0.05),见表1。
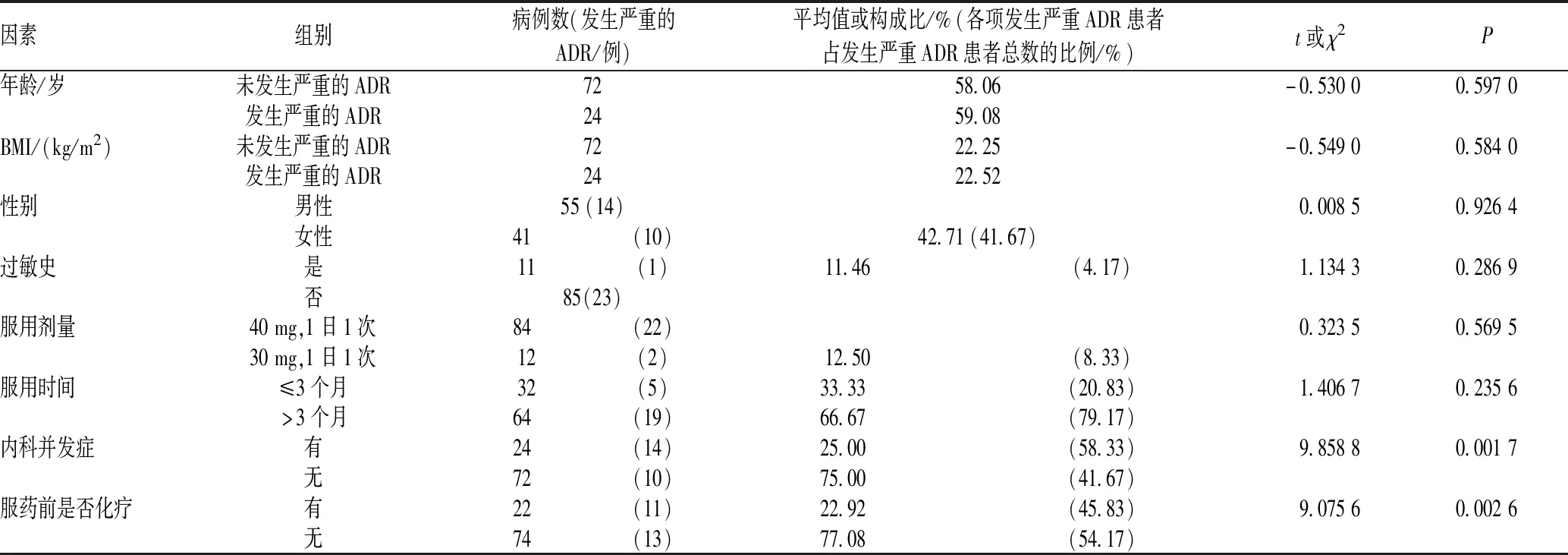
表1 阿法替尼致严重的ADR影响因素的单因素分析Tab 1 Univariate analysis of factors affecting severe ADR caused by afatinib
2.3 阿法替尼致严重的ADR影响因素的多因素、非条件Logistic回归分析
以单因素分析所得的关联为基础,以患者年龄、服用靶向药物时间和是否有内科并发症为自变量进行多因素、非条件Logistic回归分析。选择SPSS 22.0分析工具,选择Logistic回归分析,以是否发生严重的ADR为因变量,患者年龄、服用靶向药物时间和是否有内科并发症为协变量,方法选择为“输入”,结果见表2。
3 讨论
单因素分析阿法替尼导致严重的ADR危险因素计数数据比较结果显示,发生严重的ADR组患者平均年龄约为58岁,未发生严重的ADR组患者约为59岁,两组的差异无统计学意义(P>0.05),但高龄仍是ADR发生的较重要的因素[11]。单因素分析BMI结果显示,发生、未发生严重的ADR组患者平均BMI的差异很小,而BMI与体表面积成正相关,说明本研究纳入的患者BMI基线一致,因此,BMI对分析结果的影响不明显。

表2 阿法替尼致严重的ADR影响因素的多因素、非条件Logistic回归分析Tab 2 Multivariate and unconditional Logistic regression analysis of the influential factors of serious ADR caused by alfaitinib
单因素分析的计量数据结果显示,发生严重的ADR患者的性别没有差异,提示该药致ADR发生可能与性别无关;仅有11例患者记录有药物过敏史,但是否发生严重的ADR的差异无统计学意义(P>0.05),说明患者其他药物过敏史与阿法替尼致严重的ADR发生联系不明显,这可能与阿法替尼的药物作用靶点和机制有关[12-13],另外,患者病历信息中过敏史多为患者主诉,因此有漏报的可能。
服用阿法替尼的患者中,药物服用时间方面,我院临床肿瘤治疗每3个月需进行大型检查,以评估治疗效果或疾病进展情况,而ADR的发生与药物持续应用时间有一定关系[14]。因此,以3个月评估疗效时作为分界,来判断累积服用时间长短是否与严重的ADR发生有联系。通过单因素分析结果可见,服用时间的长短与严重的ADR的发生概率成正相关,服药时间越长,特别是连续服用>3个月评估期,发生严重的ADR的概率越高,说明ADR可能存在剂量累积效应。
本研究中,24例患者合并内科常见并发症,其中8例合并高血压病,10例合并糖尿病,2例合并慢性阻塞性肺疾病,4例同时合并高血压病、糖尿病。通过单因素分析,上述24例患者严重的ADR发生率与普通患者的差异有统计学意义(P<0.05)。分析其原因,存在基础疾病的患者,其病理生理状态发生变化,且高血压病等需长期服用药物,可能引起不可预料的生物效应,导致严重的ADR发生概率增加。
本研究中,22例患者在服用阿法替尼前3个月内进行了化疗,化疗方案包括紫杉醇+铂类药物、吉西他滨+铂类药物或培美曲塞二钠+铂类药物。化疗药的不良反应较大,可能对患者身体造成一定影响,也可能间接导致服用阿法替尼后严重的ADR发生率升高。单因素分析结果显示,化疗患者与未化疗患者服用阿法替尼后发生严重的ADR病例数所占比例的差异有统计学意义(P<0.05),也反映靶向药物与化疗联合治疗可能会导致ADR发生概率增加。
对有统计学差异的影响因素进行非条件Logistic回归分析结果显示,内科并发症、服药前是否化疗2个因素均对发生严重的ADR有显著影响,其OR分别为3.59、9.28,即有内科并发症的患者服用阿法替尼发生严重的ADR的概率是没有并发症患者的3.59倍;在控制其他因素条件下,患者近期进行过化疗,发生严重的ADR的风险提高9.28倍[15]。
文献报道,阿法替尼累积发生率居前3位的ADR分别为腹泻、口腔炎和皮疹,其余ADR如乏力、食欲减退、恶心及呕吐等与第1代酪氨酸激酶抑制剂类似[16]。我院服用阿法替尼患者发生的严重的ADR主要为严重皮疹和腹泻,严重口腔炎少见。针对腹泻,临床可应用蒙脱石散等止泻药对症处理;对于严重皮疹,应经专科医师会诊评估后对症处理,一般可外用类固醇类药物,合并感染者可外用抗菌药物;如果发生不能耐受的ADR,必要时需停药。综上所述,阿法替尼的临床疗效显著,但应嘱咐患者密切观察服药后ADR发生情况,尤其是合并化疗和内科并发症的患者,如发生严重的ADR而不能耐受,应嘱咐患者返院处理。

