厄他培南对比头孢曲松治疗成人复杂性尿路感染的Meta分析
高玲燕,刘雨玲,满春霞,刘 桦
(航天中心医院 药剂科,北京 100049)
复杂性尿路感染(complicated urinary tract infection,cUTI)是指尿路感染同时伴有获得感染或者治疗失败风险的合并疾病[1]。cUTI的经验性治疗方案包括氟喹诺酮类、2代或3代头孢菌素、磷霉素氨丁三醇、脲基青霉素联合β内酰胺酶抑制剂和碳青霉烯类[1,2]。
头孢曲松(ceftriaxone,CRO)属于第三代头孢菌素,具有半衰期长、安全性好、经肾排泄及尿中浓缩等优势[3~5]。 厄他培南(Ertapenem,EPT)属于 I类碳青霉烯类抗生素,具有半衰期长、尿中浓缩、对产超广谱β-内酰胺酶(extended-spectrum beta-lactamases,ESBL)和 AmpC 酶稳定、不引起铜绿假单菌耐药性增加等特点[6]。CRO和EPT均被广泛用于cUTI的治疗,但二者优劣尚无定论 。本研究对已发表的EPT与CRO治疗cUTI的RCT研究进行Meta分析,评价2种药物的有效性和安全性。
1 资料与方法
1.1 文献检索
计算机检索 PubMed、EMbase、Cochrane、CNKI、SinoMed、维普和万方数据库,检索时限均为各数据库建库起至2019年3月。中文检索词为厄他培南、头孢曲松、尿路感染、肾盂肾炎、尿道炎、膀胱炎;英文检索词为Ertapenem、Ceftriaxone、Urinary tract infections、Pyelonephritis、Urethritis、Cystitis。
1.2 文献的纳入与排除
1.2.1 纳入标准
(1)研究对象为成人 cUTI患者;(2)干预措施中试验组为EPT,对照组为CRO;(3)结局指标为关于有效性、安全性和耐受性评价的数据;(4)原始文献为随机对照试验(randomized controlled trial,RCT)。
1.2.2 排除标准
(1)非 RCT 研究;(2)综述性文献;(3)数据不完整研究;(4)药动学或药理学参数研究;(5)临床试验总结型文献等。
1.3 资料提取与质量评价
由2位研究者按照纳入和排除标准独立筛选文献,如遇分歧则讨论解决或由第三方协助裁定。按照预先设计好的表格对纳入文献提取资料。
依据Cochrane Reviewers'Handbook系统评价手册关于RCT质量评价标准进行评估:(1)随机方法是否正确和充分;(2)是否采用盲法;(3)分配隐藏是否正确和充分;(4)是否全程随访,是否报告失访人数,失访人数是否在10%以内;(5)是否选择性报告研究结果;(6)是否有其他偏倚来源。
1.4 统计学方法
采用Review Manager 5.3对纳入研究的细菌清除率、不良反应发生率的RR值(relative risk)与95%CI(confidence interval)作为指标,绘制Meta分析森林图。研究间的异质性使用I2进行评估,如果I2>50%,说明研究间存在较大的异质性,用随机效应模型进行合并分析,如果I2≤50%,说明研究间异质性低,用固定效应模型进行合并分析[7,8]。
2 结果
2.1 纳入文献及研究基本信息
共检索到110篇文献(PubMed 33篇、Embase 62篇、Cochrane 10篇、SinoMed 2篇、CNKI 2篇、万方1篇),排除重复文献、通过阅读摘要明显不符合纳入标准的研究,最后细读文献,纳入3篇符合标准、数据完整的关于EPT与CRO治疗成人cUTI的 RCT 研究[9~11]。
表1展示了纳入研究信息,研究均为多中心双盲随机对照试验,且均对失访和退出情况进行了说明。共纳入1121例患者,且均为符合疾病定义标准的>18周岁的需要使用胃肠外抗菌药物治疗的cUTI患者。3个RCT研究试验组治疗方案为 EPT 1g,Qd,对照组为 CRO 1g,Qd,Park 的研究中对照组为CRO 2g,Qd。研究的疗程均为至少连续3次使用EPT和CRO后转换成口服抗菌药物,其中注射疗程平均为4.78d,总疗程平均为12.73d,符合cUTI推荐的10~14d的治疗疗程[5]。有效性方面,均提供了注射疗程结束后(discontinuation of intravenous therapy,DCIV)和治疗 5~9d后(test of cure,TOC)的细菌清除率。安全性和耐受性方面,均报道了临床不良反应、实验室不良反应及局部注射部位反应发生率。3个研究的Jadad评分分别为4分、4分和5分。
2.2 纳入研究的偏倚风险评价
利用Stata 12软件对细菌清除率、不良反应发生率进行Egger检验:TOC的细菌清除率P=0.401,DCIV的细菌清除率P=0.595,临床不良反应发生率P=0.099,实验室不良反应发生率P=0.536,表明发表偏倚的可能性较小。
2.3 Meta分析结果
2.3.1 有效性
分析TOC的合计细菌清除率,EPT组为89.13%、CRO组为90.51%,同质性检验χ2=0.07、P=0.96、I2=0%,提示无异质性,故采用固定效应模型计算 RR 合并值 0.99(95%CI:0.94~1.05),不同药物组细菌清除率总效应Z=0.28,P=0.78,无显著性差异(见图1A)。表明胃肠外加口服治疗疗程后,EPT与CRO的细菌清除效果无统计学差异。
分析DCIV的合计细菌清除率,EPT组为98.71%、CRO组为95.45%,同质性检验χ2=1.54、P=0.46、I2=0%,提示无异质性,故采用固定效应模型计算 RR 合并值 1.03(95%CI:1.00~1.06),不同药物组细菌清除率总效应Z=2.23,P=0.03,有显著性差异(见图1B)。表明EPT在DCIV的细菌清除效果优于CRO。
2.3.2 安全性
EPT与CRO的临床不良反应主要是恶心、腹泻、呕吐、头痛,实验室不良反应主要是丙氨酸转氨酶和天冬氨酸转氨酶升高。临床方面,EPT组的合计不良反应发生率为20.17%、CRO组为17.16%。异质性检验显示 χ2=3.59,P=0.17,I2=44%,提示无异质性,故采用固定效应模型计算RR 合并值为 1.27(95%CI:0.99-1.62),合并效应量的检验结果Z=1.90、P=0.06,无显著性差异(见图1C)。实验室方面,EPT组的合计不良反应发生率为6.00%、CRO组为5.33%。异质性检验显示χ2=1.21,P=0.55,I2=0%,提示无异质性,故采用固定效应模型计算 RR合并值为 1.15(95%CI:0.72-1.86),合并效应量的检验结果Z=0.59、P=0.56,无显著性差异(见图1D)。
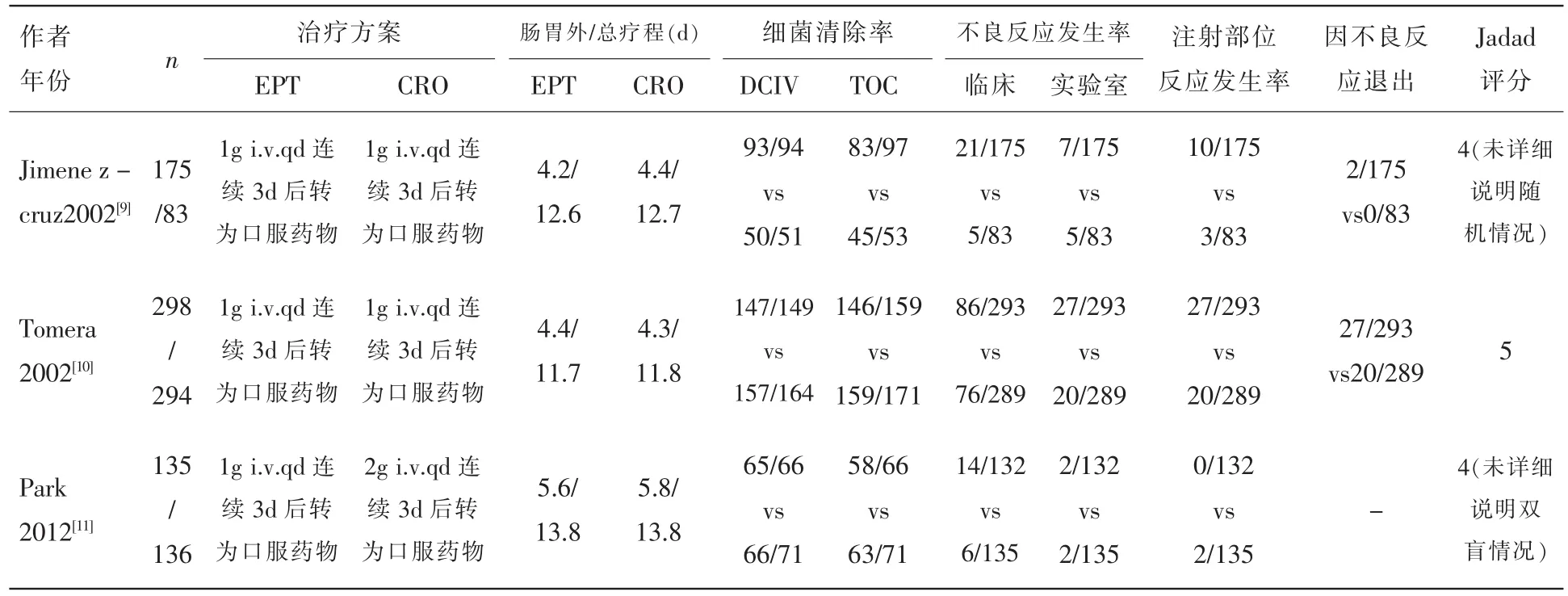
表1 纳入研究的基本信息(EPT vs CRO)
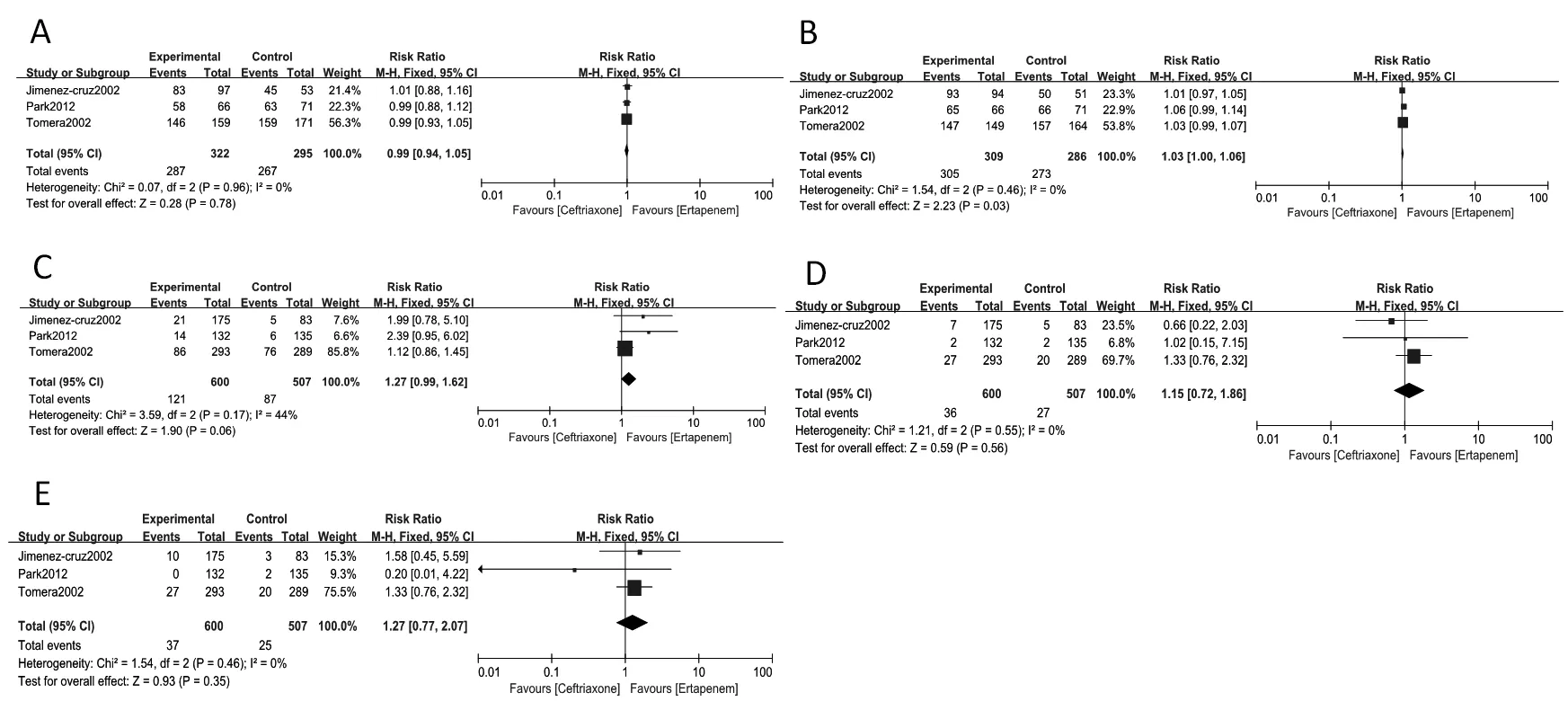
图1 EPT与CRO治疗cUTI时的细菌清除率、不良反应及耐受性比较森林图
2.3.3 耐受性
EPT与CRO主要的局部注射部位反应是静脉炎、压痛。EPT组的合计局部注射部位反应发生率为6.17%、CRO组为4.93%。异质性检验显示χ2=1.54,P=0.46,I2=0%,提示无异质性,故采用固定效应模型计算得到RR值为 1.27(95%CI为0.77~2.07),合并效应量的检验结果 Z=0.93、P=0.35,无显著性差异(见图1E)。
3 讨论
Meta分析结果显示,在胃肠外加口服疗程中,EPT与CRO治疗cUTI的有效性、安全性及耐受性均无统计学差异,而胃肠外治疗阶段,EPT治疗有效性优于CRO。分析原因可能为尿路感染致病菌模式的改变,即产ESBLs耐药菌株比例的增加。而头孢类抗菌药物对治疗ESBLs阳性菌的疗效差异很大,研究结果显示,头孢菌素对ESBLs阳性致病菌的敏感性只有1.1%,而对不产ESBLs的病原菌可达到96.7%,而EPT却对多种酶稳定,包括 ESBLs和 AmpC酶[12,13]。 3个 RCT提供的尿路感染致病菌分布及敏感性情况均提示ESBLs菌株的出现,所以这可能是导致EPT在静脉注射疗程结束时显示出更好细菌清除效果的原因。
本研究的优势是所纳入的文献质量较高,具有多方面的一致性,同时考虑了抗生素的耐药性,更具有参考意义。国内暂无2种药物治疗cUTI的药效学及安全性比较,本研究填补了国内研究的空白。不足是所纳入的研究时间间距较大。此外,由于抗生素耐药性会随着时间变化,所以耐药性监测数据应定期公开,更多的关于EPT与CRO治疗cUTI的研究应该展开。

