火焰合成Cu基催化剂在甲烷催化燃烧中的烧结行为
孟令泉,陈 欣,徐祖伟,赵海波
火焰合成Cu基催化剂在甲烷催化燃烧中的烧结行为
孟令泉1, 2,陈 欣1,徐祖伟1,赵海波1
(1. 华中科技大学煤燃烧国家重点实验室,武汉 430074;2. 华中科技大学中欧清洁与可再生能源学院,武汉 430074)
在高温催化燃烧中烧结对催化剂的活性影响巨大,而火焰合成的纳米催化剂的烧结行为鲜有研究.通过火焰喷雾热解合成了以TiO2、ZrO2、SiO2为载体的一系列Cu基负载型纳米催化剂,并将所合成的纳米颗粒用于低浓度CH4催化燃烧以评价其性能.对比反应前后催化剂的BET、XRD及TEM表征,研究了不同催化剂材料在高温催化过程中晶相转变与烧结之间的竞争关系,并发现了CuO-ZrO2的表面扩散主导以及CuO-TiO2的晶界扩散主导的烧结机制.从催化燃烧测试分析发现,CuO-ZrO2在600℃对甲烷的催化转化率达到了90%,CuO-TiO2由于其抗烧结性能较差在800℃才达到88%转化率,而CuO-SiO2反应性最差,在600℃只有30%转化率.结果表明,ZrO2负载型Cu基纳米催化剂活性较高兼具抗烧结性能.
火焰喷雾热解;催化燃烧;甲烷;烧结机制;相变与烧结竞争
煤层气在煤炭生产中被称为瓦斯,是一种有害气体,低浓度的甲烷聚集具有爆炸的危险,因此常常对煤矿生产构成安全威胁.除此之外,甲烷也是一种温室气体,其温室效应潜能值是CO2的25倍[1],并且气候变化中所关注的温室效应有超过30%比例是由于甲烷排放引起的[2].高浓度甲烷的处理相对简单,而低浓度的甲烷则很难消除,因此在矿井、化工企业、污水处理厂等场所的低浓度甲烷净化消除受到有关企业的高度重视[3].
通常甲烷催化燃烧反应温度一般较高,为350~650℃[4],对于低浓度甲烷的净化处理,燃烧所产生的热量本身较少,一般不足以促使燃烧持续进行,因而外部热量的供给将成为甲烷持续净化消除的必要条件.对此,将反应维持在较低的温度下进行能够节省更多的能量输入,提高经济性,因而催化剂应具有较高的反应活性;同时高温催化燃烧过程中,为保证催化剂的使用寿命,抗烧结性能也显得极其重要.在贵金属催化剂中,Pt和Pb因其性质稳定,反应性较好,常作为负载型催化剂中的活性物质对低浓度甲烷进行催化氧化[5-8].但是贵金属储量有限、价格昂贵等客观因素限制了其大规模使用,采用廉价金属氧化物作为替代受到人们的重视.Cu基氧化物是其中的代表,其催化温度低,一般能在550~700℃时实现对低浓度甲烷的高效转化[9-11].但是Cu基氧化物的塔曼温度较低(CuO,684℃;Cu2O,823℃),在高温甲烷催化降解中,高温常常会导致催化剂因发生烧结而失活.负载型金属氧化物催化剂被认为能够抑制高温烧结,主要是氧化物在载体上具有较高分散度并且减弱了负载金属氧化物彼此之间的烧结与团聚.作为目前广泛使用的载体材料,TiO2、ZrO2以及SiO2常常通过各种方法来制备负载型铜基催化剂并对其性能进行研究.
火焰喷雾热解法能够实现一步快速合成纳米材料,在制备过程中前驱体在很短的时间内完成分解、成核、凝并、烧结、团聚以及淬火冷却等过程.相比于常规方法制备的纳米材料,火焰合成材料在高温反应过程中的烧结行为以及负载对于表面活性相的影响目前鲜有研究.已有的大量研究工作只着眼于材料抗烧结性能的比较,尚缺乏对其烧结机理的深入研究.本文采用火焰喷雾热解法制备了高负载CuO的纳米催化剂,通过一系列表征和测试,研究了不同负载的催化剂在中高温CH4催化燃烧反应中的反应性能及反应前后催化剂形貌结构的变化.进而分析了催化剂烧结可能的原因,并从制备角度指出了改进抗烧结性能的方向.
1 实验部分
1.1 催化剂的制备
纳米催化剂在商用实验室尺度的火焰喷雾热解合成器(NPS10,Tethis)上进行制备[12].不同载体的CuO纳米催化剂按照以下工艺流程进行.一定量的三水硝酸铜(分析纯,国药集团化学试剂)作为铜源,溶解于无水乙醇(分析纯,国药集团化学试剂)中.然后,将一定量的载体前驱体,加入到硝酸铜的乙醇溶液中.不同载体TiO2、ZrO2及SiO2所对应的前驱体分别为钛酸正丁酯(分析纯,国药集团化学试剂),硝酸锆(分析纯,国药集团化学试剂)和正硅酸乙酯(分析纯,国药集团化学试剂).对混合后的前驱体进行搅拌,以至充分混合.其中,载体前驱体的金属离子物质的量浓度控制在0.5mol/L.
如图1所示,前躯体溶液通过注射泵以可控的流率注入到反应器内,经过双流体雾化形成喷雾,被甲烷/氧气预混辅助火焰点燃[13].其中的前驱体溶质开始氧化、分解,并在高温火焰中解离为原子状态,然后经历成核、碰撞凝并、烧结、冷凝等生长过程形成金属氧化物颗粒气溶胶[14-15].当气溶胶到达温度较低的区域时,碰撞凝并的颗粒进一步形成团聚体,并在真空泵的辅助下通过反应器上方玻璃纤维处的过滤器进行收集[16].将附着在过滤器上的一层纳米颗粒刮取下来便获得所制备的纳米催化剂.

图1 火焰喷雾热解实验装置
在火焰合成参数设置中,支持火焰预混气由甲烷和氧气组成,流量分别为0.75L/min和1.5L/min.分散气采用氧气,流量设定为5L/min.所制备的不同载体铜基催化剂为方便表述,以20CT、20CZ及20CS分别命名20% CuO为负载,TiO2、ZrO2及SiO2为载体的铜基催化剂.催化剂中CuO的质量分数按照公式(1)进行计算:
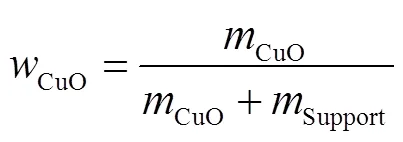
式中CuO及Support代表目标合成催化剂的氧化铜质量及载体质量.每100mL前驱体混合液的配比如表1所示.
表1 不同负载的CuO纳米催化剂的前驱体配置及火焰参数

Tab.1 Precursors configurations for CuO nano-catalysts with different supports and flame parameters
1.2 催化剂的制备
本文对新鲜样和反应后样品分别进行了表征.为加以区分,命名新鲜样为20CZ-F、20CS-F和20CT-F.反应后样品为20CZ-O、20CS-O和20CT-O.催化剂的比表面积使用美国麦克提瑞公司制造的全自动物理吸附仪(Micromeritics ASAP 2020)进行测试,为脱除样品表面的水及杂质气体,在测试之前样品将在120℃的真空干燥箱中放置24h.测试在-196℃下进行,催化剂的比表面积通过Brunauer-Emmett-Teller(BET)方法测定.催化剂的物相和晶形将通过比对标准XRD图谱进行确定,测试仪器为X射线衍射仪(RU-200B diffractometer,=0.15406nm).催化剂实际的形貌和晶体状况采用日本JEOL公司的高分辨率透射电镜(HRTEM,2100F)进行观察,采用的电子的加速电压为200kV.
1.3 催化剂的活性表征
如图2所示,在线催化燃烧评价系统用于测试样品的催化燃烧性能.其中甲烷体积分数为1.5%,空速设定为60000mL/(g·h).实验系统如图2,由配气柜、固定床反应器和气体检测器组成,混合气体的组分由3个质量流量控制器进行控制.一定量的催化剂置于石英棉上,并装填在加热炉中部的石英反应器中,其堆积厚度约为8mm.热电偶用于测量床层温度,温度控制器用于控制加热炉和反应器的温度.混合气体通过石英管上端进入反应器,经过催化剂床层后经由反应器中石英管的下端流出.气体过滤及冷凝后,使用气相微色谱(Synpec 3000B-TCD)进行组分含量的在线检测.


式中,及分别为甲烷在反应器进口端及出口端的气体体积分数.
2 结果及分析
2.1 催化剂形貌
如图3所示,经过甲烷催化性能测试,催化剂粉体的颜色发生了改变.不同载体的催化剂,其颜色变化不尽相同.其中20CT由反应前的黄褐色变为黑色,20CZ由反应前的黄褐色变为褐色,20CS由反应前的绿色变为墨绿色.
图3中为反应前后样品BET比表面积变化及其吸附脱附曲线.发现催化剂都具有滞后环,即吸附曲线和脱附曲线不一致所产生的环状结构.滞后环是由于孔隙结构的毛细冷凝造成的,因此通过对滞后环的形状来判别材料的孔隙特征.图中的滞后环属于H1型[17],此类型的纳米颗粒都具有球形结构,由于其堆积软团聚的影响才产生了以狭缝孔和堆积孔为主要形式的宏观孔隙结构,进而产生了吸附脱附等温线的分离.此外,结合反应后BET测试的结果进行判断,发现反应后的样品粉体颗粒仍保持球形结构.但是根据样品20CT和20CZ的滞后环变小以及比表面积减小的情况,表明了粉体中孔隙结构减少,高温对颗粒形貌产生了一定的影响变化.不同载体Cu基催化剂在反应前后的物性数据见表2.20CT-O的比表面积仅为20CT-F的35.5%,20CZ-O的比表面积仅为20CZ-F的55.1%.虽然两种样品粉体的比表面积在高温反应后都呈现出了下降趋势.但是二氧化钛载体的比表面积减少了新鲜样品比表面积的约三分之二,暗示其反应前后形貌变化更大.
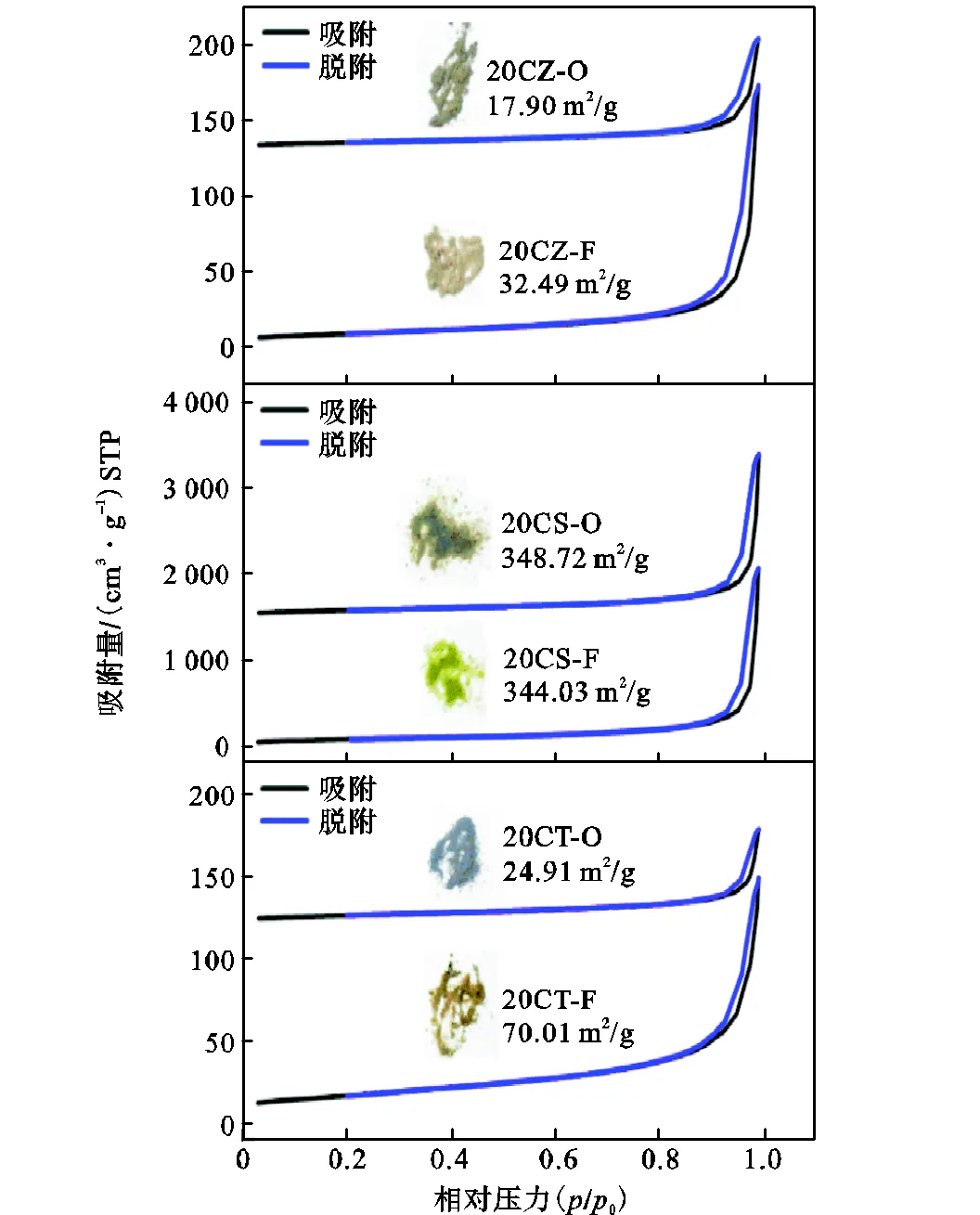
图3 Cu基催化剂反应前后的粉体形态及其氮气等温吸附脱附曲线
表2 不同载体Cu基催化剂在反应前后的物性数据
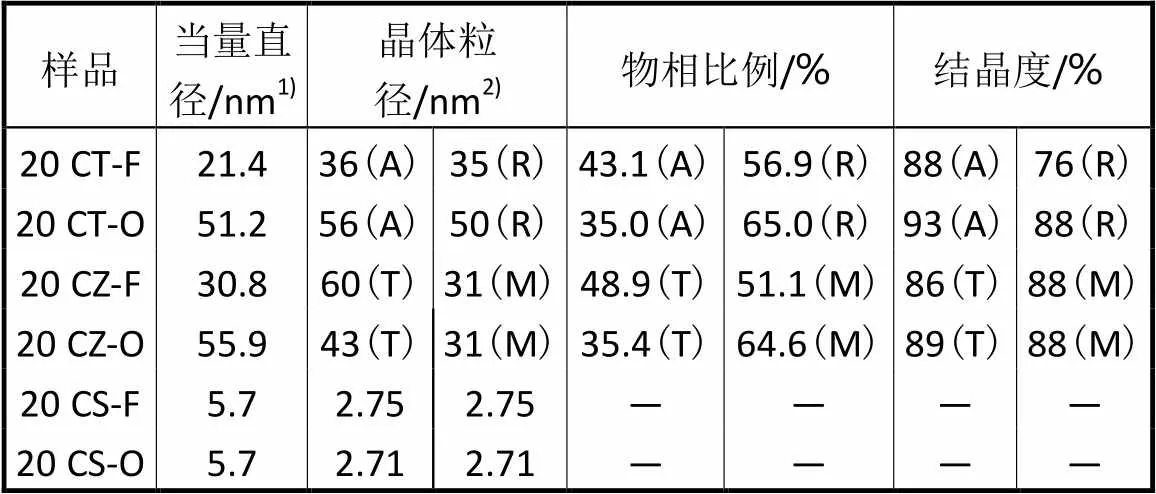
Tab.2 Physical parameters of Cu-based catalysts with different supports before and after reaction
注:1)当量直径计算公式:BET=6/(a×),其中a为BET比表面积,为样品的加权密度;2)晶体粒径由谢乐公式计算;表中,ZrO2(T—四方晶系,M—单斜晶系),TiO2(A—锐钛矿相,R—金红石相).
通常情况下,孔结构的堵塞、颗粒尺寸的增加、颗粒间的团聚都可能造成颗粒比表面积的下降.鉴于火焰喷雾热解法所制备的纳米颗粒基本为球形颗粒,颗粒内部并不存在孔隙结构,另外甲烷催化燃烧反应产物基本为二氧化碳,一般并不会引起积碳等效应和孔堵塞.根据比表面积当量直径的计算,新鲜样颗粒都呈现出较小的纳米尺寸,在反应后样品的对比中,20CT与20CZ都发生了粒径增长,其中主要原因是高温对颗粒形貌产生了影响.所以颗粒尺寸以及颗粒间团聚程度的增加可能是高温烧结引起的.分析发现,以SiO2为载体的20CS的比表面积在反应后仍和反应前比表面积相近,甚至反应后20CS-O的比表面积略高于反应前的20CS-F.类似于其他火焰合成的硅基负载的催化剂[18],20CS呈现较高的比表面积.
2.2 相变与烧结竞争分析
反应前后20CZ催化剂的X射线衍射图谱如图4所展示,ZrO2主要具有四方晶系(2=30.2°)及单斜晶系(2=28.2°),分别在图中以T和M表示.图谱4(a)中,催化剂反应前后的衍射峰发生了变化.按照以上两种晶系标准图谱相对峰强的对比可以发现,反应后单斜晶系的含量相对增加,而四方晶系的含量相对减小.
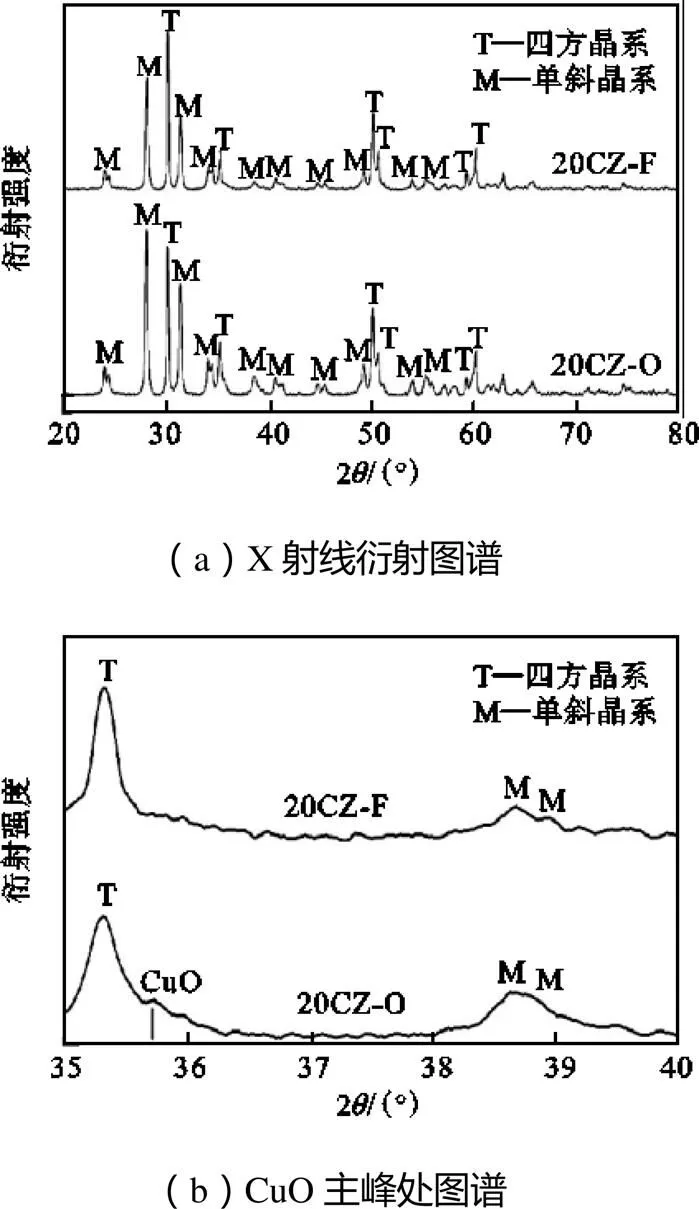
图4 反应前后CuO-ZrO2纳米催化剂的X射线衍射图谱及CuO主峰处图谱
通过表2分析发现,催化剂的结晶度在反应后只有略微提高,颗粒的结晶度处于较低的水平,是由于在高温喷雾热解过程中,颗粒中形成了较多的不定形二氧化锆.二氧化锆载体的物相组成可根据经验公式进行计算[19].从计算结果中发现四方晶系的物相比例在反应前后下降了13.5%.通过对反应前后XRD图谱的进一步对比,可以发现单斜系晶体衍射峰的峰型及峰宽并没有较大变化,而相对强度有所增加.而对于四方系晶体的衍射峰峰宽有所变大,并且相对强度有所下降.由晶体尺寸的计算结果可知,反应前后样品中的单斜晶系晶体尺寸维持在31nm左右,而四方晶系晶体的尺寸则从60nm减少了17nm,变为43nm.四方晶系晶体尺寸的减小主要是由于在ZrO2晶体上发生了晶相转变,并且此过程是发生在原有颗粒上,从而引起原有ZrO2晶体的尺寸变小[20].另外根据XRD结果发现,即使达到600℃的反应温度,ZrO2晶体仍未出现晶体生长以及明显的烧结现象,展示出良好的抗烧结特性.
对比图4(b)中CuO特征峰的区域XRD谱图,合成的新鲜纳米颗粒中并没有发现明显的CuO晶体衍射信号.说明催化剂颗粒中的氧化铜物种均以高分散或离散微晶的形式分散在ZrO2上.在600℃反应后的颗粒中,也只发现较为微弱的CuO晶体衍射信号,说明高温下20CZ中ZrO2所负载的铜物种仍保持以高分散或离散微晶的形式存在.根据实验结果可知,二氧化锆抑制了载体烧结现象的发生,另外由于良好的高温热稳定性,也抑制了所负载的铜物种之间烧结现象的发生.
反应前后20CT催化剂的XRD图谱如图5所示.新鲜样20CT-F结晶度较低,与20CZ-F类似,可能是在合成过程中生成了不定形的二氧化钛.经过高温反应后,20CT-O的结晶度均相对有所提升,锐钛矿相(2=25.3°,Anatase)的结晶度从88%提高到了93%,相对增加了5%,金红石相(2=27.4°,Rutile)的结晶度则由76%提高到了88%,相对增加了12%,两者结晶度的提升意味着高温反应环境中,不定形的金属氧化物出现了晶相生长.
如图5(a)所示,在甲烷催化反应过程中,由于高温环境,TiO2也出现了晶相转变[21],根据物相分析,反应后的20CT-O的锐钛矿相二氧化钛比例相对减小,与此相反,金红石相二氧化钛的比例相对增加.根据反应前后的晶相分析,有8.1%的锐钛矿相二氧化钛转变为了金红石相二氧化钛.
另外,20CT-O的XRD图谱中的衍射峰峰宽变窄,说明其晶体尺寸增长.晶体尺寸增加的原因有晶体生长和颗粒之间的烧结.在高温反应后,锐钛矿相二氧化钛和金红石相二氧化钛的晶体尺寸分别相对增加了56%和40%.根据之前的探讨,高温下不定形组分的晶体生长会造成颗粒晶体尺寸的增长,但20CT-F既保有较高结晶度,且反应后结晶度变化有限,因此不定形材料的重结晶难以使得晶体尺寸大幅度增长.若没有发生烧结,但发生了二氧化钛的晶相转变,这种情况下锐钛矿相与金红石相的晶体尺寸变化趋势并不相同,前者的晶体尺寸减小,后者的晶体尺寸增大,同图4中ZrO2的变化类似.然而对于反应前后20CT的对比,两种晶体的尺寸都存在大幅增长,说明高温反应过程中出现了TiO2载体的烧结.
图5(b)是CuO特征峰的区域XRD谱图,20CT-F纳米催化剂在其衍射峰图谱上并没有发现明显CuO的衍射信号,说明氧化铜物种以高分散或离散微晶的形式分散在载体TiO2上.但在经历过高温催化反应后,较为明显的CuO特征峰出现.说明颗粒上出现了团聚的CuO晶体,导致其晶体尺寸增大,因而产生较强的衍射信号,可以推断20CT催化剂中高分散CuO和离散微晶CuO在表面发生了烧结.
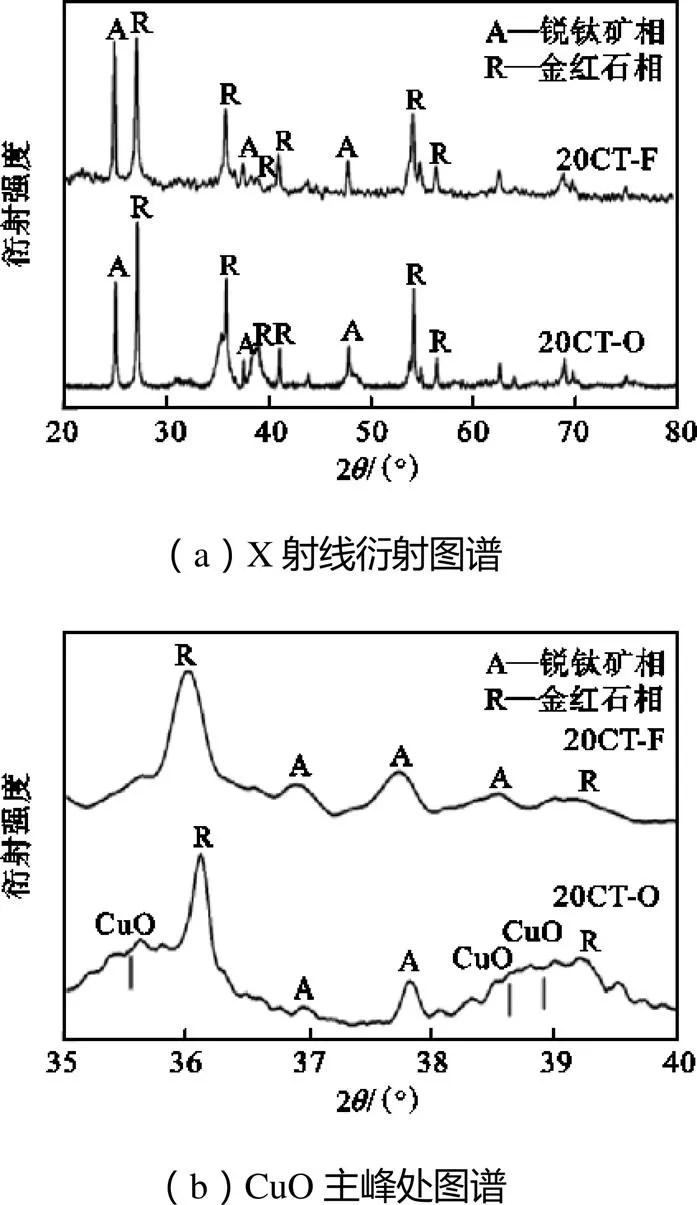
图5 反应前后CuO-TiO2纳米催化剂的X射线衍射图谱及CuO主峰处图谱
图6为20CS催化剂反应前后的XRD图谱,其中2=21.9°处较宽的衍射峰是单斜系SiO2的衍射峰.根据计算,反应前后的颗粒的晶体尺寸基本维持在2.7nm,只有BET的一半.可能是由于合成过程中形成了较多的不定形非晶态玻璃体.非晶态物质组成了20CS纳米颗粒中的主要部分,仅有一小部分SiO2形成了有序的晶体结构.
根据形貌表征结果,石英玻璃SiO2在600℃下仍具有较好的热稳定性.在甲烷高温催化反应后,20CS的比表面积甚至略有提高.比表面积的增大和晶体尺寸的减小可能由于部分不定形SiO2在高温下的晶体生长.
CuO特征峰的区域XRD谱图如图6(b)所示,反应前后20CS均未出现较强的铜物种晶体衍射信号,其中蓝色线所标出的微弱隆起可能属于不定形CuO产生的衍射信号.CuO本身与石英玻璃SiO2之间具有良好的互溶性,因此推测CuO几乎没有形成单独的晶体形态,而是大部分溶解在了载体中形成了图3中绿色粉体的硅酸铜.
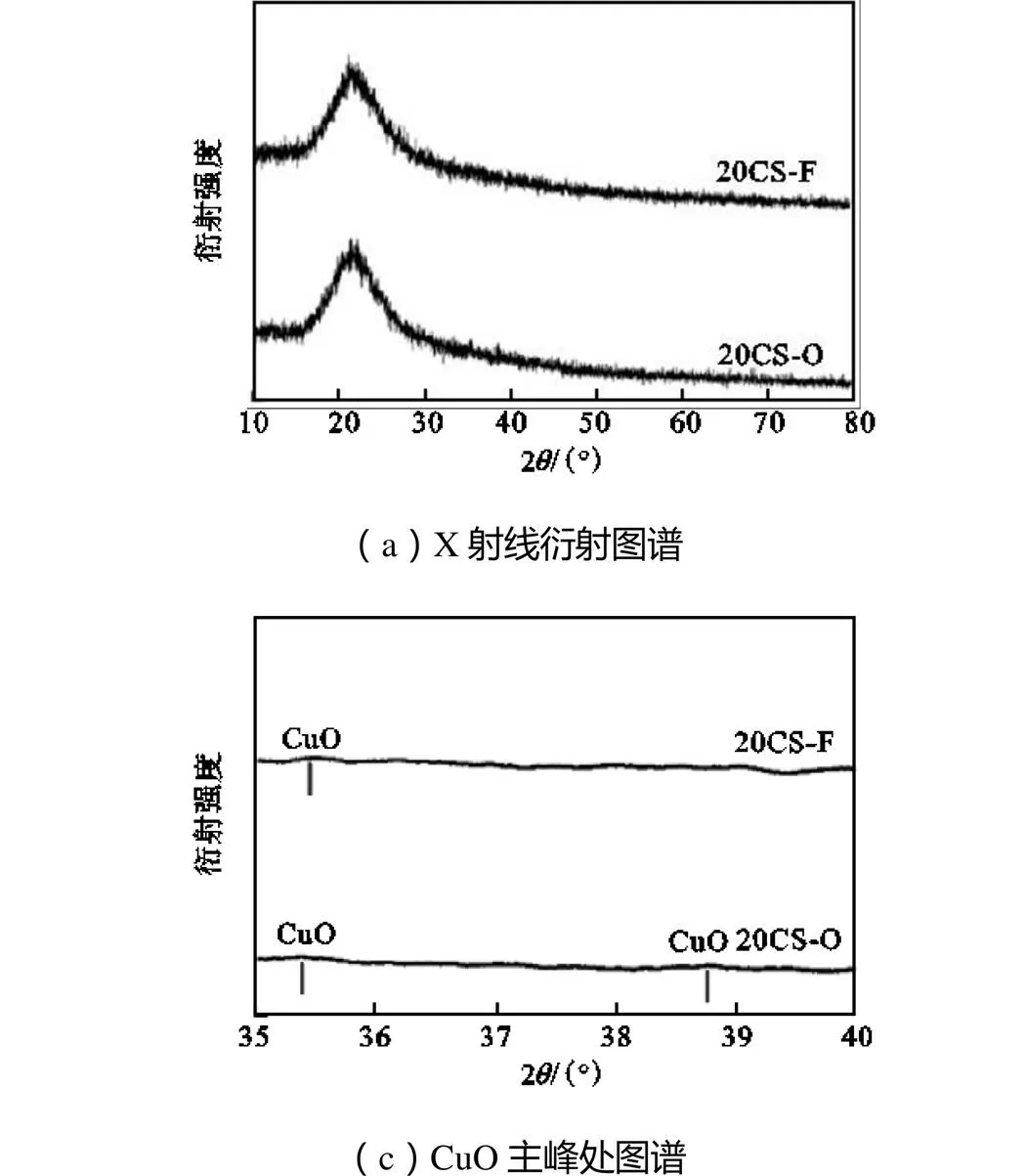
图6 反应前后CuO-SiO2纳米催化剂的X射线衍射图谱及CuO主峰处图谱
以上XRD表征表明,ZrO2在高温反应中保持了良好的抗烧结性能,晶相转变使得其晶粒尺寸减少,减弱了烧结的影响;TiO2在高温中严重烧结,晶相转变所带来的晶粒尺寸下降效应未能降低烧结的程度,在反应前后颗粒与最终的晶体尺寸大幅增加.以玻璃体为主要成分的CuO-SiO2表现出较好的热稳定性,在高温中的重新结晶过程反而增加了其比表面积.
2.3 烧结主导机制分析
图7是反应前后的20CZ高分辨透射电镜图.根据观察,20CZ-F呈现出与BET分析中一致的软团聚形式颗粒团,进一步观察颗粒形态发现,大部分的颗粒呈现为球状和条状,尺寸较为均匀,基本分布在30nm至60nm的区间内.纳米颗粒边缘表面出现了约为2nm的非晶态层,可能属于不定形的CuO及ZrO2,对应了XRD分析中20CZ结晶度较低的结果.
反应后的催化剂样品在图7(b)中可以发现其尺寸均匀性变差,表现为更多大小不均的颗粒,并且出现颗粒间的团聚,而颗粒之间的接触部分出现了不定形非晶态物质的黏连.由于两个颗粒在发生黏连过程中出现了不均匀的原子空位,这会产生应力作用促使黏结部分的原子沿晶界运动,最后突破晶界发生融合[22].但是晶体ZrO2颗粒由于其表面具有较低的表面能,未发生此种以晶界扩散为主导的融合[23].然而以表面扩散为主导的颗粒融合仍发生在非晶体颗粒与晶体颗粒之间.这主要是因为火焰喷雾热解过程中会产生具有较高表面能的不定形ZrO2,高表面能会使得表面突出部分的原子迁移,进而造成颗粒表面平缓.因此在高温反应之后,虽然纳米颗粒晶体粒径没有增大,但是其比表面积减小了.

图7 20CZ反应前后的高分辨透射电镜图
图中纳米颗粒表面的非晶态外层在反应后明显变薄,这是由于非晶态CuO及ZrO2在高温下重新结晶.在图中纳米团簇里发现了较多尺寸小于20nm的小颗粒以及一些尺寸在50nm至100nm之间的大颗粒.小颗粒的形成可能是由于四方晶系ZrO2晶体颗粒向单斜晶系ZrO2晶体的晶相转变.根据测得的晶面参数,小颗粒晶体确实基本属于单斜晶系ZrO2晶体.
与20CZ-F相同,20CZ-O中也没有直接发现CuO晶体,但根据透射电镜图谱进一步分析后,会发现疑似的CuO晶体分布在大颗粒的外层部分,说明ZrO2表面出现了铜物种的聚集.由此,在经过600℃的高温甲烷催化反应后,ZrO2展现出较好的热稳定性,对载体本身具有抗烧结的能力,并且作为载体也抑制了表面铜物种间的相互烧结.
20CT-F及20CT-O的高分辨透射电镜图如图8所示.反应前晶粒尺寸均匀的颗粒在反应后出现了较为混乱的团聚颗粒结构.与20CZ反应前后变化相类似,20CT上的非晶态层在高温反应之后基本消失,说明TiO2表面非晶态物质同样也发生了重结晶.图8(b)中,可以观察到颗粒之间存在着晶界,而高温的烧结一般会促使晶界的产生.因此在电镜图中展现出区别于新鲜20CT颗粒间的非紧密堆积聚集,而出现了颗粒烧结后形成的较大颗粒.

图8 20CT反应前后的高分辨透射电镜图
对颗粒的晶面间距进行了测量,并未发现小粒径锐钛矿相TiO2颗粒之间的烧结团聚,而烧结现象主要发生在颗粒粒径较小的金红石相TiO2上,因此可以认为在高温下小颗粒的锐钛矿相颗粒相对更稳定.在对大颗粒之间的观察中,并未发现烧结团聚,仅存在大颗粒间的非紧密接触现象.
然而一般都认为金红石相TiO2的热稳定性优于锐钛矿相TiO2.但本文中的现象在分子动力学模拟中得到了类似的结论,在Naicker等[24]相关的分子动力学模拟工作中发现,小颗粒TiO2在具有较大比表面积的时候,锐钛矿相二氧化钛比金红石相二氧化钛更加稳定.金红石相颗粒相比于锐钛矿相颗粒具有更高的表面能占比,因此具有高表面能的小颗粒金红石相TiO2更容易发生烧结.随着小颗粒间烧结团聚,其表面原子占总体颗粒原子的比例不断减小,颗粒粒径增大,其表面能占颗粒总能量的比例也会趋于平稳.此时表面能将不再诱导颗粒间烧结现象的产生,因此大颗粒之间发生烧结现象较少.除去载体的烧结现象,TiO2大颗粒周围出现了较多的CuO晶体,说明CuO晶体在TiO2表面烧结形成了富集的铜物种团簇.由此,TiO2之间在高温催化反应过程中容易出现烧结现象,并且其所负载的CuO之间也会发生烧结现象.
2.4 CH4催化燃烧结果分析
图9为不同载体负载Cu基催化剂对甲烷的催化燃烧的性能评价曲线.其中反应温度低于500℃时,20CZ具有同20CT相近且良好的催化转化能力.对于甲烷催化燃烧,常规方法制备的Cu基负载型纳米催化剂认为的其优化负载量为8%[25],若对比500℃之前的甲烷催化降解效果,火焰合成法制备的负载型催化剂的反应活性优于常规方法合成的负载型催化剂.然而在反应温度上升到700℃之后,20CT对甲烷氧化反应的转化率上升缓慢;在800℃时,其转化率仅有88%.在500℃之后,20CZ展现出明显优于20CT的反应活性,其转化率仍随温度上升而进一步提高,并且在600℃时就具有低浓度甲烷90%以上的转化能力.在600℃之后,20CZ对甲烷的转化效率上升较为缓慢,在800℃时只达到了97%的甲烷催化转化效率.

图9 纳米催化剂对甲烷的催化燃烧性能测试结果
相较于20CT与20CZ,20CS的催化反应性能相对较差,较高的起始反应温度及其缓慢的转化率上升速率都说明其整体反应活性较差.但当温度高于700℃之后,20CS的催化转化率却超过了在低温段活性较好的20CT,这主要归功于石英玻璃SiO2高温下较好的热稳定性,避免了所负载的CuO烧结.
为探究不同Cu基载体高温下烧结的影响,催化剂性能测试采用升温及降温的两个过程进行评价.由于CuO在达到700℃之后会开始分解为Cu2O[26],故将性能评价的上限温度设定为600℃,一般低浓度甲烷催化燃烧在此温度下的铜基催化剂也具有较高的转化能力[27].根据图10中的测试结果,对比升温降温过程中性能曲线,发现所合成的铜基催化剂在600℃之后的降温过程中均出现了一定程度的活性衰减.其中以TiO2为载体的催化活性衰减最大.在500℃这一温度点时,催化转化率在升温过程中达到了75%,而到降温过程中转化率却只有49%. 20CZ和20CS虽然也存在一定的反应性下降,但同20CT相比下降幅度较小.

图10 纳米催化剂对甲烷催化燃烧的升温和降温测试结果
结合之前催化剂的形貌表征结果,可以发现热烧结对催化剂反应性能产生了较为明显的影响.在高温反应区段内,TiO2及ZrO2为载体的Cu基催化剂中会发生不同程度的晶相转变,新鲜样催化剂经过高温反应后其形貌与原来的物相组成发生了巨大变化.由晶相转变造成的颗粒不均匀及晶体结构混乱将致使颗粒中活性位点减少.另外甲烷高温反应中表面的高分散CuO将会发生烧结形成CuO团簇,而所形成的CuO团聚体的催化活性一般较差,相当于进一步减少了活性位点的数量.此外烧结及颗粒团聚将造成比表面积的减少,因而甲烷的反应区域会严重缩减.根据实验的结果来看,负载型催化剂的载体确实能够有效减缓和削弱烧结现象的发生,就本实验中ZrO2较好的抗烧结性能保持了所负载CuO晶体的形貌,并且维持了较高的反应活性,使其即使存在颗粒间黏结团聚的情况下仍能具有较高的甲烷转化效率.
对于火焰合成的纳米材料,由于在制备过程中在颗粒内部极易形成高浓度的固溶体,而固溶体中的离子对于晶体的晶相转变起着重要作用.对于不同的催化反应,晶向转变对反应的促进和抑制也是不同的,这要求选择合适的活性相负载量来控制固溶体浓度来控制晶向转变的过程.此外,火焰合成的纳米材料一般具有较高的表面能,在低温反应中,高表面能能提高反应活性,而在高温反应中,高的表面能会诱导烧结,因此适当控制火焰参数(如降低火焰温度,减小火焰速度等)来降低最终合成材料的表面能也有重要意义.
3 结 论
(1) ZrO2颗粒之间会发生一定程度烧结,其主要形式为颗粒之间表面的不定形非晶态层粘连.这主要是由于ZrO2具有相对较低的表面能,从而致使颗粒晶体间的烧结融合现象较少.
(2) 根据表征测试结果发现,由于 ZrO2具有较低表面能,不仅抑制了ZrO2颗粒之间的烧结,同时还抑制了表面负载CuO的烧结.使得CuO能够稳定负载于ZrO2表面上.TiO2高温热稳定性较差,载体之间出现了明显的烧结现象,并且其表面出现了CuO大晶体聚集,表明颗粒表面上的铜物种也发生了烧结团聚现象.
(3) 高温反应过程中纳米催化剂的晶相转变和烧结影响了催化剂的形貌和结构,进而影响了催化剂的性能.从火焰合成的源头参数出发对这些影响因素进行控制,有利于催化剂性能的改进.
[1] Setiawan A,Kennedy E M,Stockenhuber M. Development of combustion technology for methane emitted from coal-mine ventilation air systems[J].,2017,5:521-538.
[2] Moss A.:[M]. UK:Chalcombe Publications,1993.
[3] Lashof D,Ahuja D. Relative contributions of greenhouse gas emissions to global warming[J].,1990,344(6266):529-531.
[4] Ji Y,Yanbing G. Nanostructured perovskite oxides as promising substitutes of noble metals catalysts for catalytic combustion of methane[J].,2018,29:252-260.
[5] Cargnello M,Delgado Jaen,Hernandez Garrido,et al. Exceptional activity for methane combustion over modular Pd@CeO2subunits on functionalized Al2O3[J].,2012,337(6095):713-717.
[6] Deutschmann O,Maier L,Riedel U,et al. Hydrogen assisted catalytic combustion of methane on platinum[J].,2000,59(1-2):141-150.
[7] Colussi S,Gayen A,Farnesi C M,et al. Nanofaceted Pd/O sites in Pd/Ce surface superstructures:Enhanced activity in catalytic combustion of methane[J].,2009,48(45):8481-8484.
[8] Widjaja H,Sekizawa K,Eguchi K,et al. Oxidation of methane over Pd/mixed oxides for catalytic combustion [J].,1999,47(1/2/3/4):95-101.
[9] Artizzu P,Garbowski E,Primet M,et al. Catalytic combustion of methane on aluminate-supported copper oxide [J].,1999,47(1/2/3/4):83-93.
[10] Hu W,Lan J,Guo Y,et al. Origin of efficient catalytic combustion of methane over Co3O4(110):Active low-coordination lattice oxygen and cooperation of multiple active sites[J].,2016,6(8):5508-5519.
[11] Geng H,Yang Z,Zhang L,et al. Effects of O2/CH4ratio on methane catalytic combustion over Cu/g-Al2O3particles[J].,2016,41(40):18282-18290.
[12] Bettini L G,Dozzi,M V,Foglia F D,et al. Mixed-phase nanocrystalline TiO2photocatalysts produced by flame spray pyrolysis[J].,2015,178:226-232.
[13] Koirala R,Pratsinis S E,Baiker A. Synthesis of cata-lytic materials in flames opportunities and challenges[J].2016,45:3053-3068.
[14] Li S,Ren Y,Biswas P,et al. Flame aerosol synthesis of nanostructured materials and functional devices:Processing,modeling,and diagnostics[J].,2016,55:1-59.
[15] Kelesidis G A,Goudeli E,Pratsinis S E. Flame synthesis of functional nanostructured materials and devices:Surface growth and aggregation[J].,2017,36(1):29-50.
[16] Mädler L,Kammler H,Mueller R,et al. Controlled synthesis of nanostructured particles by flame spray pyrolysis[J].,2002,33(2):369-389.
[17] Sing K S W. Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity(Recommendations 1984)[J].,1982,54(11):2201-2218.
[18] Rittler A,Deng L,Wlokas I,et al. Large eddy simulations of nanoparticle synthesis from flame spray pyrolysis[J].,2017,36(1):1077-1087.
[19] Toraya H,Yoshimura M,Somiya S. Calibration curve for quantitative analysis of the monoclinic tetragonal ZrO2system by X‐ray diffraction[J].,1984,67(6):C-119-C-121.
[20] Hanaor D A H,Sorrell C C. Review of the anatase to rutile phase transformation[J].,2011,46(4):855-874.
[21] Shannon R D,Pask J A. Kinetics of the anatase rutile transformation[J].,1965,48(8):391-398.
[22] 桂进发,张永亮,赵海波. CuO与负载间相互作用的密度泛函理论[J]. 燃烧科学与技术,2017,23(2):173-179.
Gui Jinfa,Zhang Yongliang,Zhao Haibo. Density funtional theory calculation for CuO-support interactions in Cu-based oxygen carriers[J].,2017,23(2):173-179(in Chinese).
[23] Zhao H,Zhang Y,Wei Y,et al. Understanding CuO-support interaction in Cu-based oxygen carriers at a microcosmic level[J].,2017,36(3):4069-4077.
[24] Naicker P K,Cummings P T,Zhang H,et al. Characterization of titanium dioxide nanoparticles using molecular dynamics simulations[J].,2005,109(32):15243-15249.
[25] Xu B,Dong L,Chen Y. Influence of CuO loading on dispersion and reduction behavior of CuO/TiO2(anatase) system[J].,1998,94(13):1905-1909.
[26] Wang P,Means N,Howard B H,et al. The reactivity of CuO oxygen carrier and coal in chemical-looping with oxygen uncoupled (CLOU) and in-situ gasification chemical-looping combustion(iG-CLC)[J].,2018,217(1):642-649.
[27] Gonzalo A,Francisco G,Joaquin C,et al. Effect of copper species and the presence of reaction products on the activity of methane oxidation on supported CuO catalysts[J].:,2008,77(3):325-338.
Sintering Behaviors of Cu-Based Catalysts via Flame Spray Pyrolysis in Methane Catalytic Combustion
Meng Lingquan1, 2,Chen Xin1,Xu Zuwei1,Zhao Haibo1
(1. State Key Laboratory of Coal Combustion,Huazhong University of Science and Technology,Wuhan 430074,China;2. China-EU Institute for Clean and Renewable Energy,Huazhong University ofScience and Technology,Wuhan 430074,China)
The activity of catalysts is substantially influenced by their sintering behaviors during the high temperature catalytic combustion. However,few studies have focused on the sintering behaviors of nano-catalysts prepared by flame synthesis. In this paper,Cu-based catalysts with supports of TiO2,ZrO2and SiO2were synthesized via flame spray pyrolysis(FSP),which were further applied to the catalytic combustion experiment of low-concentration CH4. The characterizations by BET,XRD and TEM were also compared before and after the reaction to study the competition between the transformation of crystal-phase and particle sintering in different catalysts during the high-temperature catalysis. The sintering mechanism was revealed,in which CuO-ZrO2was dominated by surface diffusion while CuO-TiO2by crystal diffusion. The activity test showed that CuO-ZrO2obtained 90% CH4conversion at 600℃. Due to the deficiency of anti-sintering,CuO-TiO2reached 88% conversion at 800℃. The CH4conversion of 30% was achieved at 600℃ by inactive CuO-SiO2. Results showed that the ZrO2-supported Cu-based nano-catalysts demonstrated both good anti-sintering performance and higher activity for the CH4catalytic combustion.
flame spray pyrolysis(FSP);catalytic combustion;methane;sintering mechanism;competition between phase transformation and sintering
TK16
A
1006-8740(2019)05-0414-09
10.11715/rskxjs.R201901017
2019-01-17.
国家自然科学基金资助项目(51606079).
孟令泉(1993—),男,硕士研究生,lq-meng@outlook.com.
赵海波,男,博士,教授,klinsmannzhb@163.com.

