磁性吸附剂MZFS吸附偶氮染料中性红的性能及机理
曾红杰,余 静,王盈盈
磁性吸附剂MZFS吸附偶氮染料中性红的性能及机理
曾红杰,余 静*,王盈盈
(成都信息工程大学资源环境学院,四川 成都 610225)
利用正硅酸乙酯水解制备得到"核-壳"结构的磁性吸附剂MZF@SiO2(MZFS),采用X射线衍射(XRD)、透射电子显微镜(TEM)、振动样品磁强计(VSM)和傅利叶变换红外光谱(FT-IR)对MZFS的结构和性能进行表征,并研究MZFS对偶氮染料中性红(NR)的吸附性能.结果表明,拟二级动力学和Freundlich模型均能较好地描述该吸附过程,吸附过程的速率控制步骤为化学吸附;吸附自由能为0.472-0.773kJ/mol,D为-20~0kJ/mol,D为37.5kJ/mol,表明该过程是以物理吸附为主的自发吸热过程.FT-IR结果表明吸附的主要作用力为分子间氢键,MZFS可采用15%wt H2O2进行原位再生.研究结果能为偶氮染料废水处理方法的革新提供基础理论数据.
吸附;纳米复合材料;偶氮染料;磁分离;再生
偶氮染料废水是公认的难处理废水,其可生化率低,对人类和动植物危害大[1–4],常见的处理方法有物理法[5–7],高级氧化法[8–11],生物法[12–13],以及各种组合处理技术[14–16].吸附法被广泛用于染料废水处理中,常用的吸附剂有以活性炭为代表的碳材料吸附剂[17–19],利用生物材料或农产品废弃物制备的吸附剂[20–22],天然矿土材料[23–25],金属氧化物[26–28]等,而吸附剂的固液分离性能及再生循环使用性能是吸附法的瓶颈所在.因此,环境吸附材料的一个重要研究方向是开发易于固液分离、具有吸附-降解功能的新型吸附剂.
为改善吸附剂的固液分离性能,磁性纳米粒子(MNPs)逐渐用于吸附剂研究[29–32],由于MNPs独特的磁性特性、易于回收等优点,磁性吸附剂被人们关注[33–35].但MNPs因高表面能量而易团聚,比表面积较低,其在溶液中的分散稳定性较差[37],将MNPs进行表面改性制备的磁性纳米复合材料(MNCs)可提高MNPs的比表面积、改善其稳定性和分散性,目前对MNPs表面改性的方法主要是在其表面包裹修饰聚合物[38]、表面活性剂[39]、贵金属[40]和无机氧化物[41]等,常用的MNPs有Fe2O3和Fe3O4,其中Fe3O4中的Fe2+很容易失去一个电子变成Fe3+,导致MNPs磁性能降低,影响固液分离性能,不利于循环利用.而锰锌铁氧体Mn1-xZnFe2O4(MZF)MNPs用锰、锌取代易氧化的Fe2+,具有更好的抗氧化性,可极大提高材料的磁稳定性[42],当为0.4(Mn0.6Zn0.4Fe2O4)时, MZF MNPs的饱和磁化强度最大[43],有利于磁分离. 实验室前期已制备得到具有尖晶石结构的Mn0.6Zn0.4Fe2O4MNPs,利用正硅酸乙酯水解得到SiO2包覆的具有“核-壳”结构的MZF@SiO2(MZFS). MZFS具有较大的比表面积,因具有磁性而易于固液分离,磁核MZF中的Mn和Fe均具有非均相类Fenton催化活性[36],故MZFS是一种集磁分离、吸附与降解功能于一体的新型多功能纳米复合材料.
偶氮染料中性红(NR, C15H17ClN4)废水具有色泽深,水质复杂,难处理等特点[44].本文以NR作为目标污染物,研究了MZFS对NR的吸附性能和吸附机理,考察了MZFS的稳定性与循环使用性能,希望能为磁性纳米复合物吸附剂的应用以及偶氮染料废水处理方法的革新提供基础理论数据.
1 材料与方法
1.1 试剂与仪器
试剂:自制Mn0.6Zn0.4Fe2O4(MZF),正硅酸乙酯(TEOS,SiO2质量分数为28%);过氧化氢(H2O2质量分数为30%);中性红、柠檬酸等均为分析纯(成都市科龙化工试剂厂).
仪器:DX-2700X射线衍射仪(中国辽宁丹东方圆仪器厂);JSM-7500F型扫描电子显微镜(日本电子株式会社);GENESIS型能谱仪(美国EDAX公司); JEM-2100F型高分辨率透射电子显微镜(日本电子株式会社); SSA-4220型孔隙比表面分析仪(北京彼奥德电子技术有限公司);BHV-525型振动样品磁强计(日本理研电子公司);UV-2250型紫外-可见分光光度计(日本岛津公司);THZ-82型回转式气浴恒温振荡器(江苏正基仪器有限公司);Nicolet IS50型傅立叶红外光谱仪(美国Thermo Scientific公司);GGX-6型火焰原子吸收(北京科创海光仪器有限公司).
1.2 实验方法
1.2.1 MZFS的制备 将自制MZF与一定浓度的柠檬酸溶液在水浴锅中混合搅拌,调节pH值为5.50,搅拌180min后,加入一定量的氨水调节溶液pH值至10.00,逐滴加入TEOS,继续水浴加热搅拌12h.反应完成后,静置冷却,移去上清液,用无水乙醇和蒸馏水对下层沉淀物进行抽滤洗涤至中性,然后置于真空干燥箱内60℃条件下干燥120min,制得SiO2包覆的"核-壳"结构磁性纳米复合物MZFS.
1.2.2 吸附实验 将0.5g MZFS加入50mL一定初始浓度的NR溶液(pH值为5.00)中,转速200r/min,在30℃的恒温振荡器中进行吸附,30min后取出锥形瓶,磁分离后取上清液用紫外-可见光分光光度计在530nm处测定溶液中NR的浓度,NR的去除率与吸附量计算如下:
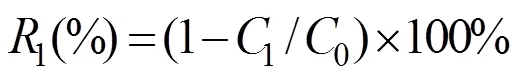

式中:1为NR的去除率,%;1为吸附后NR浓度, mg/g;0为初始NR浓度,mg/g;为MZFS吸附NR的量,mg/g;为NR溶液的体积,L;为MZFS质量,g.
1.2.3 MZFS再生循环实验 新鲜MZFS(orig- MZFS)吸附NR后,加入一定量15%wt H2O2,再加入一定量蒸馏水至一定体积,放入恒温振荡器中,温度为303K,转速为200r/min,进行吸附剂再生,再生300min后,磁分离,用去离子水洗涤MZFS至水相呈中性后烘干,得到再生的MZFS(re-MZFS), 然后再次进行吸附,如此循环6次,MZFS的再生率计算如下:
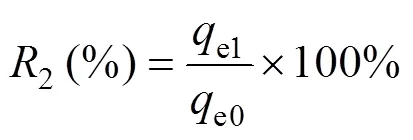
式中:2为MZFS的再生率,%;e1为re-MZFS对NR的平衡吸附量,mg/g;e0为orig-MZFS对NR的平衡吸附量,mg/g.
2 结果与讨论
2.1 MZFS的表征
由图1(a)可知,MZFS中磁核MZF各衍射峰的位置与Mn0.6Zn0.4Fe2O4的标准卡片(JCPDS74- 2401)相比整体略有偏移,表明MZFS中的磁核是具有尖晶石结构的混合晶体,可能在MZF制备过程中生成了其他具有尖晶石结构的铁氧化物.未发现晶体SiO2特征峰存在,说明SiO2以无定型的形态存在.
由图1(b)可见,MZFS为不规则球体;从图1(c)得到O、Si、Mn、Zn和Fe元素质量百分含量分别为33.96%、20.79%、6.19%、32.49%和6.57%.图1(d)中颜色较深部分为MZF,外部颜色较浅部分为SiO2包覆层,MZF被SiO2包覆层完全包裹住,硅包覆层具有丰富的孔结构.
根据IUPAC分类,MZFS的N2吸附-脱附曲线[图1(e)]属于Ⅳ型.在脱附过程中,相对压力为0.4~ 0.7区域出现了吸附滞后环,这是由于毛细管凝聚所造成的,是介孔材料的典型吸附行为,这说明MZFS具有介孔结构;滞后环的形状为H2型,表明MZFS孔结构复杂,可能包括典型的"墨水瓶"孔、孔径分布不均的管形孔和多孔吸附质或均匀粒子堆积孔.由图1(f)MZFS的BJH孔径分布图可知,MZFS最可几孔径为2.0nm;利用BET测得MZFS的比表面积和孔容分别是241.5m2/g和0.3566cm3/g.

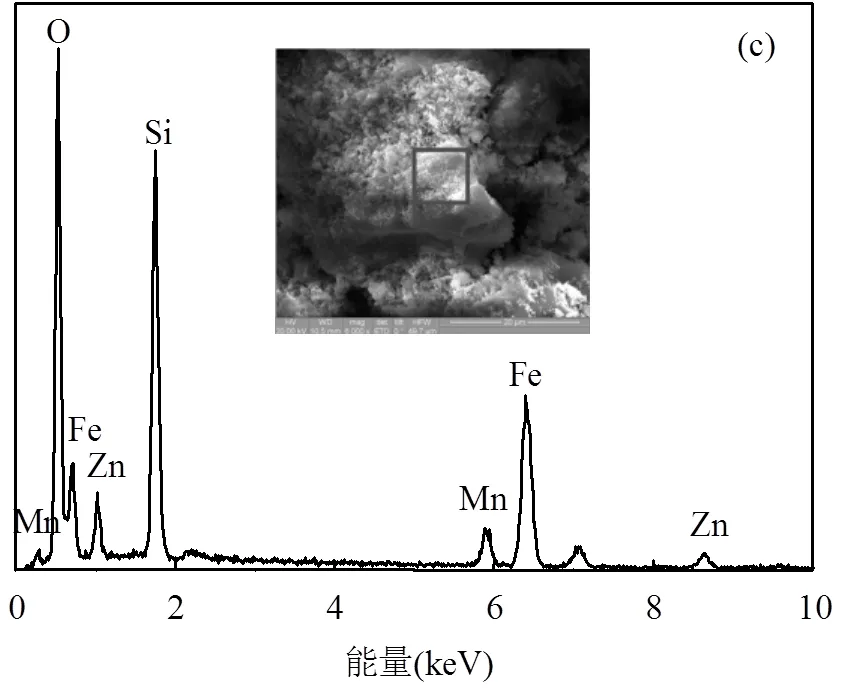
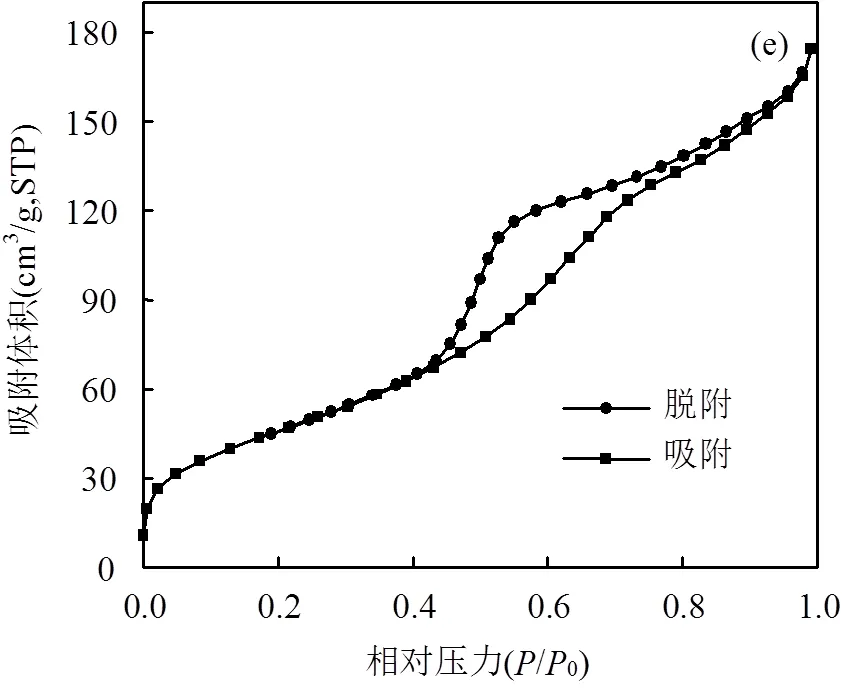
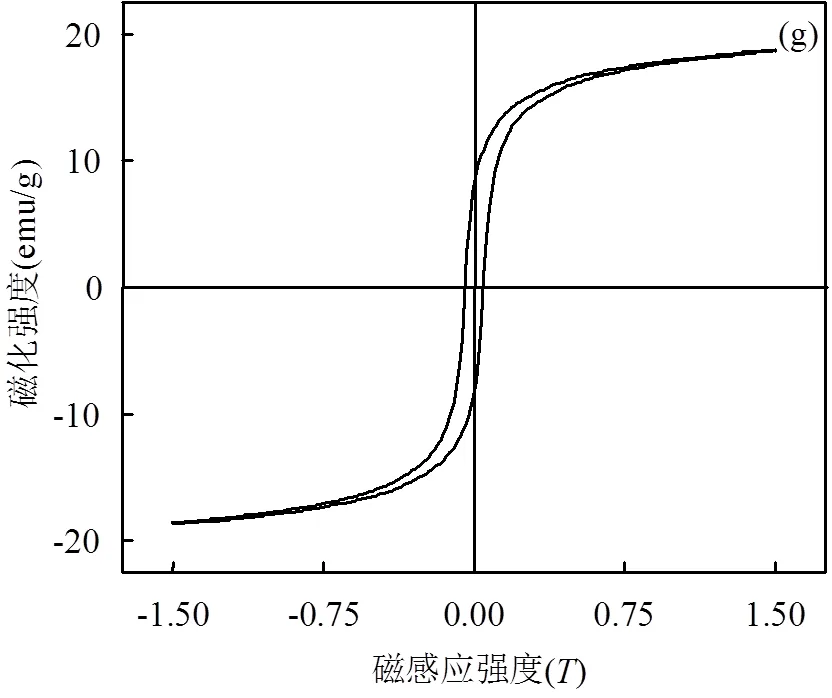
图1 MZFS的表征分析
(a) XRD谱图;(b) SEM照片;(c) EDS图;(d) TEM照片;(e) N2等温吸附-脱附曲线;(f) BJH孔径分布图;(g) 磁滞回线;(h) 磁分离效果
图1(g)为MZFS的磁滞回线,MZFS的饱和磁化强度(Ms)为18.6emu/g,剩磁(Mr)和矫顽力(Hc)分别为8.38emu/g和0.044T,较低的Mr和Hc可保证MZFS在多次使用后,仍具有较好的分散性和磁分离效果[45].实验中MZFS能在3min内实现固液分离[图1(h)],再次使用时只需轻微震荡即可分散.
2.2 吸附动力学
由图2(a)可见,MZFS吸附NR在起始几分钟内速率较高,此后吸附速率随吸附时间的延长而减缓,约60min后达到吸附平衡;将动力学数据分别采用拟一级(式(4)),拟二级(式(5)),Elovich(式(6))动力学方程和颗粒内扩散方程(式(7))进行非线性拟合[46–47],拟合结果见表1,表2和图2.
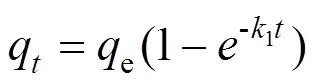
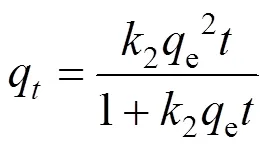
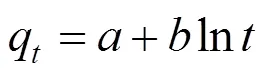
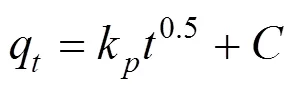
式中:q为t时刻吸附量,mg/g;e,平衡吸附量,mg/g;1为拟一级吸附速率常数,min-1;2为拟二级吸附速率常数,mg/(g·min);为初始速度,mg/(g·min);为Elovich模型的解吸常数,g/mg;k为颗粒内扩散速率常数,mg/(g·min);值的大小反映了边界层厚度.
由表1可知,拟二级动力学模型比拟一级动力学模型的复相关系数2大,且通过模型拟合得到的平衡吸附量e,cal更接近实验所得平衡吸附量e,exp,故拟二级动力学模型能更好地描述MZFS对NR的吸附过程.这是由于拟二级动力学模型包括了外部液膜扩散、表面吸附和颗粒内部扩散等吸附过程[48],故能更真实全面地反映NR在MZFS上的吸附过程;同时也表明该吸附过程中化学吸附为速率控制步骤[49].而Elovich模型(式(6))可以较好地描述化学吸附的变化规律,用Elovich模型对动力学数据进行拟合,由表2拟合结果可知,解吸常数随温度增加而逐渐变小,表明该吸附过程中的速控步骤化学吸附为吸热过程.
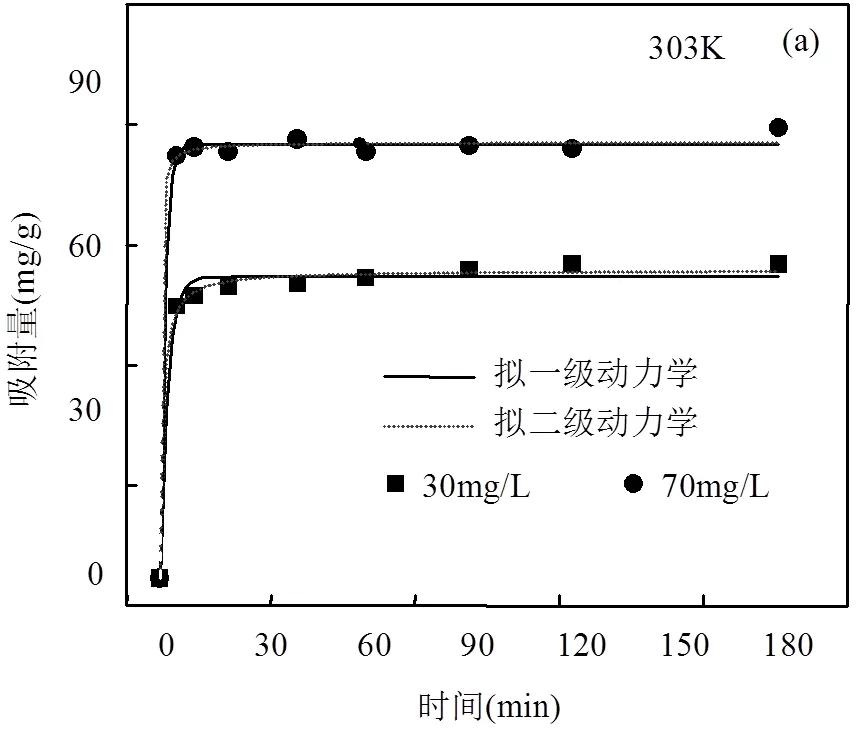
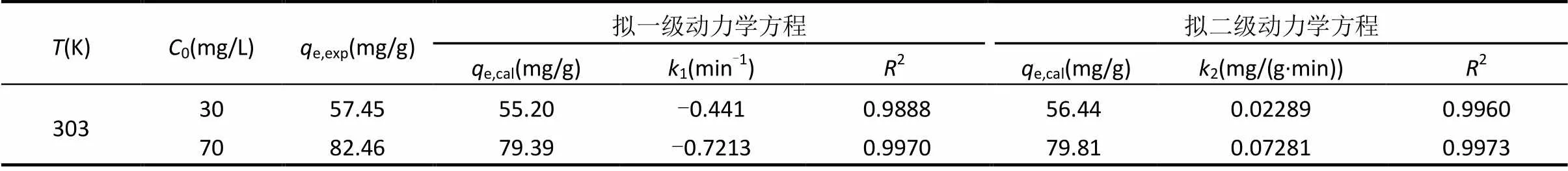
表1 MZFS吸附NR的不同动力学模型拟合参数
根据颗粒内扩散模型(式(7))的假设,如果q对0.5作图得到的曲线是线性的,且该直线通过原点,那么颗粒内扩散作用是控制整个吸附过程速率的唯一因素,由图2(b)可见,颗粒内扩散过程并不是吸附速率的控制步骤.吸附的最初阶段是由颗粒内扩散控制吸附速率.随着吸附过程的进行,溶液中NR浓度逐渐降低,吸附剂外表面的活性位点逐渐达到饱和,NR进入吸附剂颗粒内部而吸附,导致吸附阻力增大,因此颗粒内扩散速率减慢,吸附速率减慢.
根据上述动力学拟合结果可知,吸附的最初阶段是由颗粒内扩散控制吸附速率,该吸附过程的速控步骤为吸热的化学吸附,与MZFS中孔-微孔结构并存、且呈现孔口径小、孔腹大的“墨水瓶”状孔隙结构特点有关[50],可能是由于NR杂环上的N和支链氨基上的N均有可能与MZFS表面存在大量的羟基形成氢键所致.
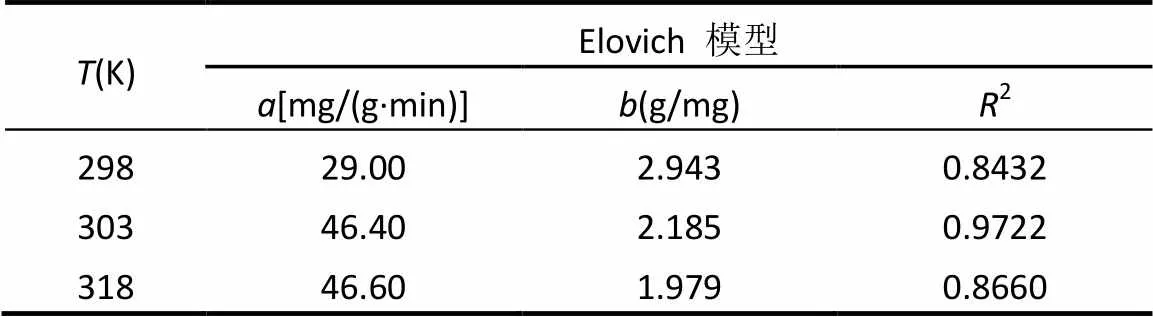
表2 MZFS吸附NR的Elovich模型拟合参数
2.3 吸附等温线与热力学
采用Langmuir[式(8)][51]、Freundlich[式(9)][52]和Dubinin-Radushkevich(D-R)模型[式(10)][53]对298,303,308,313,318K下MZFS吸附NR的平衡数据进行非线性拟合,拟合结果如图3和表3所示.