几种动物生鲜肌肉组织样品DNA提取方法的比较研究
纪 艺,姜媛媛,汪小福,徐晓丽,徐俊锋,李玥莹,陈笑芸,*
(1.沈阳师范大学 生命科学学院,辽宁 沈阳 110034; 2.浙江省农业科学院 农产品质量标准研究所,省部共建农产品质量安全国家重点实验室(筹),浙江 杭州 310021)
肉和肉制品是人类生活的重要营养来源。近年来,随着食品工业的迅猛发展,在经济利益的驱使下,国内外一些不法分子为牟取暴利,肉制品掺假屡禁不止,引发人们对食品安全的恐慌[1-7]。因此,开展食品掺假鉴定是保证食品安全的重要措施。以检测DNA为基础的实时荧光定量PCR技术具有特异性强、灵敏度高、可定量和自动化程度高等优点[8-9],已被广泛用来鉴定食品中的动物源性成分[10-13]。从动物肌肉组织中提取高质量的DNA,是开展肉制品掺假检测和监测工作的前提与基础。
目前用于提取动物肌肉组织DNA的方法有很多,主要包括改良CTAB法、SDS法、异硫氰酸胍法、PVP法及以上述方法为基础的试剂盒法[14-28]。本研究对改良CTAB法和常见商品化试剂盒进行比较分析,为日常肉制品掺假检测提供方法依据。
1 材料与方法
1.1 检测对象
生鲜牛肉、羊肉、猪肉、鸡肉和鸭肉,购自浙江省农业科学院畜牧兽医研究所。
1.2 主要试剂
CTAB裂解液配方为:1%十六烷基三甲基溴化铵(CTAB),50 mmol·L-1Tris/HCl(pH 8.0),0.7 mol·L-1NaCl,10 mmol·L-1EDTA(pH 8.0);TE缓冲液(pH 8.0)配方为:10 mmol·L-1Tris/HCl(pH 8.0),1 mmol·L-1EDTA(pH 8.0);饱和酚:氯仿:异戊醇体积比为25∶24∶1;异丙醇;70%乙醇。Premix Ex Taq(Probe qPCR)预混液购自日本TaKaRa公司,引物和探针由杭州尚亚赛生物科技有限公司合成。
1.3 主要仪器
NanoDrop 2000核酸蛋白测定仪购自美国Thermo公司,CFX96荧光定量PCR仪和QX200型数字PCR仪购自美国Bio-rad公司,DYCP-31C型核酸电泳仪购自北京六一生物科技有限公司,ZF-258全自动凝胶成像分析系统购自上海嘉鹏科技有限公司。
1.4 试验方法
1.4.1 样品处理和DNA提取
按照试剂盒说明书或方法要求称取一定量的样品,用无菌手术刀将试验材料切成小块,先在液氮中将样品迅速冷冻并研磨成粉末备用。采用改良CTAB法及目前国内外使用较广泛的7个动物组织DNA提取试剂盒分别对5个常见动物肌肉组织样品进行DNA提取,每个动物样品设置3个平行重复。
改良CTAB法参考文献[28]进行,称取50 mg样品于2 mL离心管中磨碎,加入600 μL CTAB裂解液充分振荡混匀,加入等体积的饱和酚-氯仿-异戊醇混合液,充分振荡30 s,12 000 r·min-1离心3 min后取上清液,加0.8倍体积的异丙醇,轻轻摇动30 s,12 000 r·min-1离心4 min后取沉淀,加入500 μL 70%乙醇清洗1次,常温干燥10~20 min后加入100 μL TE溶液(pH 8.0)溶解,-20 ℃保存备用。
试剂盒检测共选取7款商品化动物组织DNA提取试剂盒,其中国外品牌3个(代号为F1~F3),4个国内品牌(代号为D1~D4)。其中,D1、F1~F3的原理为蛋白酶K法,D2和D3的原理为SDS法,D4是DNA快速萃取法,即从组织中快速分离但不提纯DNA,并可立即用于荧光定量PCR反应。称取不同试剂盒所需的动物肌肉组织粉末并置于2 mL离心管中,具体操作详见试剂盒说明书。
1.4.2 DNA质量和浓度测定
取1 μL DNA样品溶液,用NanoDrop 2000进行DNA浓度、纯度和盐残留等指标的检测。
1.4.3 DNA完整性检测
配制1%琼脂糖凝胶,吸取5 μL提取的鸭DNA样品溶液与上样缓冲液混匀后加入上样孔,120 V电泳20 min后在凝胶成像分析系统拍照留存。
1.4.4 DNA提取物对实时荧光定量PCR的抑制作用
由于目前市面上常用廉价的鸭肉作为肉制品掺假物,本试验围绕8种提取方法提取的鸭肌肉组织DNA,检测其是否会抑制PCR反应。以鸭肌肉组织DNA为模板,利用TaqMan探针法实时荧光定量PCR体系来检测不同的DNA提取物是否会抑制鸭IL-2核基因的PCR扩增。参考文献[29]合成引物和探针序列,核基因引物序列上游序列为5′-GGAGCACCTCTATCAGAGAAAGACA-3′,下游序列为5′-GTGTGTAGAGCTCAAGATCAATCCC-3′,探针序列为FAM-TGGGAACAAGCATGAATGTAAGTGGATGGT-BHQ1。将鸭肌肉组织DNA稀释至同一浓度后作为模板,再进行TaqMan法进行实时荧光定量PCR。PCR反应体系为:DNA模板2 μL,2×TaqMan反应液12.5 μL,10 μmol·L-1的上下游引物各2 μL,10μmol·L-1探针0.5 μL,ddH2O补足到25μL。PCR反应程序为:95 ℃预变性5 min; 95 ℃变性10 s,58 ℃退火延伸32 s,共40个循环。通过Ct值的变化来探讨不同方法提取的DNA溶液是否会抑制PCR反应。
2 结果与分析
2.1 不同提取方法对生鲜肌肉组织样品DNA完整性的影响
PCR扩增对模板DNA的质量要求较高。用1%琼脂糖凝胶上电泳检测核酸提取质量(图1),改良CTAB法、3个国外品牌(F1~F3)、3个国内品牌(D1~D3)均可提纯得到条带相对单一、高分子量的肌肉组织DNA条带。与改良CTAB法和F1相比,其他试剂盒法提取的DNA条带更亮,表明提取的DNA浓度更高。而DNA快速萃取法(D4)提取的DNA无清晰条带,表明在DNA提取过程中已发生较大程度的降解。
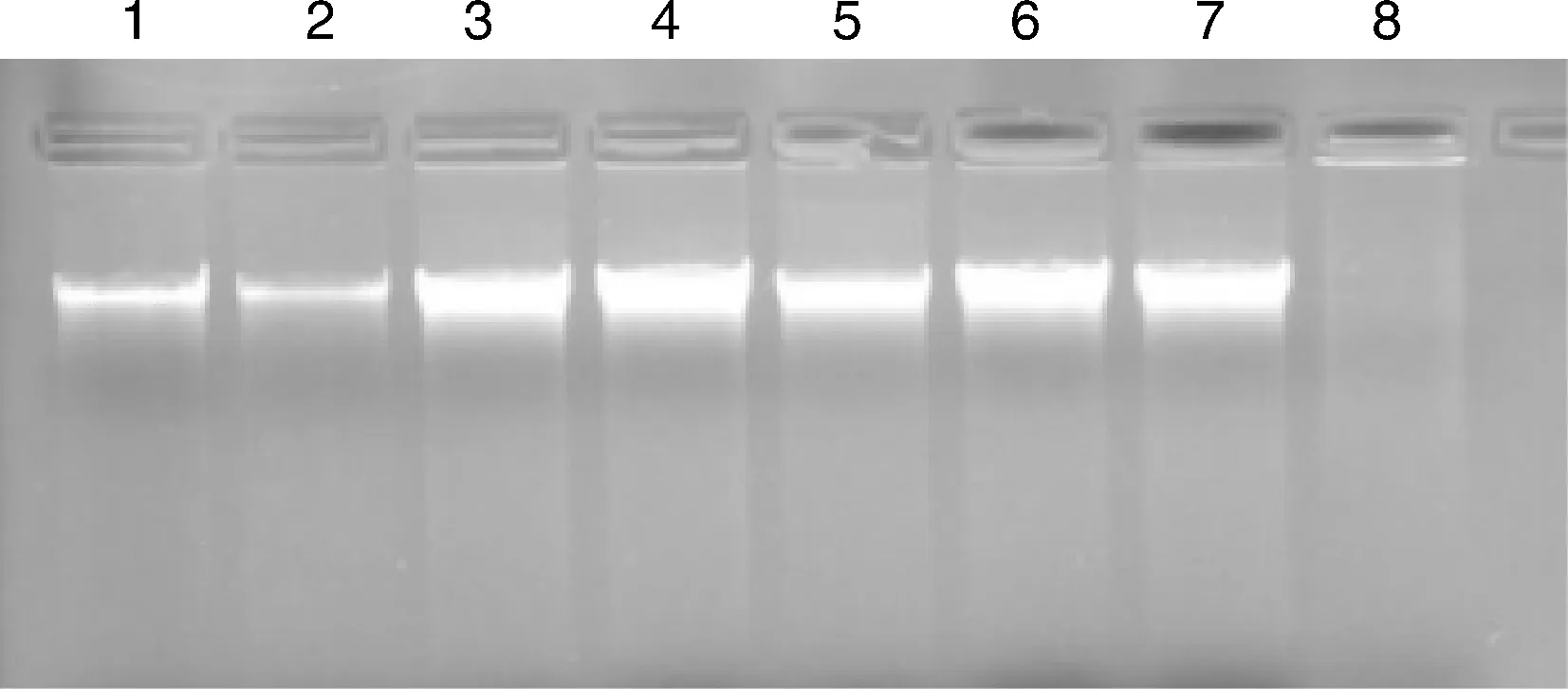
1,改良CTAB组;2~4,F1~F3;5~8,D1~D4。1, CTAB-based group; 2-4, F1-F3; 5-8, D1-D4.图1 不同方法提取的鸭源性DNA电泳检测图Fig.1 Electrophoresis detection of duck DNA extracted by eight DNA extraction methods
2.2 不同提取方法对生鲜肌肉组织样品DNA浓度和纯度的影响
采用NanoDrop 2000核酸蛋白测定仪测定DNA浓度。鉴于每种方法的初始取样量不同,因此将浓度均换算为每25 mg样品所提取的DNA浓度。如表1所示,国外品牌F1试剂盒的DNA总量最低,与鱼加工制品中的结论一致[30];改良CTAB法提取的DNA总量高于F1试剂盒;其他方法提取的DNA总量要高于改良CTAB法和F1,且提取平均总量相当。
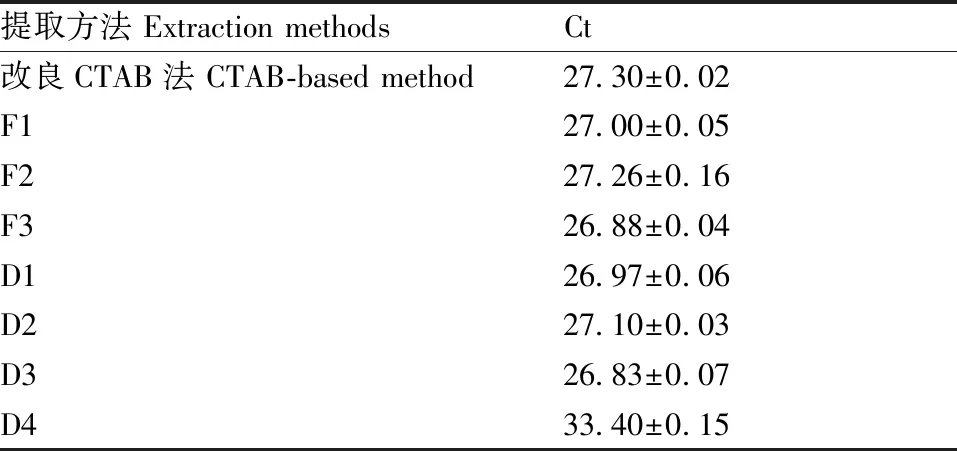
采用NanoDrop 2000测定所提取DNA的杂质去除情况,D260/D280可用来衡量蛋白质的去除情况,D260/D230可用来衡量盐分去除情况。如表1所示,DNA快速萃取法获得的DNA纯度最低,所有被检样本DNA的D260/D280为1.08~1.45,表明提取的DNA中存在较多的蛋白残留。对改良CTAB法而言,牛羊肉肌肉组织中提取核酸的纯度较低(1.6 如图2所示,不同方法所提取的鸭源性DNA均能用于PCR扩增。当鸭肌肉组织DNA稀释至同一浓度后,进行TaqMan法实时荧光PCR时,除DNA快速萃取法(D4)外,其他7种方法的Ct值都在26.83~27.30之间(表2),说明这7种方法所提取的DNA质量均较好,不影响PCR扩增。而DNA快速萃取法的Ct值要比其他7种方法的Ct值大,表明该方法虽然在提取速度上占有优势,但提取的DNA中可能存在某些PCR抑制因子,能显著抑制PCR反应。 表1 不同肉源品种DNA提取的比较 Table1Comparison of DNA extraction from different meat sources 提取方法Extraction methods样品种类SpeciesD260/D280D260/D230DNA浓度DNA concentration/(ng·μL-1)DNA总量DNA content/μg改良CTAB法鸭肉 Duck1.91±0.010.63±0.01129.6±1.012.96±0.10CTAB-based method牛肉 Beef1.61±0.020.75±0.0153.6±2.05.36±0.20羊肉 Mutton1.66±0.010.53±0.0162.8±1.06.28±0.10鸡肉 Chicken1.79±0.010.66±0.01100.1±1.510.01±0.15猪肉 Pork1.78±0.010.77±0.0153.9±1.05.39±0.10F1鸭肉 Duck1.88±0.012.18±0.0118.0±0.71.80±0.07牛肉 Beef1.85±0.011.85±0.026.00±0.20.60±0.02羊肉 Mutton1.81±0.012.02±0.0111.1±1.01.11±0.10鸡肉 Chicken1.87±0.012.29±0.0126.9±1.02.69±0.10猪肉 Pork1.85±0.021.94±0.016.6±0.30.66±0.03F2鸭肉 Duck1.98±0.011.99±0.01532.5±5.053.25±0.50牛肉 Beef2.00±0.012.11±0.0118.0±1.01.80±0.10羊肉 Mutton1.94±0.012.11±0.0136.0±1.03.60±0.10鸡肉 Chicken2.02±0.012.11±0.02327.7±3.032.77±0.30猪肉 Pork1.90±0.011.97±0.0146.2±1.04.62±0.10F3鸭肉 Duck1.98±0.012.78±0.01416.8±3.041.68±0.30牛肉 Beef2.06±0.012.76±0.0329.4±1.02.94±0.10羊肉 Mutton2.02±0.022.24±0.0183.8±1.08.38±0.10鸡肉 Chicken2.10±0.012.19±0.01201.0±3.020.10±0.30猪肉 Pork2.00±0.012.10±0.0181.4±1.08.14±0.10D1鸭肉 Duck2.07±0.012.24±0.01413.8±1.041.38±0.10牛肉 Beef2.02±0.017.22±0.0132.2±1.03.22±0.10羊肉 Mutton2.01±0.013.13±0.01124.7±1.012.47±0.10鸡肉 Chicken2.07±0.012.39±0.01208.4±2.120.84±0.21猪肉 Pork1.97±0.012.62±0.0186.0±1.08.60±0.10D2鸭肉 Duck2.02±0.011.58±0.01796.9±3.679.69±0.36牛肉 Beef1.85±0.010.84±0.0146.5±1.04.65±0.10羊肉 Mutton1.97±0.011.28±0.01100.9±3.010.09±0.30鸡肉 Chicken2.01±0.011.47±0.01317.4±2.331.74±0.23猪肉 Pork1.95±0.011.17±0.01164.0±1.216.40±0.12D3鸭肉 Duck2.03±0.012.30±0.01560.1±2.356.01±0.23牛肉 Beef2.05±0.012.91±0.0124.6±0.62.46±0.06羊肉 Mutton1.95±0.012.62±0.0182.2±1.08.22±0.10鸡肉 Chicken2.07±0.012.40±0.01163.2±1.216.32±0.12猪肉 Pork1.97±0.012.69±0.0185.9±1.08.59±0.10D4鸭肉 Duck1.35±0.030.37±0.01443.0±3.144.30±0.31牛肉 Beef1.08±0.010.14±0.01149.2±1.814.92±0.18羊肉 Mutton1.09±0.061.18±0.01152.2±1.215.22±0.12鸡肉 Chicken1.45±0.050.39±0.01466.8±2.946.68±0.29猪肉 Pork1.17±0.030.21±0.01259.2±1.625.92±0.16 根据上述测定的DNA浓度、D260/D280、D260/D230、实验耗时及PCR扩增结果等数据,对各DNA提取方法进行综合分析。改良CTAB法价格较低,但起始量要求高,操作烦琐,耗时长(6 h);F1试剂盒法去除杂质、盐渍效果好,但耗时长(6 h),DNA获得率低;F2试剂盒法去除杂质、盐渍效果好,但价格昂贵,耗时长(6 h);F3试剂盒耗时4 h,但价格昂贵;D1试剂盒价格相对低廉,提取的DNA纯度高、盐残留少,但操作步骤烦琐;D2试剂盒提取的DNA纯度高,获得率高,但盐残留多,耗时长(6 h);D3试剂盒耗时较短(4 h),提取的DNA纯度高、盐残留少,DNA获得率高;D4试剂盒操作简便,耗时短(3 h),但去除杂质效果差,纯度低,盐残留多。 图2 TaqMan法实时荧光定量PCR扩增鸭源性DNA中IL-2核基因的扩增曲线Fig.2 The real-time TaqMan PCR for IL-2 detection with the duck-derived genome DNA extracted by the eight methods 表2 八种方法提取鸭源性DNA用于实时荧光定量PCR扩增IL-2核基因的Ct值 Table2The Ct values of the real-time fluorescent PCR amplification theIL-2 gene with the duck-derived genome DNA extracted by the eight methods 提取方法 Extraction methodsCt改良CTAB法 CTAB-based method27.30±0.02F127.00±0.05F227.26±0.16F326.88±0.04D126.97±0.06D227.10±0.03D326.83±0.07D433.40±0.15 食品安全关系着人类身体健康,是全社会关注的热点问题。近年来肉制品掺假屡禁不止,引发人们对食品安全的恐慌,也对食品监管部门快速、准确进行动物源性成分检验和鉴定提出了更高的要求。以DNA为基础的PCR技术已经被广泛用来鉴定食品中的动物源性成分,而高质量、高纯度及结构完整的DNA是影响PCR扩增的重要因素。因此,快速、稳定、优质的DNA提取方法是PCR扩增成功的关键[20]。 本研究对常见的5种常见肉类的肌肉组织进行DNA提取,并对完整性、DNA浓度、纯度、盐残留和耗时等指标进行了对比。8种提取方法虽然均可用肌肉组织的DNA提取,但每种方法各有利弊。改良CTAB法虽然价格实惠且对PCR扩增无抑制作用,但其操作较为繁琐,提取时间长,且涉及有机溶剂抽提,对人体有一定的潜在伤害;DNA快速萃取法耗时最短,但DNA纯度和盐残留指标最差,且提取的DNA溶液中含抑制PCR的成分,影响荧光定量PCR的扩增效率;原理为蛋白酶K法的F1试剂盒虽然去除杂质、盐渍效果较好,但试剂盒耗时长,且DNA得率最低,性价比较低;而基于蛋白酶K法和SDS法的F3和D3试剂盒的耗时相对较短,DNA的纯度高,盐残留少,DNA总量理想,DNA提取液对实时荧光定量PCR的抑制少。 综上所述,对常见动物肌肉组织而言,基于蛋白酶K法和SDS法的F3和D3试剂盒在试验耗时、DNA纯度和浓度、盐残留、对荧光定量PCR的抑制等方面均优于其他试剂盒方法,可优先选择这2种试剂盒进行DNA提取。本研究可为食物掺假和物种鉴别工作中DNA提取方法及样品处理方案提供参考。2.3 不同提取方法提取的DNA提取物对实时荧光定量PCR的抑制作用
2.4 不同DNA提取方法的比较


3 讨论

