人教版与全华版探究化学反应速率影响因素的实验对比
汪金虹 李学强


摘要:大陆人教版和台湾全华版高中化学中的实验设置有很大的差异,本文以浓度和温度对化学反应速率的影响的实验为例,通过对比两版教材中实验设置的理论研究、实验试做,以及高中课堂(高二)学生对实验的试做,观察实验现象、收集实验数据,从实验类型、实验原理、实验效果、学生对实验的兴趣,以及实验设置的理念等各角度进行对比分析,得出结论。对两版教材中影响化学反应速率的因素的对比研究,可以为人教版教材中的实验改进提供建议,同时可以丰富学生的知识视野、启发学生的思维。
关键词:人教版;全华版;化学反应速率;对比分析
文章编号:1008-0546( 2019)08-0082-03
中图分类号:G632.41 文献标识码:B
doi: 10.3969/j .issn.1008-0546.2019.08.026
化学反应速率在高中化学中占有非常重要的地位,对学生理解化学反应的本质具有很重要的意义。人教版教材中对研究影响化学反应速率的实验分别选自必修2和选修4,必修2只设置了温度和催化剂对化学反应速率影响的实验,且实验原理和实验过程都较简单,本文选择选修4教材中的实验进行对比。人教版教材中的实验注重探究性,旨在通过实验探究,观察实验现象获取新知识,教材中只给出了实验药品,没有列出特定的实验步骤和操作方法,属于探究性实验。全华版教材中的实验是在学习完理论知识后设置的,目的在于通过实验验证理论知识的准确性,实验既给出了实验用品,又给出了特定的实验步骤、实验装置图和实验操作方法,属于验证性实验。
一、两版教材中浓度对化学反应速率影响的实验对比研究
1.全华版教材中浓度对化学反应速率影响的实验
(1)实验原理
103( aq)+3HS03( aq)→ I-(aq)+3SOi-(aq)+3H+(aq)
103( aq)+51-(aq)+6H+(aq)→312(s)+3H20(1)
反应过程中产生碘单质,利用碘遇淀粉变蓝色的特性,通过蓝色出现的时间判断化学反应速率的快慢。
实验药品:碘酸钾固体、亚硫酸氢钠固体、稀硫酸溶液、淀粉指示剂。
(2)實验过程
①溶液的配制
A溶液:称取2.14g KIO3固体,加蒸馏水配制成500mL 0.02mol/L的KI03溶液。
B溶液:称取0.0416g NaHSO3固体,加蒸馏水配制成lOOmL 0.004mol/L NaHS03溶液。
称取2 9土豆淀粉加入20mL的蒸馏水,搅拌均匀后再加400mL热水,冷却至室温后,取淀粉溶液的上清液与NaHS03溶液混合,再加SmL稀硫酸溶液,配制得B溶液。
②观察实验现象及记录实验数据
首先取lOmL 0.02mol/L KI03溶液和lOmL B溶液混合后立即计时并观察实验现象。
另取4支试管,依次配制不同浓度的溶液,
溶液A H20
8mL+2mL
A1 cl= 0.016mol/L
6mL+4mL
A2 c2= 0.012mol/L
4mL+6mL
A3 c3 =0.008mol/L
2mL+8mL
A4
c4=0.004mol/L
分别与lOmL的B溶液混合,记录各自的反应时间。
实验现象:几组不同浓度反应物的现象都由无色变为蓝色,但变色时间长短不同。
2.人教版教材中浓度对化学反应速率影响的实验
(1)实验原理
2KMn04+ 5H2C204+ 3H2S04=K2S04+ 2MnS04+10C02↑ +8H20
发生氧化还原反应,使高锰酸钾溶液的紫色褪去,通过高锰酸钾紫色褪去的时间判断化学反应速率的快慢。
(2)实验过程
①溶液的配制
KMn04溶液:称取0.316g固体配成200mLO.Olmol/L KMn04溶液
H2C204溶液:称取9g固体配制成500mL 0.2mol/LH2C2O4溶液
②观察实验及记录数据
由于笔者在上课前进行实验试做时发现,室温下此反应高锰酸钾溶液褪色的时间会长达10分钟以上,反应时间过长,课堂中的学生实验无法实验,故将条件改为35℃左右的热水浴,将不同浓度的混合液放在同一水浴中。
取两支试管,各加入4mL O.Olmol/L的KMn04酸性溶液,然后向一支试管中加2rriL O.lrriol/L H2C204(草酸)溶液,记录溶液褪色所需的时间;向另一支试管中加2mL 0.2mol/L H2C204溶液,记录溶液褪色所需的时间。
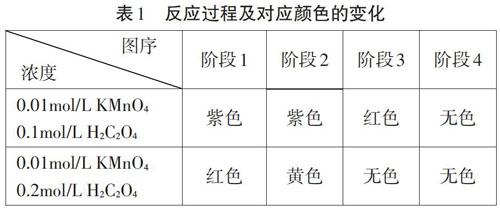
人教版教材中浓度对化学反应速率影响的实验现象经过了四个不同的变色阶段,最终都变为无色,变色过程见表l所示:
3.实验数据及结果分析
两版教材中浓度对化学反应速率影响的实验现象数据统计见表2所示:
全华版教材设置了5组不同浓度的反应物进行对比,由实验数据可以看出随着碘酸钾浓度的依次减小,反应时间逐渐增大,时间间隔明显,而且每组反应时间都不长,适合课堂实验。人教版教材中共设置了两组不同浓度的实验,由实验数据可知,即使在热水浴中反应时间也要两分钟左右,且颜色是由紫色一红色一黄色一无色,反应过程中颜色变化较复杂,达不到预期的实验效果。由上述可得出结论,关于探究浓度对化学反应速率影响的实验,全华版教材中的实验对比明显、实验结果能充分验证理论知识,所以,对于此实验全华版教材中的优于人教版教材中的。
二、两版教材中温度对化学反应速率影响的实验对比研究
1.全华版教材中温度对化学反应速率影响的实验
实验药品:全华版教材中关于温度对化学速率影响的实验药品与浓度实验相同,只是将原来0.02mol/L KI03溶液稀释至O.Olmol/L,得到As溶液,继续与原来的B溶液反应。
(1)实验过程
①用分度吸量管精确量取lO.OmL的As溶液,置入一试管中,再用另一支分度吸量管,吸取lO.OmL的溶液B,置入另一支试管中。
②将两试管放入装有八分满的大烧杯(500mL)中,测量大烧杯的水温,将此两试管静置一段时间(约3-5分钟)后,利用水浴法使两溶液的温度与水温相同。
③将同温度的两溶液,同时倒入一个干净小烧杯( lOOmL),立即按下秒表计时,轻轻摇动烧杯使溶液混合均匀,当溶液显现出蓝黑色时,停止计时并记录反应所需的时间。
④以冰块或加热等方式改变不同的水浴温度( 15℃-35℃),选择4个不同的温度,重复上述步骤1到步骤3,测量不同反应温度下溶液显现蓝黑色所需的时间。
(2)实验现象
在15℃、20℃、26℃、35℃水浴中静置过的反应物混合后溶液均能快速变为蓝色。
经实验过程发现,不论是热水浴还是冷水浴,反应都很快就能完成,经15℃的冷水静置4min左右反应时间为4.9ls,当温度升高时反应时间更短。
2.人教版教材中温度对化学反应速率影响的实验
(1)实验原理
Na2S203+H2S04一Na2S04+S02 ↑ +S↓ +H20
反应过程依据出现S单质白色沉淀的时间判断化学反应速率的快慢。
(2)实验过程
①配制溶液
称取7.9克硫代硫酸钠固体配制成500mL O.lmol/L溶液;稀释浓硫酸得到O.lmol/L的稀硫酸溶液。
②观察实验现象及记录实验数据
取两支试管各加入5mL O.lmol/L Na2S203溶液,另取两支试管各加入5min O.lmiol/L H2S04溶液:将盛有Na2S203溶液的两試管分别放入8℃的冷水和35℃的热水中,分别迅速倒入5mL O.lmol/L H2S04溶液后开始计时,记录出现浑浊的时间。
实验现象:35℃水浴的烧杯出现大量的浑浊:8℃水浴的烧杯出现少量浑浊。
实验发现在冷水中和热水中出现浑浊的时间明显不同,热水中出现沉淀的时间短,且现象明显、易于观察。
3.实验数据及结果
两版教材中温度对化学反应速率影响的实验现象及数据统计见表3所示:
全华版教材共设置了五组探究温度对化学反应速率影响的实验,虽然使用的药品和浓度相同,减少了实验准备工作,但经实验过程发现,实验过于灵敏,可能是由于碘酸钾浓度过大,几组实验的时间间隔差别太小,不能充分验证温度越大反应速率增大的结论。人教版教材设置了两组实验,分别是在冷水和热水中进行,没有明确规定实验的温度,学生实验过程中为了与全华版教材中的实验形成对比,选择8℃与35℃的水浴,实验现象明显,能形成鲜明对比,由于两种水温下,时间间隔大,笔者建议还可在这两温度间选择几种温度进行实验。
三、结论
经实验研究发现,关于浓度对化学反应速率的影响的实验,学生更认同全华版教材中的,关于温度对化学反应速率的影响认为人教版教材中的实验对比更鲜明,但建议多加几组实验,进行对比。由此可见两版教材都有各自的优缺点,通过对比分析可以吸收不同教材中的优势。
参考文献
[l]宋心琦主编.普通高中课程标准实验教科书:化学反应原理:选修4[M].北京:人民教育出版社,2007
[2]林万寅主编.普通高级中学基础化学(三)[M].台北:全华图书股份有限公司,2016:12
[3]石月香.人教版与翰林版浓度对反应速率影响实验对比[J].中国现代教育装备,2017(12):31-32

