高灵敏乙型肝炎病毒核酸检测在术前筛查中的应用价值
李宝琪 陈培松 黄浩 余学高 黄彬★
乙型病毒性肝炎(viral hepatitis B)简称乙肝,是世界性重大卫生问题。乙肝由乙型肝炎病毒(hepatitis B virus,HBV)引起,可表现为急性肝炎、慢性肝炎和重型肝炎,甚至可演变成肝硬化、肝癌。尽管近年来预防和控制工作取得很大成效,但我国人口基数大,乙肝患者人群庞大,防治形势依然严峻。据报道,目前中国大约有9 300 万人感染HBV,其中2 000 万是慢性乙肝患者[1]。根据2006年全国人群乙肝血清学调查显示,一般人群乙型肝炎表面抗原(HBsAg)阳性率为7.18%,相比于1992年的9.75%虽有所下降,但是,成人HBsAg 阳性率仍高于8%,因此对乙肝的防控仍不容松懈[2]。
HBV 可经血液或血制品传播,并且医源性传播风险较高,包括使用未经严格消毒的医疗器械、不安全进行注射、手术、侵入性操作及血液透析等。因此,为了有效防范、避免和减少手术过程中HBV 的院内交叉感染和传播,以及防范医疗风险和医疗纠纷的发生等,HBV 感染筛查被列为术前筛查的必检项目。目前临床上主要通过免疫学方法检测HBV 血清标志物。该方法虽可反映患者HBV 感染的免疫状态,但易漏检隐匿性感染或感染初期机体未产生特异性抗体的窗口期感染者。若患者感染未知的病毒亚型,该方法也难以检出[3]。
高敏HBV DNA 检测技术灵敏度高、特异性好,缩短了检测的窗口期,能直接反映体内病毒的复制状况,因而在临床上应用越来越广泛。为了提高术前筛查中乙肝的检出率,准确反映患者体内HBV 的复制情况和传染性,有效避免医源性传播,本研究将高敏PCR 法用于术前筛查,并与临床常用的化学发光微粒子免疫分析法(chemiluminescence microparticle immunoassay,CMIA)进行比较,两者定性结果不一致的采用Roche 全自动核酸检测系统进行验证,探讨高敏HBV DNA 检测在术前筛查中的应用价值。
1 材料与方法
1.1 临床样本
收集2019年1月至4月间中山大学附属第一医院术前筛查患者的血清标本519 例,剔除患者的重复标本,避免脂血、溶血等。将每例血清标本分为两份,一份用于血清学检测,当天进行;另一份用于核酸检测,离心分离血清后保存于-80℃备用,避免反复冻融。
1.2 主要仪器与试剂
ABI ViiA7 型荧光定量PCR 扩增仪购自美国ThermoFisher 公司,Smart32 半自动核酸提取仪购自中山大学达安基因股份有限公司,Architecti2000SR 免疫分析仪购自美国Abbott 公司,Cobas AmpliPrep 全自动核酸提取仪和Cobas TaqMan 48全自动病毒载量检测仪购自瑞士Roche 公司,高灵敏乙型肝炎病毒核酸定量检测试剂盒和核酸提取纯化试剂购自中山大学达安基因股份有限公司,Architect HBsAg 试剂盒购自美国Abbott 公司,乙型肝炎病毒核酸定量检测试剂盒(内标法)购自瑞士Roche 公司。
1.3 方法
1.3.1 高敏PCR 法检测HBV DNA
在核酸提取试剂盒的预封装96 孔板中加入4 μL 内标液、20 μL 蛋白酶K、200 μL 血清样本和阴性质控品、临界阳性质控品、强阳性质控品及4 个阳性定量标准品,将其放入Smart32 半自动核酸提取仪,按核酸提取试剂盒说明书设置提取程序。运行结束后,将所得核酸(40 μL/孔)加入PCR 反应管中(含配置好的反应液20 μL)。将PCR 反应管放入ABI ViiA7 型荧光定量PCR 扩增仪,HBV DNA 扩增程序为:50℃2 min,1 个循环;95℃15 min,1 个循环;94℃15 s,55℃45 s,45 个循环。
所采用的高敏HBV DNA 检测试剂盒的检测下限为10 IU/mL,若FAM 检测通道无明显对数增长期,且VIC 检测通道有对数增长期,或定量结果低于相应试剂盒检测下限,则判定该标本核酸检测阴性;若FAM 检测通道和VIC 检测通道均有对数增长期,且Ct 值小于45,定量结果大于相应试剂盒检测下限,则判定该标本核酸检测阳性。
1.3.2 CMIA 法检测HBsAg
在每日常规质控通过后,将待检标本放入Architect-i2000SR 免疫分析仪进行检测,严格按照试剂说明书操作,记录仪器最终检测结果。HBsAg 正常参考范围为0.00~0.05 IU/mL,HBsAg>0.05 报告为阳性。
1.3.3 Roche 全自动核酸检测系统检测HBV DNA
对于上述核酸检测方法与血清学检测方法定性结果不一致的标本,进一步采用Roche Cobas AmpliPrep/Cobas 全自动核酸检测系统检测HBV DNA。血清标本经Cobas AmpliPrep 全自动核酸提取仪提取核酸,将配好的PCR 反应体系转移到Cobas TaqMan 48 全自动病毒载量检测仪进行高敏荧光定量PCR。
所采用的HBV DNA 定量检测试剂盒的检测下限为20 IU/mL,结合PCR 扩增曲线与Ct 值综合判断,若定量结果低于20 IU/mL,则判定该标本HBV DNA 阴性;若定量结果大于20 IU/mL,则判定该标本HBV DNA 阳性。
以2 方法一致的结果和Roche 全自动核酸检测系统复核的结果为这批标本的最终结果(金标准结果),用以评价高敏PCR 法和CMIA 法的检测性能。
1.3.4 统计学分析
采用SPSS 22.0 统计学软件分析,计量资料以P50(P25,P75)表示,行Kruslal&Wallis H 检验和Mann-Whitney U 检验分析;计数资料以%表示,行χ2检验:以P<0.05 为差异有统计学意义。
2 结果
2.1 高敏PCR 法与CMIA 法的检测结果比较
519 例患者标本中,HBsAg 阳性标本90 例,阳性率为17.3%,其中13 例标本(占阳性样本的14.4%)的HBV DNA 低于高敏PCR 法的最低检测限;HBV DNA 阳性标本79 例,阳性率为15.2%,其中2 例标本HBsAg 阴性,CMIA 的漏检率为2.5%。有15 例标本的定性检测结果不一致。经χ2检验分析,高敏PCR 法与CMIA 法对HBV 的检出率差异有统计学意义(P<0.05),见表1。

表1 HBV DNA 与HBsAg 检测结果比较Table 1 Comparison the results of HBV DNA and HBsAg
2.2 HBsAg 阳性标本的HBV DNA 定量
90 例HBsAg 阳性标本按HBsAg 定量结果分为5 组,经Kruskal-Wallis H 检验得到5 组间HBV DNA 载量差异,且差异有统计学意义(P<0.05),经Mann-Whitney U 检验两两比较,I 组HBV DNA 高于II、III、IV、V 组,差异有统计学意义(P<0.05)。其余各组间差异无统计学意义(P>0.05)。见表2。

表2 HBsAg 阳性标本的HBV DNA 定量结果比较Table 2 Comparison of HBV DNA quantitative results in HBsAg-positive samples
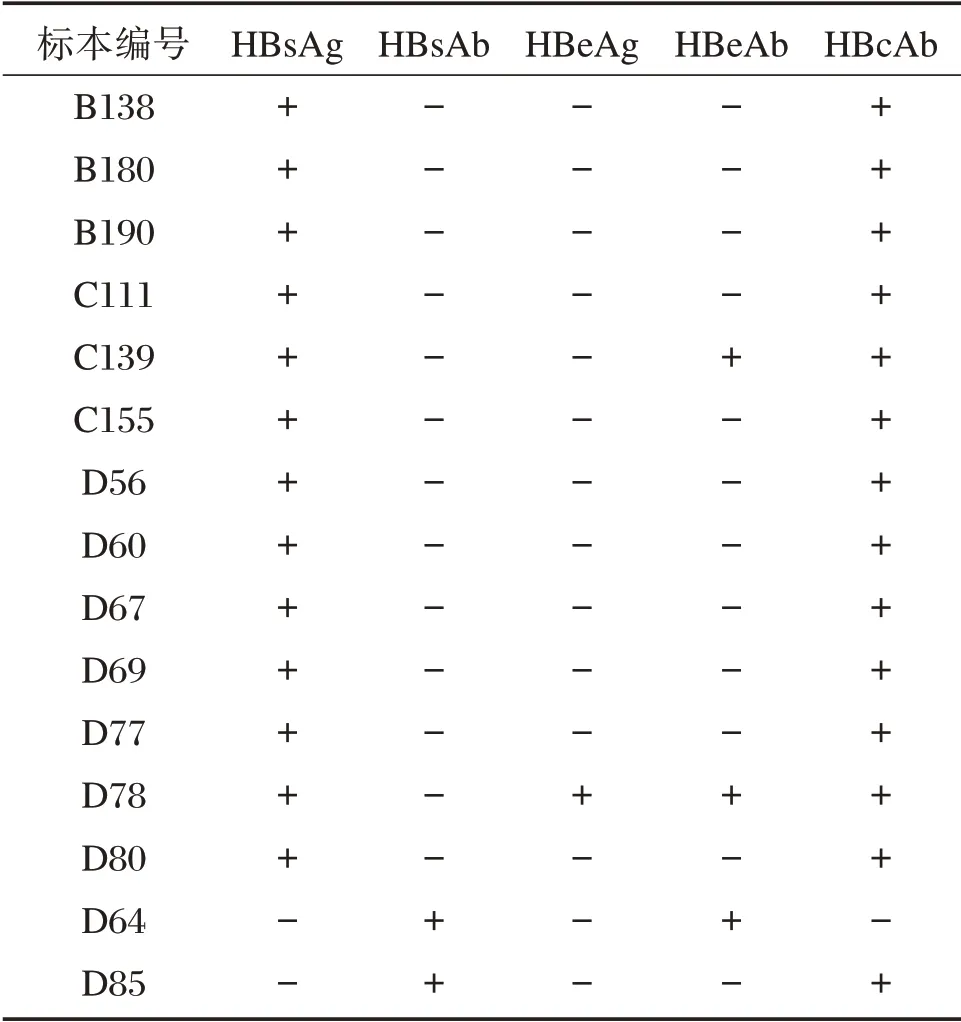
表3 15 例结果不一致标本乙肝两对半检查结果Table 3 Serum markers for HBV infection of 15 samples with inconsistent results
2.3 检测结果不一致标本的复核
15 例定性检测结果不一致的标本经Roche 全自动核酸检测系统复核后,13 例HBV DNA 阴性而HBsAg 阳性标本的HBV DNA 均低于该方法的最低检测限,仍为阴性。这13 例标本的两对半结果中11 例为HBsAg、HBcAb 阳性,1 例为HBsAg、HBeAb 和HBcAb 阳 性,1 例 为HBsAg、HBeAg、HBeAb 和HBcAb 阳 性,结 果 见 表3。2 例HBV DNA 阳性而HBsAg 阴性标本的HBV DNA 高于该方法的最低检测限,仍为阳性,见表4。

表4 15 例结果不一致标本的复核情况Table 4 Redetection of 15 samples with inconsistent results
2.4 高敏PCR 法与CMIA 法的检测性能比较
高敏PCR 法的灵敏度、特异度、阳性预测值(positive predict value,PPV)和阴性预测值(negative predict value,NPV)均为100.0%;CMIA法检测HBsAg 的灵敏度、特异度、PPV、NPV 分别为97.5%、97.0%、85.6%、99.5%。高敏PCR 法检测HBV 的特异度和PPV 高于CMIA 法(P<0.05),其他指标的差异无统计学意义(P>0.05),见表5。
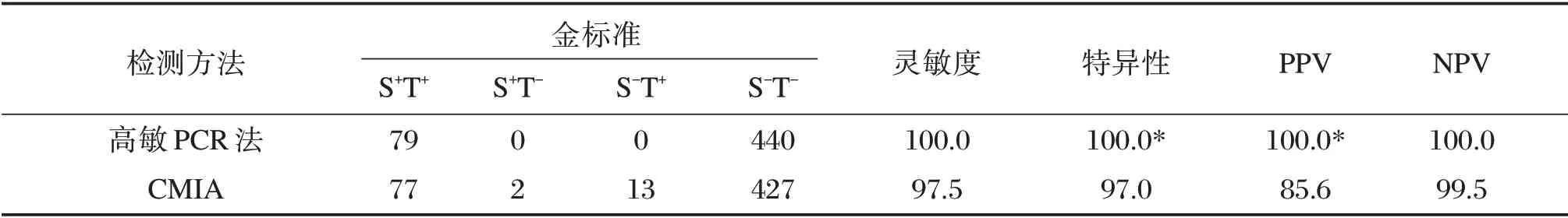
表5 高敏PCR 法与CMIA 法的检测性能[n(%)]Table 5 The performance of high-sensitive PCR and CMIA[n(%)]
3 讨论
HBV 主要通过输注血液、血制品,皮肤黏膜破损和不安全注射等途径传播,其医源性传播风险较高,使用未经严格消毒的医疗器械、手术、侵入性操作以及血液透析等均有感染风险。有研究表明,维持性血液透析患者的肝炎病毒感染率比一般人群高,可能与反复输注血液及血制品、透析用品消毒不严格和院内交叉感染有关[4]。因此把控血液安全、严格做好术前筛查是阻断HBV传播的关键环节。
目前,临床上检测HBV 感染的方法主要有血清学检测技术和分子诊断技术两种。血清学检测是利用病毒抗原或针对病毒抗原的特异性抗体检测患者体内血清标志物的方法,HBV 血清学检测指标主要包括HBsAg、HBsAb、HBeAg、HBeAb 和HBcAb;主要检测方法有胶体金法、酶联免疫吸附试验、化学发光法和重组免疫印迹试验等,其中化学发光法具有较高灵敏度与特异性[9],且适用于自动化仪器检测,在临床上得到广泛应用。然而血清学检测存在缺陷,易漏检感染窗口期、病毒隐匿性感染或者血清中病毒拷贝数极低的患者[5-6]。因此为了实现对HBV 感染的早期诊断,有效防范和避免医疗过程中的交叉感染及医疗纠纷等,需要更为灵敏且能反映病毒传染性的检测方法。高敏PCR 法灵敏度高、特异性好通过设计针对病毒保守序列的特异性引物扩增病毒及其变异株核酸,并将检测信号放大,显著提高了检出率,很好地解决了血清学检测的缺陷。并且可进行高灵敏度病毒载量检测,操作简便,在临床上应用广泛。高敏HBV DNA 定量检测(最低检测限10~15 IU/mL)已被美国肝病学会、欧洲肝病学会及2015年中华医学会肝病学分会、中华医学会感染病学分会出台的慢性乙型肝炎防治指南推荐使用[7-9]。
本研究中90 例HBsAg 阳性标本按HBsAg 定量结果被分为5 组,I 组(HBsAg>5 000 IU/mL)标本的HBV DNA 显著高于II、III、IV 和V 组,但II、III、IV、V 组之间的HBV DNA 定量结果差异并无统计学意义,提示当血清标本HBsAg 定量水平处于0.05~5 000 IU/mL 间时,它们的HBV DNA 定量结果没有显著差异。目前血清HBsAg 与血清HBV DNA 定量之间的相关性仍存在争议[10-12],有报道指出在慢性HBV 感染过程中两者之间是否存在相关性与患者所处的感染阶段有关[13]。另有报道指出HBeAg 阳性患者中血清HBsAg 与血清HBV DNA定量之间存在良好相关性,而在HBeAg 阴性患者中两者不存在相关性[14]。
90 例HBsAg 阳性标本中HBV DNA 阳性率为85.56%,有13 例标本经高敏PCR 法检测低于最低检测限,为阴性。查询病历得知这13 名患者均为慢性乙肝患者,12 例为HBeAg 阴性患者。研究报道,慢性乙肝患者用药治疗后,HBV 的复制可被抑制,不具有传染性,但HBV S 区基因可整合至宿主肝细胞基因组中持续表达HBsAg,因而血清中HBsAg可长期阳性,但此时血清中HBV DNA 可低于高敏PCR 法的最低检测限而检测不到[15-16]。该13 例标本的HBsAg 平均含量为(543.10±487.48)IU/mL,12 例标本均为较低水平[17-18],含量介于(20.02~978.21)IU/mL,另1 例标本的HBsAg 含量为1 720.96 IU/mL,两对半为HBsAg、HBeAg、HBeAb 和HBcAb 阳性。高敏PCR 法均检测不到这13 例患者血清标本中的HBV DNA,这与黄劲松等的研究结果一致[19],低水平HBsAg 不足以评价HBV 的复制情况和传染性,需结合核酸检测结果。因此,相比于血清学检测,尤其是血清HBsAg 处于较低水平时,高敏HBV DNA 检测更能准确反映患者体内病毒的复制情况和传染性。
519 例血清标本中,79 例HBV DNA 阳性标本中有2 例HBsAg 阴性,CMIA 法的漏检率为2.5%。查询病历得知,该2 例患者均为肾移植术后患者。其中1 例患者乙肝两对半检测无异常,HBsAb 滴度处于较低水平,另外1 例患者HBcAb 阳性。这2 例患者可能为HBV 窗口期感染或隐匿性HBV 感染(occult hepatitis B virus infection,OBI),需随访跟踪调查。有学者对HBsAg 阴性血液进行高敏PCR确认,发现0.07%为假阴性,且造成假阴性的主要原因是OBI[20],OBI 患者血清中HBsAg 含量低于血清学试剂盒检测下限,可能是由于HBV PreS/S 区突变导致抗原变异或表达减少,也可能与患者免疫状态有关,从而表现为血清中HBsAg 检测阴性而血清或肝组织中有低载量HBV DNA[21-22]。OBI 可导致不明原因肝癌、输血感染、器官移植感染和慢性肝炎等,且血清学筛查难以发现,而高敏HBV DNA 检测可弥补这一缺陷。
本研究中15 例高敏PCR 法与CMIA 法定性结果不一致的样本采用Roche 全自动核酸检测系统复核后,高敏PCR 法的检测结果与Roche 全自动核酸检测系统的结果完全一致。高敏PCR 法的结果与金标准结果相比,灵敏度、特异度、PPV、NPV均为100%,提示研究中所用的国产高敏PCR 试剂检测性能优良,能达到优异的检测效果[23]。且与进口试剂相比,能大大降低检测成本,造福广大患者。
综上所述,高敏HBV DNA 定量检测可用于术前筛查乙肝患者,能准确反映患者体内HBV 的复制情况和传染性,及时发现隐匿性感染,有效防止医源性传播。

