酸度控制的不同MnO2的水热制备及电化学性能
朱 刚,史亚鹏,王陶陶,苏 悦,费少春,李念雪,李佳奇
(1.西安文理学院化学工程学院,西安 710065;2.力神电池股份有限公司研究院,天津 300384)
1 引 言
MnO2是一种非常重要的功能材料,具有价格低廉、结构多样、应用广泛等特点,因而备受科研工作者关注。尤其是近年来MnO2作为电极材料用于超级电容器和锂离子二次电池等储能器件,吸引了更多研究者的目光。研究结果表明,MnO2的电化学性能与其结构和形貌有密切关系,因而MnO2的制备一直是研究者的关注点之一,尤其是同一体系中不同晶相和形貌MnO2的可控制备。Suib小组[1]基于K2Cr2O7和MnSO4在酸性介质中的反应通过改变反应温度制备了树枝状和海胆状α-MnO2。Gao等[2]借助于KMnO4和铵盐之间的反应通过改变溶液中共存阴离子的种类制备了三种形貌的α-MnO2。Yu等[3]通过向K2S2O8和MnSO4反应体系中添加Fe(NO3)3和Al(NO3)3,分别制备了线团状ε-MnO2和纳米棒簇α-MnO2。Yang课题组[4]通过改变KMnO4和MnSO4体系的反应时间,制备了α-MnO2纳米线和β-MnO2微米棒。Zhang等[5]通过同时改变反应温度和时间制备了MnO2纳米花和纳米棒。
虽然研究者已经采用水热/溶剂热法、回流法、液相沉淀法等多种方法制备了大量不同晶相和形貌的MnO2,但在同一体系中实现不同结构和形貌的可控制备依然具有挑战性。依据实验条件,充分了解如何控制不同结构MnO2的生长和形态具有重要意义。目前,关于反应温度和时间、反应物种类、溶剂、添加剂等对MnO2结构和形貌影响的报道很多,而关于体系酸度的影响研究较少。本文以KMnO4为锰源、CO(NH2)2为还原剂,采用水热合成技术可控制备MnO2。考察体系酸度对MnO2结构和形貌的影响。此外,研究制备所得MnO2作为锂离子二次电池电极材料的电化学性能。
2 实 验
实验试剂均为分析纯,包括:高锰酸钾、尿素和浓硫酸,实验用水为去离子水。称取0.237 g KMnO4和0.541 g CO(NH2)2,依次加入小烧杯中,再向其中加入15 mL H2O。室温下快速磁力搅拌30 min,所得溶液转入25 mL压力溶弹。110 ℃水热反应6 h。抽滤并洗涤沉淀后,在60 ℃干燥12 h,得到棕黑色粉末,记为S1。保持其他条件不变,将溶剂H2O换为不同浓度的H2SO4溶液进行对照实验,具体条件如图1所示,所得产物分别记为S2、S3和S4。
将产物S4、聚偏氟乙烯和乙炔黑混合均匀,用N-甲基吡咯烷酮调成泥浆状,涂覆在铜箔上。80 ℃干燥6 h,裁片,110 ℃真空干燥12 h。以锂片为对电极和参比电极,组装纽扣电池。
采用D2 PHASER型X-射线衍射仪(XRD)进行产物的物相和结构分析,扫描速率为8°/min,扫描范围为5°~70°。采用S-3400N型扫描电子显微镜(SEM)进行产物的形貌观察。采用V-Sorb 2800型气体吸附分析仪进行产物的比表面积测试。采用CT2001A LAND型电池测试系统对组装电池的循环性能和倍率性能进行测试(25 ℃)。

图1 MnO2的制备路线图Fig.1 Preparation route of MnO2
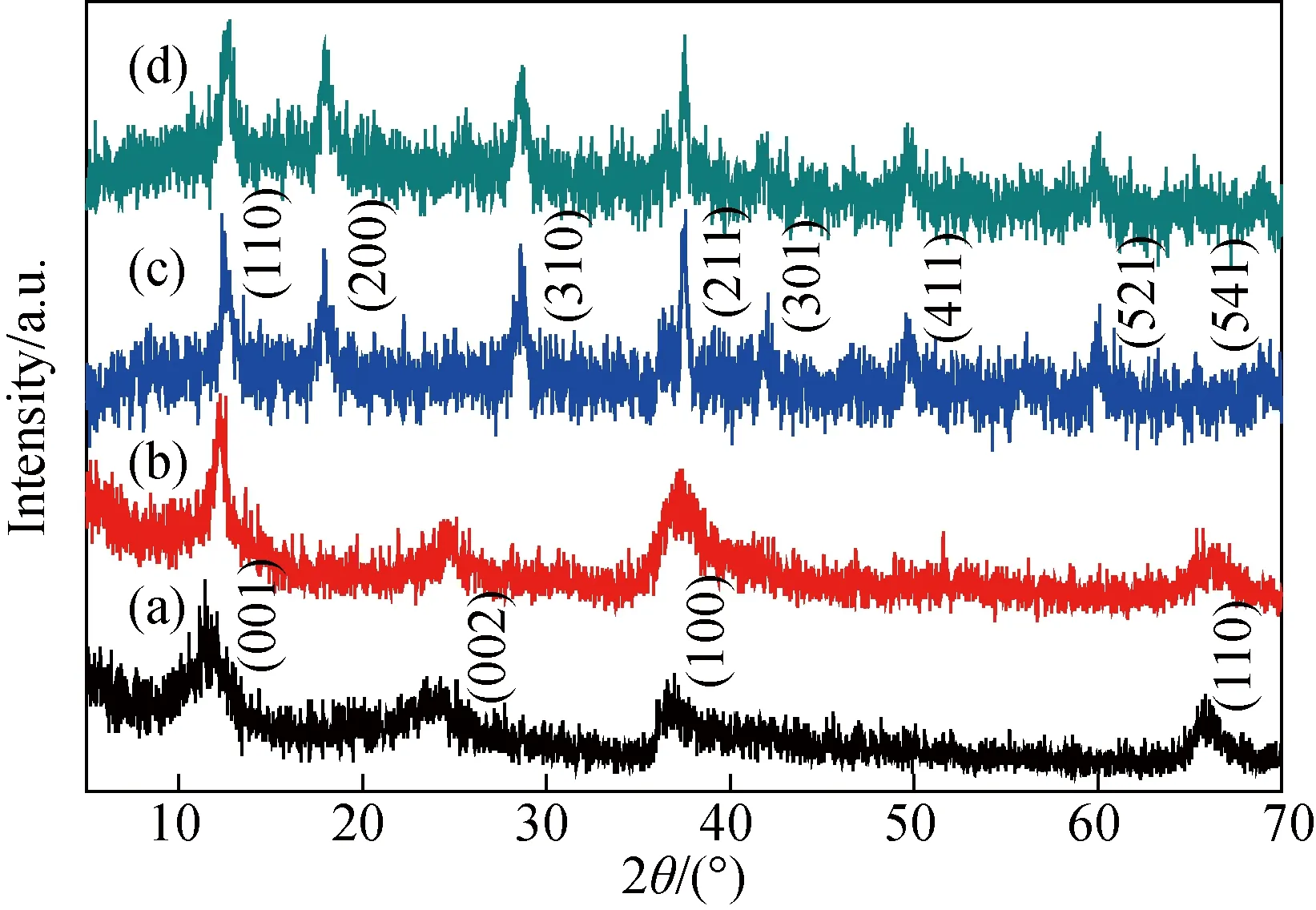
图2 产物的XRD图谱Fig.2 XRD patterns of the products
3 结果与讨论
在不同酸度条件下,KMnO4和CO(NH2)2水热反应所得产物S1、S2、S3和S4的XRD图谱分别如图2(a)、(b)、(c)和(d)所示。可以看出,衍射峰清晰可见且较为尖锐,表明产物的结晶性良好。S1和S2具有相似的XRD图谱,在约12°、24°、36°和66°位置出现衍射峰,对应(001)、(002)、(100)和(110)晶面,表明产物为δ-MnO2(JCPDS No. 80-1098)[6]。δ-MnO2为层状结构,层间距约为0.7 nm,层间有K+离子和水分子(见图1)。S3和S4具有一致的XRD图谱,各衍射峰分别对应(110)、(200)、(310)、(211)、(301)、(411)、(521)、(541)晶面,可指标化为α-MnO2(JCPDS No. 44-0141)[7]。α-MnO2具有隧道型结构,隧道尺寸为0.46 nm×0.46 nm,孔道中有K+和水分子(见图1)。XRD图谱上未出现其他物质的衍射峰,说明制备MnO2的纯度高。由图2还可知,随着酸度的增加,MnO2由层状结构向隧道型结构转变。当溶液中H+浓度逐渐增大时,MnO2层板中的Mn3+会歧化,从而导致层板坍塌,最终转变为隧道结构。
图3为产物S1、S2、S3和S4的SEM照片。可以看出,四种产物的形貌明显不同。在近中性条件下,S1为颗粒状,均一性较差。在0.2 mol/L H2SO4溶液中,S2主要呈球形,直径约3 μm。同时有颗粒状产物共存。当H2SO4溶液浓度增大为0.5 mol/L时,S3为规则的纤维状,长度约1.5 μm,直径100 nm左右。MnO2纤维发生了一定程度的团聚,形成了束状。由图3(d)可见,S4为海胆状。由内插图中放大的照片可以清晰看到,海胆为空心结构。海胆直径约为3 μm,形貌较为规整,分散性良好。

图3 产物的SEM照片Fig.3 SEM images of the products
具有空心结构(包括空心球、空心海胆、空心八面体,等)的物质有很多优点,如比表面积高、密度小、渗透性强,因而是现代材料科学研究热点之一。Wang等[8]以碳球为硬模板,制备了γ-MnO2空心海胆。Liu课题组[9]向反应物中添加三氯化铁,在150 ℃水热条件下制备了α-MnO2空心海胆。相比之下,本方法在制备α-MnO2空心海胆时具有反应温度低、无模板添加等优点,而且反应物廉价易得。
由图1~3结果和上述讨论可知,在温度和时间保持不变的条件下,基于KMnO4和CO(NH2)2之间的水热氧化还原反应可以制备出两种结构、四种形貌和三个维度的纯相MnO2。酸度是决定实验结果的关键因素,仅通过体系酸度的改变,就可以控制MnO2的类型。结构和形貌是决定材料性能的重要因素,因而该实验结果对于可控制备不同晶相和形貌MnO2具有重要的参考价值。
应用氮气吸-脱附技术对S4的表面性质进行测试,其吸-脱附温度线如图4所示。可以看出,在p/p0=0.9~1的高压范围内出现了明显的迟滞环,这与空心海胆表面纳米棒交错形成的间隙有关[10]。根据IUPAC的规定,曲线属于II型等温线,迟滞环为H3型[11]。孔径分布分析结果表明,S4为多孔材料,材料中包含微孔、介孔和大孔,以介孔为主。测试结果表明,S4的BET比表面积高达95 m2/g。该数值高于Sung等[12]制备的γ-MnO2海胆和α-MnO2纳米线的比表面积,与Xu等[13]制备的α-MnO2空心球和空心海胆的比表面积相当。高的比表面积为电子和离子的有效传输提供了可能性,从而使材料可能具有高的电化学容量。
为了评价制备的空心海胆MnO2的电化学性能,组装MnO2/Li半电池并对其进行充放电测试。当电流密度为0.1 A/g时,S4电极前三次充放电曲线如图5所示。第一次充放电循环中,在约0.4 V处出现了宽的放电平台,该平台对应LixMnO2还原为Mn。第二和第三次放电平台重合且较第一次放电平台略有升高。三条充电曲线上的电压平台一致,在1.3 V和2.2 V左右,表明Mn的氧化分两步进行[14]。由图5还可以看出,首次放电容量和充电容量相差较大,这与MnO2和Li之间的不可逆转化反应(导致Li损失)以及电解质分解有关。
在0.01~3.0 V的电势窗口中,电流密度为0.1 A/g的条件下,对空心海胆MnO2的循环稳定性进行测试,结果如图6所示。首次放电比容量高达1318.8 mAh/g,充电比容量为897.1 mAh/g,库伦效率为68%。首次放电比容量高于MnO2的理论比容量(1232 mAh/g),这归因于电化学反应过程中固体电解质膜的生成、失水和界面储能等[15]。第二次放电比容量为946.7 mAh/g,充电比容量为904.6 mAh/g,库伦效率达到96%。由图6可见,放电比容量曲线比较平坦。随着充放电次数的增加,比容量缓慢减小。循环至140圈时,比容量稳定在701.8 mAh/g,容量保持率为74%(与第二圈相比),平均1次充放电容量损失不到2 mAh/g。该循环性能优于Nithyadharseni等[16]采用熔盐法制备的MnO2的循环稳定性。库伦效率曲线几乎与横坐标平行,随着循环圈数的增加库伦效率保持在98%以上。
图7给出了不同电流密度下空心海胆MnO2的倍率性能曲线。随着电流密度的成倍增大,放电比容量平稳降低,这表明在不同电流密度下电化学反应稳定进行。在电流密度为0.1 A/g、0.2 A/g、0.4 A/g和0.8 A/g的条件下,比容量分别约为925 mAh/g、634 mAh/g、370 mAh/g和225 mAh/g。当电流密度由0.8 A/g变为0.1 A/g时,比容量仍可以达到886 mAh/g,这表明空心海胆MnO2电极材料能承受大电流冲击,具有良好的结构和电化学稳定性。该倍率性能与Zhang等[17]采用硬模板法制备的棉絮状δ-MnO2的倍率性能相当,优于无模板时制备的α-MnO2的倍率性能,较好的倍率性能与MnO2材料具有的空心海胆状形貌和高的比表面积密切相关。
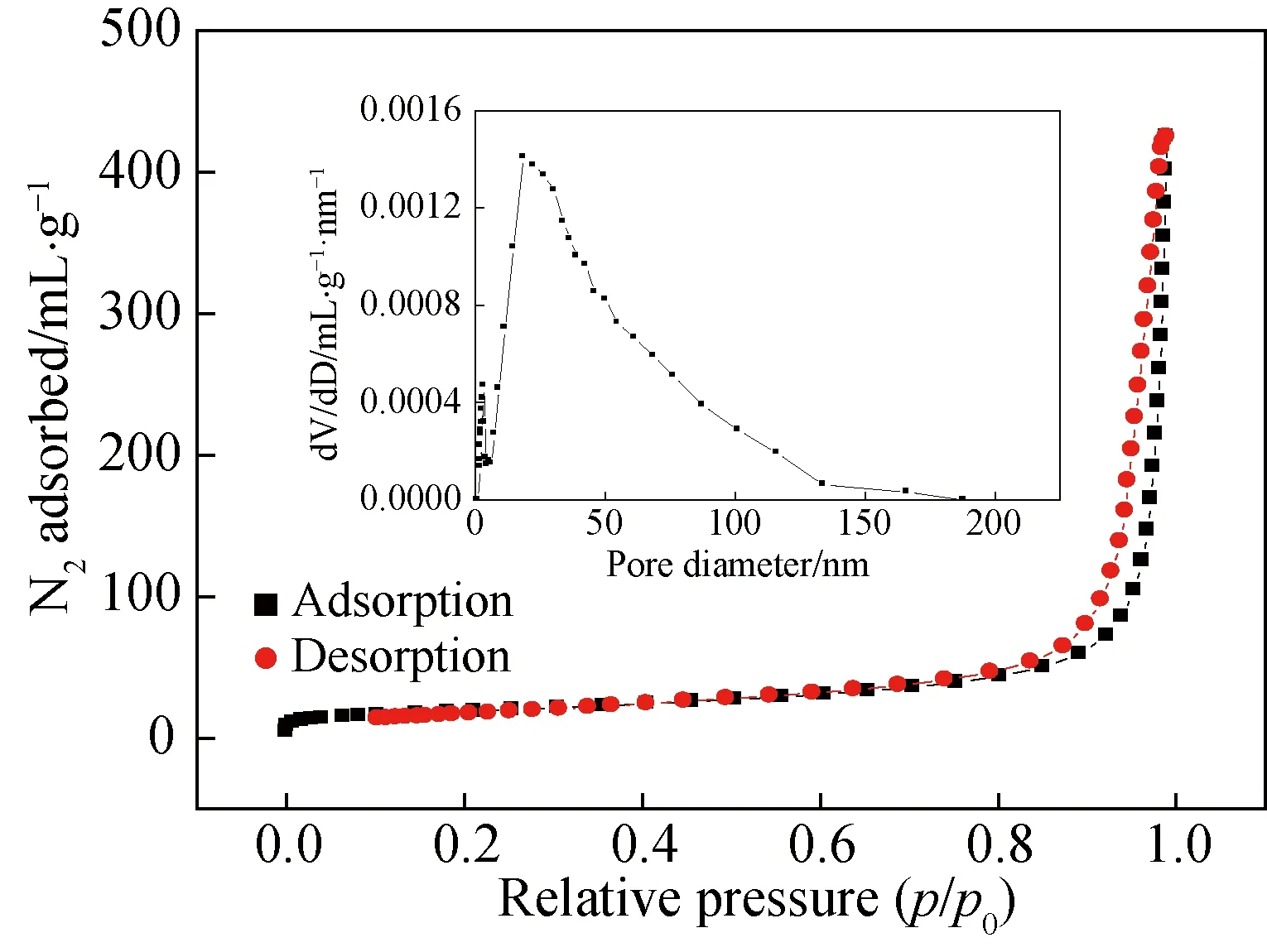
图4 S4的氮气吸-脱附等温线Fig.4 N2 adsorption-desorption isotherms of S4
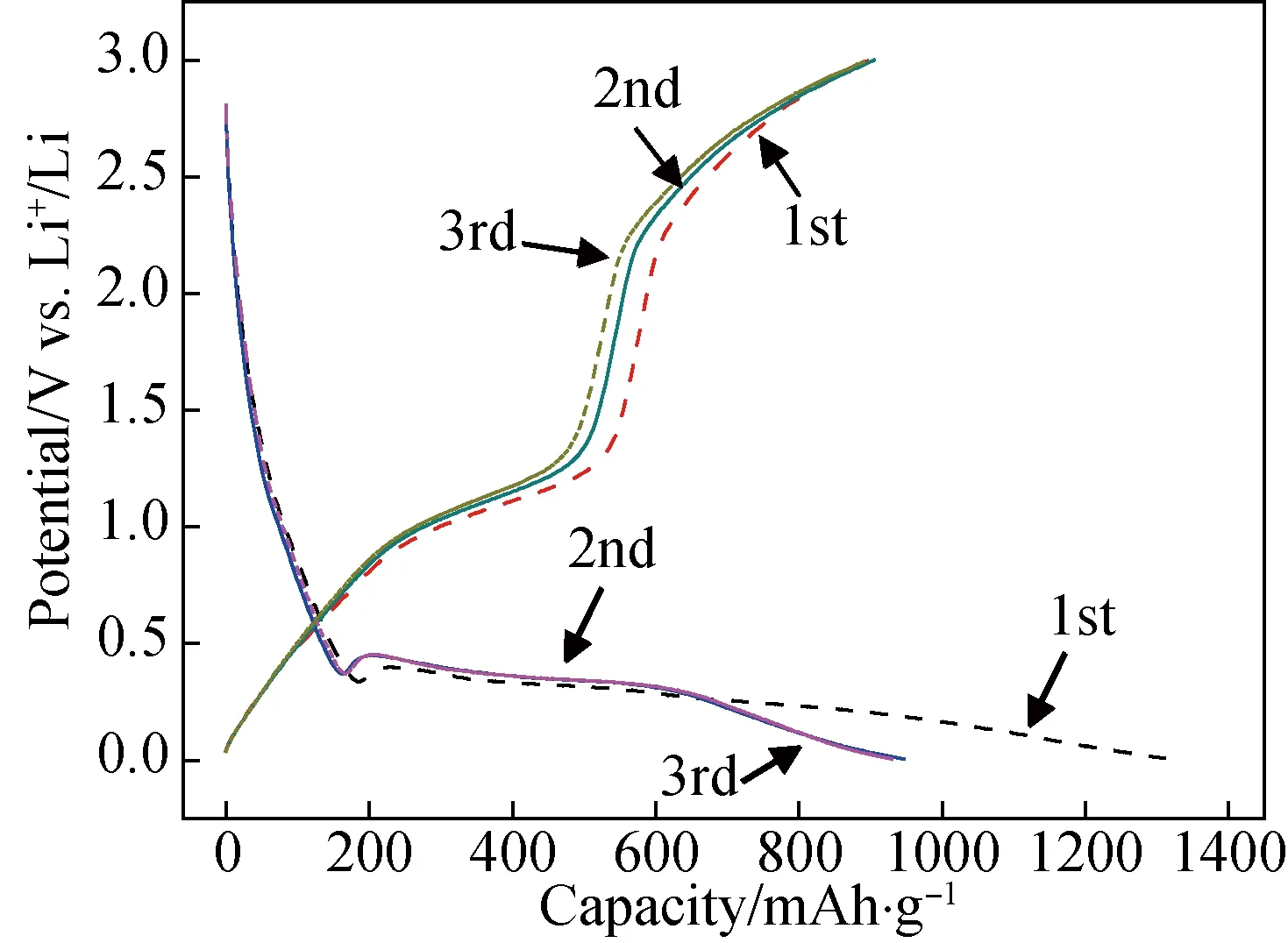
图5 S4电极的前三次充放电曲线Fig.5 The discharge-charge curves for initial 3 cycles of S4
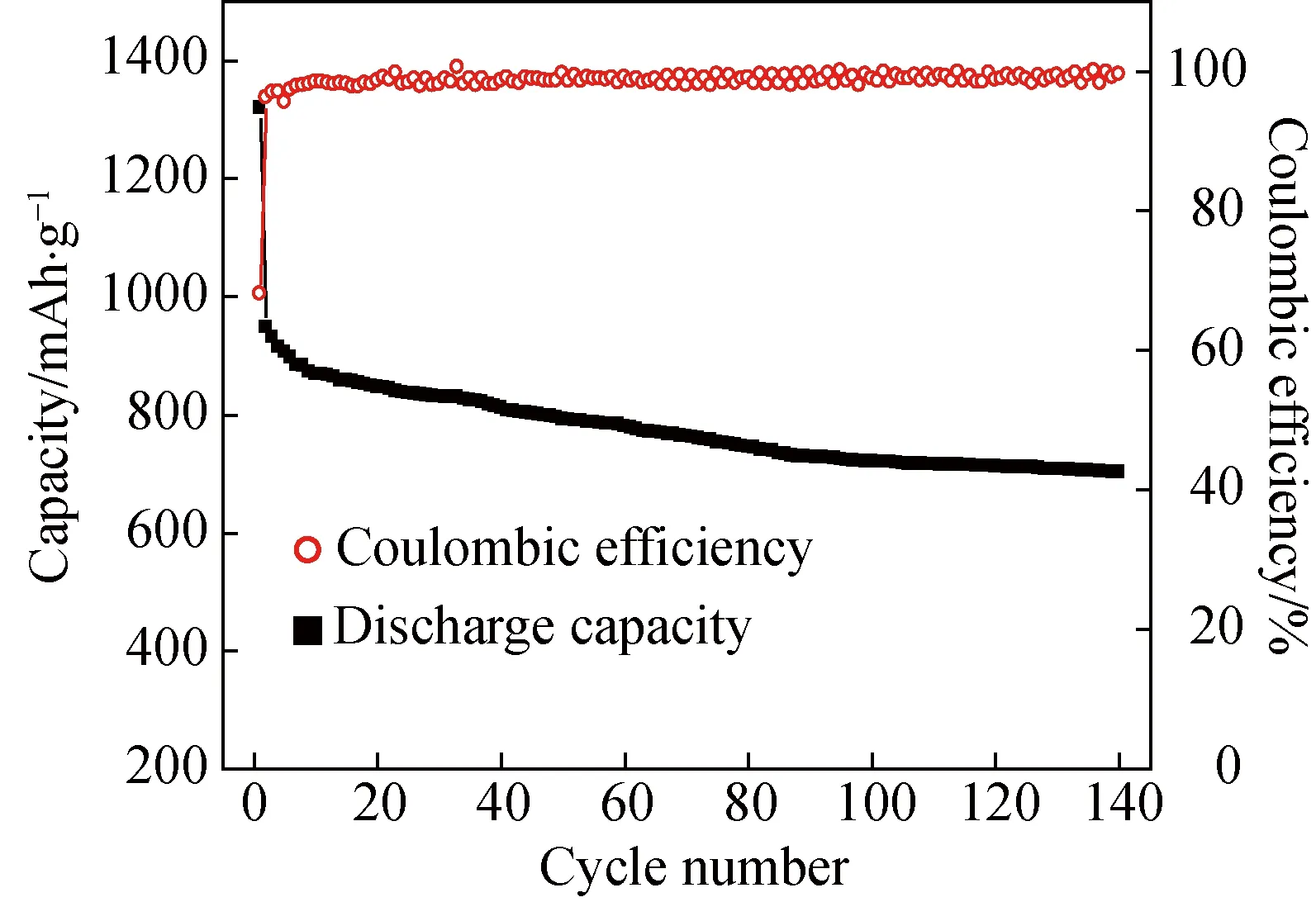
图6 S4电极的循环性能曲线Fig.6 Cycling performance curves of S4

图7 S4电极的倍率性能曲线Fig.7 Rate capability profiles of S4
4 结 论
基于KMnO4和CO(NH2)2之间的氧化还原反应,采用中温水热合成技术可控制备了颗粒状、球形、纤维状和海胆状MnO2。体系酸度是决定产物晶相、形貌和维度的关键因素。空心海胆状MnO2的比表面积高达95 m2/g。MnO2空心海胆具有高的比容量、良好的稳定性能和倍率性能,是一种潜在的锂离子二次电池电极材料,也有望用于超级电容器和钠离子电池。

