化学平衡模型的建立

摘 要:化学平衡是高中课本选修四的重点内容,也是高考的必考内容。对于初学者来说,要靠逻辑思维的想象能力;对想象能力稍微欠缺的同学来说,学起来比较吃力,理解较为困难。通过多年的教学发现利用生活中的一个例子解决这个问题,可以达到事半功倍的效果,使复杂问题简单化。
关键词:化学平衡;正反应;逆反应;化学反应速率
一、化学平衡的建立
1.化学平衡的定义:就是指在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应混合物中各组分的浓度保持不变的状态。
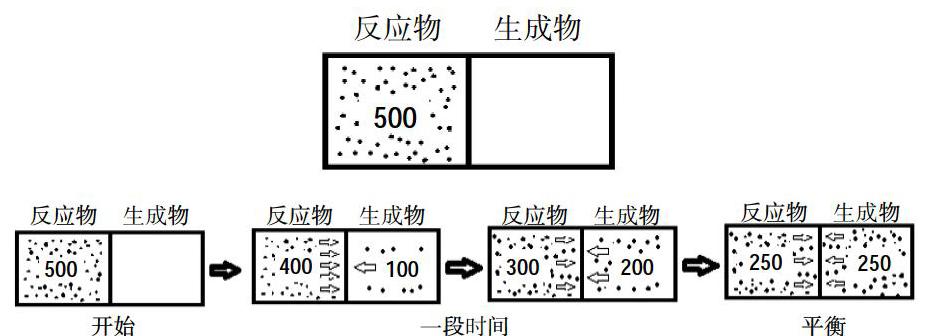
建立如下模型:
在一个长方形的密闭容器中间加一个隔板,在左边放入500只蜜蜂,充当反应物,当隔板去掉时,蜜蜂就向右边飞,相当于反应开始。
2.化学反应速率的表示方法:用单位时间内反应物浓度的减少或生成物的浓度增加来表示。
模型中,我们用左边蜜蜂的减少、右边蜜蜂的增加来表示,把蜜蜂向右边飞行称为正反应,向左边飞行称为逆反应,单位时间内飞行的数量称为反应速率。开始时向右边飞行的蜜蜂最多,即正反应速率最大,而向回返的蜜蜂最少,即逆反应速率最小,随着时间的推移,向右边飞的逐渐减少,即正反应速率逐渐减小,而向回返的蜜蜂逐渐增多,即逆反应速率逐渐增大。
3.化学平衡:随着时间进行,左边蜜蜂逐渐减少,右边蜜蜂逐渐增多,向右边飞行蜜蜂也逐渐减少,向左边飞行蜜蜂逐渐增多,在化学反应上,反应物浓度逐渐减少,生成物浓度逐渐增多,正反应速率逐渐减小,而逆反应速率逐渐增大。等两边的蜜蜂各有250只时,左右飞行的蜜蜂数量相等,且数量维持不变时即正反应速率和逆反应速率相等,两边的数量也不再随时间发生变化,即各组分的浓度保持不变,达到平衡状态。
二、化学平衡的特征
1.逆:可逆反应,是指在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。在本模型中,蜜蜂在相同的条件下可以向左飞行,也可以向右飞行。也就是反应物可以变成生成物,生成物也可变作反应物。
2.等:正反应速率等于逆反应速率,但不等于零。在本模型中,向右飞行的蜜蜂和向左飞行的蜜蜂数量相等,且一直在飞,即正逆反应速率相等。
3.动:动态平衡,即平衡后,蜜蜂仍然在飞行。
4.定:反应混合物中各组分的浓度保持不变,各组分的含量一定。在本模型中,左右两边蜜蜂的数量不再改变,即反应物浓度不再随时间改变。
5.变:条件改变,原平衡被破坏,在新的条件下建立新的平衡。即平衡会发生移动,下面展开集中分析。
三、外界条件对化学平衡的影响
化学平衡移动:当一个可逆反应达到平衡后,如果改变浓度、温度、压强等反应条件,原来的平衡状态会被破坏,化学平衡会发生移动,在一段时间后达到新的平衡。
1.浓度对平衡的影响。
在达到平衡后,我们再向左边放入100只蜜蜂,左边的蜜蜂数量突然增多,相当于增大反应物浓度。此时,向右边飞行的蜜蜂也突然增多,相当于正反应速率突然增大,而逆反应速率在这一瞬间没有变化,紧接着向右飞的逐渐减少,向左飞的在原来的基础上逐渐增大,最终相等。相当于增大反应物浓度,正反应速率突然增大后,慢慢减小,而逆反应速率在原来的基础上慢慢增大,直至相等,整体来说,正反应速率大于逆反应速率,平衡向正反应方向移动。由于整体的蜜蜂数量增多,左右飞行的蜜蜂比原来要多,相当于平衡后的反应速率比上次平衡的要大。这完全符合下面图像。
若将右边蜜蜂取出100只,相当于减小生成物浓度,完全可以用上述模型来解决。
等效平衡:如果从右边放入蜜蜂,和左边放入达到平衡的效果是一样的。或者,一边放100只,另一边放400只,也是一样的,即:等效平衡。
2.催化剂对平衡的影响。
可以采取增加蜜蜂的体能,如兴奋剂,可以解释反应速率加快但平衡不移动的原因。
3.如果只给一边加热或者将中间的隔板移动,则可以解释,平衡后各物质的浓度不一定相等,也不一定成一定比例。
4.若给蜜蜂中混入苍蝇,飞行碰撞忽略不计则可以解释加入惰性气体对平衡的影响。
这是我对化学平衡的一点肤浅理解,不妥之处,请批评指正。
作者简介:李明发(1979—),男,漢,甘肃合水,本科,一级教师,研究方向:中学化学。

