基于代谢组学技术分析磷酸三苯酯诱导斑马鱼胚胎发育毒性的分子机制
张杏丽,邹威,周启星
1. 河南师范大学环境学院,黄淮水环境与污染防治教育部重点实验室,河南省环境污染控制重点实验室,新乡453007 2. 南开大学环境科学与工程学院,环境污染过程与基准教育部重点实验室,天津市城市生态环境修复与污染防治重点实验室,天津 300071
随着各国对溴代阻燃剂环境效应的关注以及欧洲对五溴联苯醚和八溴联苯醚的禁用,有机磷阻燃剂(organophosphate flame retardants, OPFRs)作为理想替代品其使用量快速上升。OPFRs除了具有良好的阻燃效果外,兼有增塑和润滑的功效,广泛应用于建材、纺织、化工、塑料及电子等行业[1]。大多数OPFRs主要以物理添加方式而非化学键合成方式加入到材料中,在产品生命周期中极易从材料中泄露或者挥发进入周围环境。研究表明,OPFRs已广泛分布于各种环境介质,包括水环境、大气环境、土壤/沉积物及生物体内[2-6]。人体样本如尿液、血浆、头发、指甲和母乳中也检测出OPFRs[7-10]。我们之前的研究表明,由于污水灌溉,湖北、重庆、四川和广西地区采集的大米样品中均检测出OPFRs,其中受测的6种OPFRs总含量为0.38~287 ng·g-1,平均含量为69.9 ng·g-1[11];另外乳制品、饮料、肉类和蔬菜中也检测到OPFRs[11-12]。OPFRs已经成为一类新型有机污染物在全球范围内普遍存在。
磷酸三苯酯(triphenyl phosphate, TPhP)是一类生产量和检出频率较高的OPFRs,广泛应用于聚氯乙烯材料、印刷电路板以及商业混合阻燃剂如FM550阻燃剂和AC073阻燃剂中。在我国华北地区,95%的河流水样中检出TPhP,最高浓度为15.7 ng·L-1[13]。松花江水体中TPhP浓度为4.5~65 ng·L-1[14]。广州、贵屿、哈尔滨、西安、厦门、南京、成都和北京8个城市饮用水(自来水和瓶装水)中总OPFRs浓度为85.1~325 ng·L-1,TPhP是检出率较高的OPFRs[15]。TPhP已经被证实具有生殖毒性、发育毒性、内分泌干扰效应和神经毒性[16-19]。例如,Li等[20]发现TPhP暴露影响了日本青鳉鱼精巢发育进而破坏了其生殖能力。Hong等[21]发现TPhP穿过血脑屏障进入中国成年雄性稀有鲦鱼头部引起神经毒性,通过破坏紧密连接复合体损坏血脑屏障的完整性,通过激活炎症反应因子抑制中枢神经区细胞增殖和神经树突的密度,最终破坏鱼的学习和记忆能力。Isales等[22]发现TPhP通过与视黄酸受体相互作用影响斑马鱼生长发育。TPhP在水环境中存在浓度为几ng·L-1到几百ng·L-1,目前,仍缺乏环境当量浓度下TPhP的毒理数据资料及详细的致毒机理。
代谢组学是继基因组学和蛋白组学后新发展起来的一门学科,通过研究生物体内源性代谢物的整体变化,灵敏地指示和确证外来干扰物在组织和器官水平的毒性效应,某种特定代谢物的蓄积可能标志着某通路的缺陷或某信号响应的激活,而代谢物的动态变化可以作为毒性损伤的标志物,因此,代谢组学技术在回答低浓度环境污染物对生物体响应机制中具有不可替代作用[23]。我们曾利用代谢组学技术发现,痕量氧化石墨烯通过抑制氨基酸代谢、降低非饱和脂肪酸与饱和脂肪酸的比值引起斑马鱼胚胎发育畸形[24]。然而,有关环境当量浓度TPhP对生物体代谢组学的影响研究尚未见报道。
鉴于此,本研究以斑马鱼为模式生物,采用基于气相色谱-质谱联用仪(GC-MS)的代谢组学技术,探讨环境当量浓度(0.0025~1 μg·L-1)和高于环境浓度(10、100和1 000 μg·L-1)TPhP暴露对斑马鱼整体代谢组学的扰乱程度,筛选对TPhP毒性敏感的目标代谢物,同时将变化的代谢物与斑马鱼胚胎生长发育毒性指标相结合,从代谢物水平阐述TPhP诱发斑马鱼发育毒性的分子机制,为今后详细阐述TPhP生物毒性机制提供新思路和技术支撑。
1 材料与方法(Materials and methods)
1.1 斑马鱼胚胎的获得与培养
6个月龄的成年野生型斑马鱼(Daniorerio),购自国家斑马鱼资源中心(China Zebrafish Resource Center, CZRC)。斑马鱼养殖于装有控温装置的鱼缸中,养殖水为海盐浓度为60 mg·L-1的人工海水,温度保持(28.5±1) ℃,光周期为14 h光照/10 h黑暗,鱼缸中养殖水在循环过程中采用过滤系统进行过滤以保持水体清洁。饵料为丰年虾,每日早晚各喂1次。挑选个体大小相同雌雄斑马鱼于前一天晚上按照雌雄比例1∶1放入产卵盒中,用隔板隔开,将产卵盒放入人工气候培养箱中(中国博讯SPX-300I-C)。次日早上8:00将产卵盒中隔板取出,使雌雄斑马鱼自然交配,1 h后,收集鱼卵,得到斑马鱼胚胎。胚胎用斑马鱼胚胎培养液E3溶液(5 mmol·L-1NaCl,0.17 mmol·L-1KCl,0.33 mmol·L-1CaCl2,0.33 mmol·L-1MgSO4,pH=7.4)清洗干净去除排泄物和死卵。然后将健康斑马鱼胚胎转移到E3溶液中,置于人工气候培养箱中培养至2.5 hpf (hours post fertilization),用于后续实验研究。
1.2 TPhP暴露实验
TPhP标准品(CAS号115-86-6,纯度99.5%)购自上海百灵威科技有限公司,标准品用二甲基亚砜(DMSO,色谱纯,德国Merck)配制成浓度为10 mg·L-1的储备液,置于4 ℃冰箱中避光保存。然后用E3溶液将上述TPhP储备液稀释成1 000、100、10、1、0.1和0.0025 μg·L-1梯度浓度染毒溶液,染毒体系中DMSO终浓度为0.01%(体积比)。将2.5 hpf斑马鱼胚胎暴露于E3溶液(空白对照组,CK),0.0025、0.1、1、10、100和1 000 μg·L-1TPhP溶液中7 d。暴露实验在96孔板中进行,每孔一枚受精卵。每隔24 h更换一次染毒溶液以保证TPhP染毒浓度恒定不变,整个胚胎染毒实验均在人工气候培养箱中进行,培养箱温度为(28±1) ℃,光照周期为光暗比14 h/10 h。
1.3 斑马鱼心跳、孵化、死亡和畸形观察
每个浓度取120尾2.5 hpf斑马鱼胚胎于96孔板中进行7 d的暴露实验,设置3个生物重复,即每组包含40尾斑马鱼胚胎。体视镜(日本,Olympus ZL 61)下观察记录72 hpf斑马鱼胚胎的孵化情况,以幼鱼脱离绒毛膜作为成功孵化的标准。同时每组随机取出发育至72 hpf的斑马鱼胚胎6尾,在倒置显微镜(日本,Olympus X71)下连续观察1 min,记录斑马鱼胚胎的心跳次数。每天在体视显微镜下(日本,Olympus ZL 61)观察40尾斑马鱼幼鱼的畸形和死亡情况,以不运动、无心跳和血液不流动作为胚胎死亡的标准,胚胎畸形按照心包/卵黄囊水肿、尾/脊椎弯曲和面部畸形等标准进行判断,并对畸形的斑马鱼进行拍照,最终统计各组发育至7 dpf(days post fertilization)的斑马鱼幼鱼的死亡率和畸形率。
1.4 斑马鱼幼鱼线粒体膜电位分析
JC-1是检测线粒体膜电位的理想荧光探针,JC-1红色荧光到绿色荧光的转变显示线粒体膜电位下降。每个浓度取36尾发育至2.5 hpf斑马鱼胚胎于96孔板中暴露7 d,设置3个生物重复,即每组包含12尾斑马鱼。暴露结束后,每组随机取出6尾斑马鱼幼鱼,E3冲洗干净后,在含6 μmol·L-1JC-1的E3溶液中避光孵育1 h。染色结束后,用新鲜E3溶液冲洗数次,斑马鱼在0.08%三卡因(质量比)中麻醉后,在倒置荧光显微镜(日本,Olympus X71)下观察拍照,激发波长和发射波长分别为485 nm和535 nm。利用Image J软件对斑马鱼体内荧光强度进行定量分析。
1.5 斑马鱼幼鱼的GC-MS代谢组学分析
斑马鱼体内代谢物分析方法参考我们之前文献进行[24]。具体步骤如下;每个浓度取144尾2.5 hpf斑马鱼胚胎于96孔板中进行7 d的暴露实验,设置3个生物重复,即每组包含48尾斑马鱼胚胎。暴露结束,每组随机取30尾斑马鱼幼鱼,迅速放入液氮中冷冻合并为一个样品,之后每个样品均加入2 mL提前保存于-20 ℃的甲醇/氯仿/水混合提取液(体积比为2.5∶1∶1),在研钵中冰浴研磨成匀浆。微波萃取20 min,萃取温度40 ℃。萃取液转移到灭菌的1.5 mL离心管中,4 ℃高速离心10 min,转移上清液到10 mL离心管中,沉淀中再次加入1 mL混合提取液,同等条件下微波萃取,离心,合并2次上清液到10 mL离心管中。加入500 μL灭菌后的高纯水到离心管样品中,离心后得到分层的样品溶液,上层是甲醇/水相提取物,下层是氯仿提取物,先氮吹,然后冷冻干燥。将干燥得到的提取物连同离心管进行封口密封,置于-80 ℃低温冰柜中保存。
代谢物的GC-MS(美国,Agilent 6890A/5977A)测定采用两步衍生化法。首先加入50 μL用吡啶溶解的甲氧氨基盐酸盐,密封,涡旋振荡,30 ℃水浴孵育90 min,再加入80 μL硅烷化试剂N-甲基-N-(三甲基硅烷)-三氟乙酰胺(MSTFA),37 ℃水浴孵育30 min。转移衍生化好的样品到样品瓶中。
气相色谱参数:MDN-35毛细管色谱柱(30 m),升温程序为80 ℃,保留2 min,然后以15 ℃·min-1的速率升温到325 ℃,保留6 min,传输线温度为250 ℃。气相色谱进样参数:进样量为1 μL,进样口温度设置为230 ℃,不分流进样模式,载气为氦气,流速2 mL·min-1,进样模式为自动进样。质谱参数:离子源温度为250 ℃,质量扫描范围是m/z 70~600,采集速率每秒20个scan,溶剂延迟170 s,检测器电压1 700~1 850 V,质谱亏损设置为0,灯丝偏置电流为70 V,仪器进行自动调谐。谱图解卷积参数:力可公司自带的商业软件Chroma TOF,基线消除设置为1(0.5~1),谱图平滑(smoothing)为5数据点(3~7),峰宽(peak width)3 s(3~4 s),信噪比S/N(signal-tonoise ratio)为10(2~15)。数据采集以scan模式获得总离子流色谱图(TIC),利用NIST 14数据库对代谢物进行定性分析,生成包含样本信息、化合物名称、保留时间、峰面积和定性值等信息的文件。根据保留时间和定性值筛选代谢物,以峰面积表示代谢物的相对含量。
1.6 数据处理
所有的实验组均设置3个生物重复,结果用平均值±标准偏差表示。所得实验数据使用SPSS 20.0统计软件进行单因素方差(ANOVA)分析,当P<0.05时,认为在统计学上具有显著性。代谢物热图利用软件MeV 4.9绘制。同时将筛选出的代谢物数据导入SIMCA-P13.0(瑞典,Umetrics AB,Umea)软件包进行多元统计分析,数据先用无监督统计模型主成分分析(principal components analysis, PCA),得出对照组和处理组之间代谢物的离散趋势。再进行有监督统计模型的正交最小二乘法判别分析(orthogonal partial least squares discriminate analysis, OPLS-DA)[25-26],将差异代谢物与斑马鱼的畸形率建立相关性,选择定义变量权重重要性排序(variable importance in projection, VIP)大于1的变量进行研究。最后,用MetaboAnalyst 3.0数据库对差异倍数在1.5倍的代谢物进行通路定位,找出显著富集的代谢通路[27]。
2 结果(Results)
2.1 斑马鱼胚胎发育分析
如图1a所示,空白对照组斑马鱼72 hpf孵化率达96%,当TPhP浓度为0.0025~10 μg·L-1时,斑马鱼胚胎孵化率与空白对照组无显著差异,当TPhP浓度为100和1 000 μg·L-1时,胚胎孵化率分别为73.3%和46.7%,显著低于对照组(P<0.05)。当TPhP浓度为10、100和1 000 μg·L-1时,斑马鱼72 hpf心率明显低于空白对照组(图1b)。TPhP浓度为100和1 000 μg·L-1,斑马鱼幼鱼7 d的死亡率分别为18.2%和38.9%,畸形率分别为18.0%和31.1%,显著高于空白对照组(图1c和图1d)。畸形类型包括脊柱弯曲、尾巴弯曲、卵黄囊肿、心包囊肿,其中脊柱、尾巴弯曲和心包囊肿出现的频率显著大于其他畸形类型,TPhP浓度越大,心包囊肿出现频率越大,表明TPhP显著影响斑马鱼的心脏发育。
2.2 线粒体膜电位分析
对暴露7 d的斑马鱼幼鱼进行JC-1染色,倒置荧光显微镜下观察发现,空白对照组红色荧光较多(图2a),高浓度TPhP处理组斑马鱼体内绿色荧光较多(图2b)。当TPhP浓度为100和1 000 μg·L-1时,红色和绿色相对荧光强度比值明显低于空白对照组(图2c),当TPhP浓度为0.0025~10 μg·L-1时,差异不显著。结果表明,当TPhP浓度≥100 μg·L-1,斑马鱼幼鱼线粒体膜电位下降,TPhP诱导斑马鱼线粒体损伤。
2.3 斑马鱼幼鱼代谢组学分析
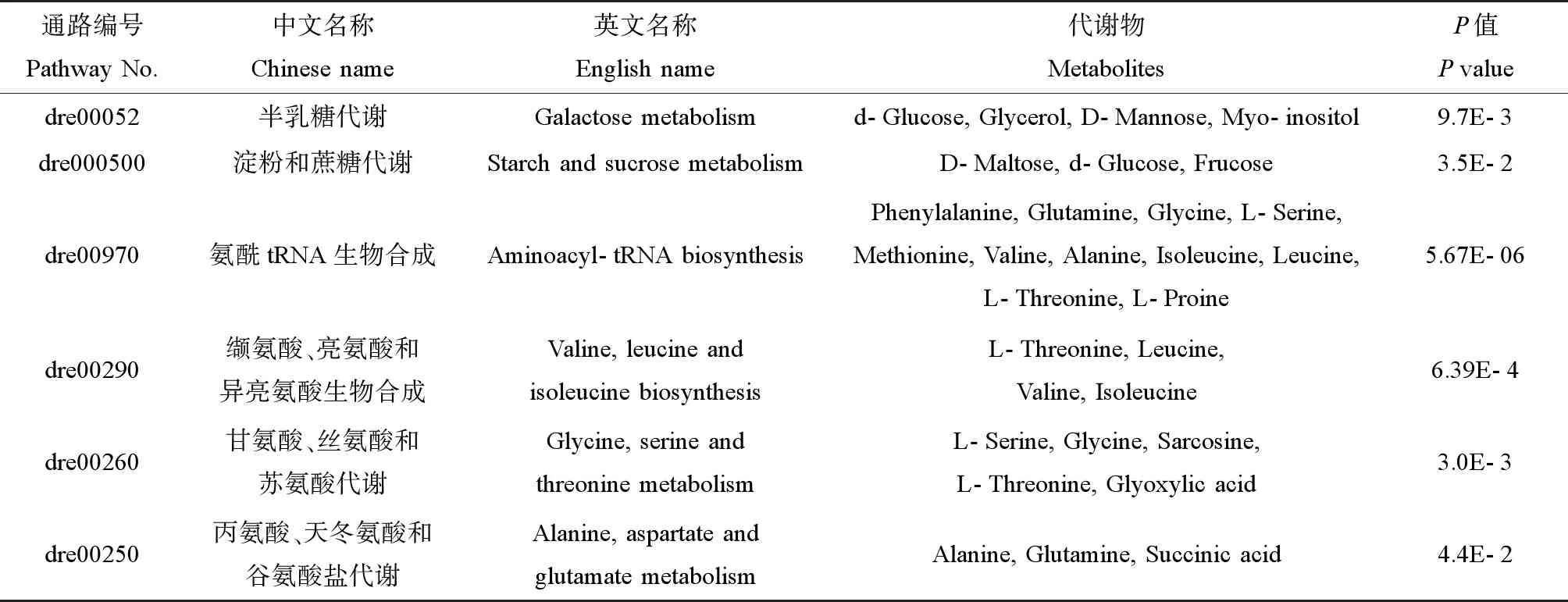
空白对照组和TPhP处理组斑马鱼幼鱼代谢组学分析结果如表1和图3所示。样本经甲醇/氯仿/水混合提取液提取,衍生化后进行GC-MS分析,共得出54种代谢物,主要包括碳水化合物、氨基酸、脂肪酸、其他小分子酸和胆固醇等。代谢物的相对水平通过热图展示(图3a),从代谢轮廓可以看出,随着TPhP浓度增高,大部分代谢物相对含量降低。层次聚类(HLC)分析发现,7个实验组可以分成3组,分别是空白对照组/0.0025 μg·L-1处理组/0.1 μg·L-1处理组,1 μg·L-1处理组/10 μg·L-1处理组/100 μg·L-1和1 000 μg·L-1处理组,表明当TPhP浓度≥1 μg·L-1时,影响斑马鱼幼鱼的代谢过程。通过SIMCA-P 13.0对代谢物进行PCA分析发现,空白对照组、0.0025与0.1 μg·L-1处理组聚集在一起,没有明显分开,而1、10、100和1 000 μg·L-14个处理组与空白对照组明显分开(图3b),表明这4个处理组中斑马鱼幼鱼代谢状况与空白对照组存在明显的差异,PCA分析进一步证实TPhP浓度在≥1 μg·L-1时干扰了斑马鱼幼鱼的代谢过程。
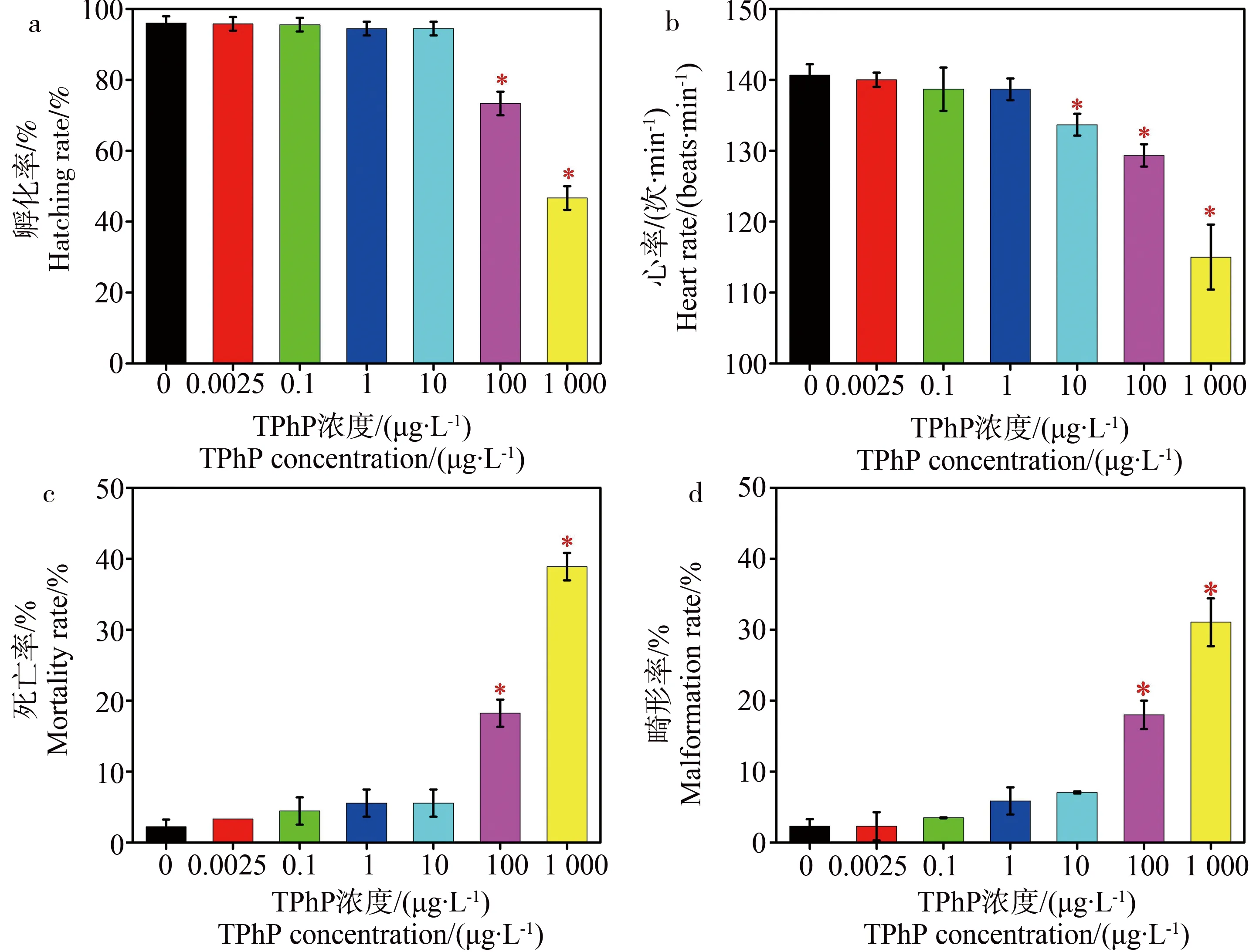
图1 磷酸三苯酯(TPhP)暴露对斑马鱼胚胎孵化率(a)、心率(b)、致死率(c)和畸形率(d)的影响注:* 表示处理组斑马鱼胚胎考察指标与对照组相比差异显著(P<0.05)。Fig. 1 Effects of triphenyl phosphate (TPhP) on the hatching (a), heart rate (b), mortality (c) and malformation (d) of zebrafish during embryogenesis Note: *denotes P<0.05, compared to the control.
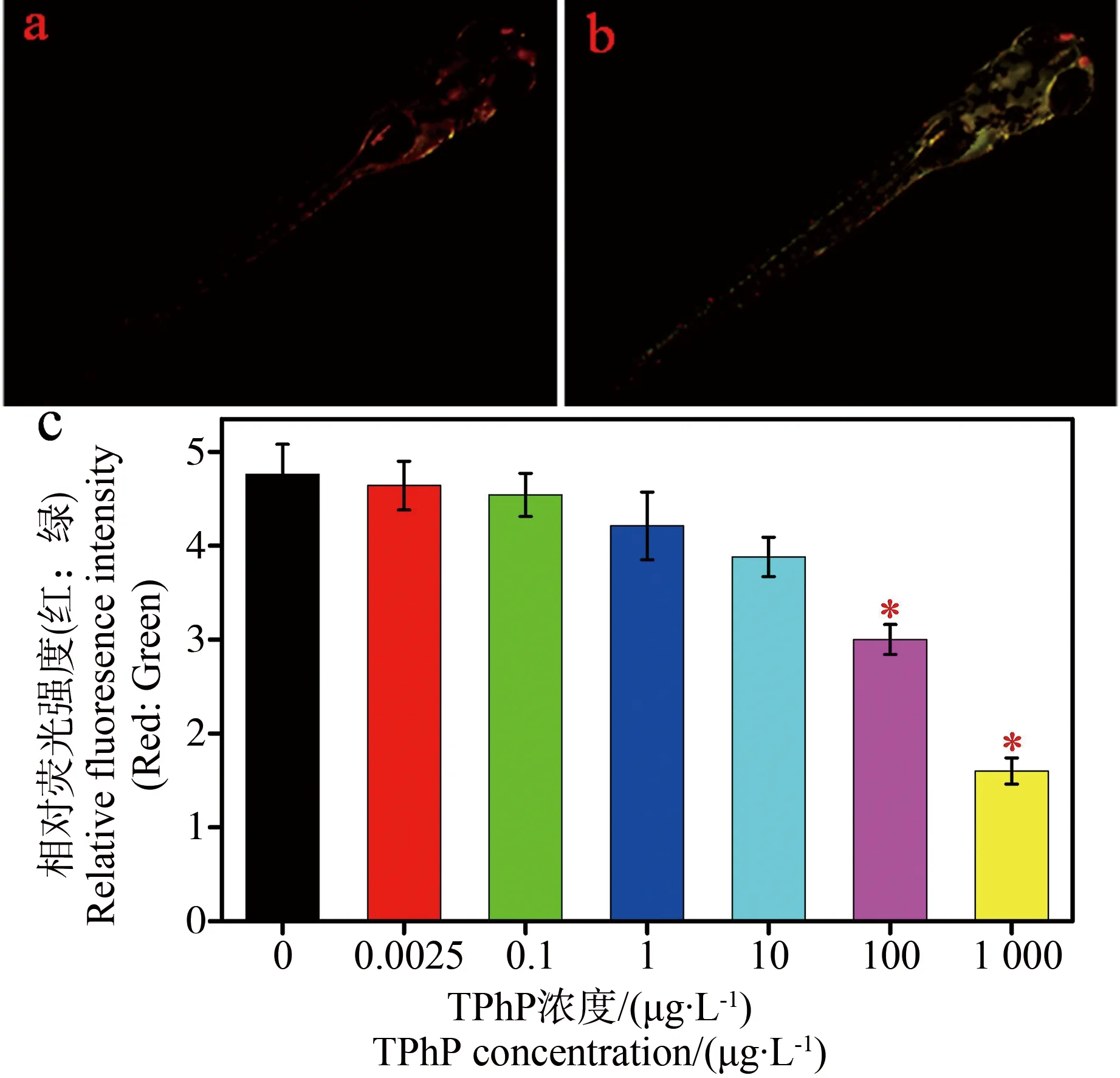
图2 TPhP对斑马鱼幼鱼线粒体膜电位的影响注:a,空白对照组;b, 1 000 μg·L-1 TPhP处理组; *表示处理组考察指标与对照组相比差异显著(P<0.05)。Fig. 2 Effects of TPhP on mitochondrial membrane potential in zebrafish larvae Note: a, zebrafish larvae in control; b, zebrafish larvae in 1 000 μg·L-1 TPhP group; *denotes P<0.05 compared to the control.
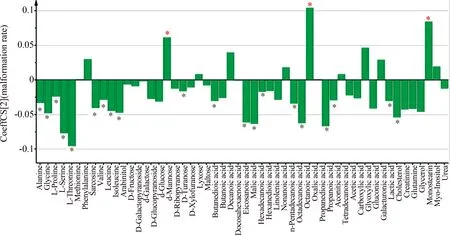
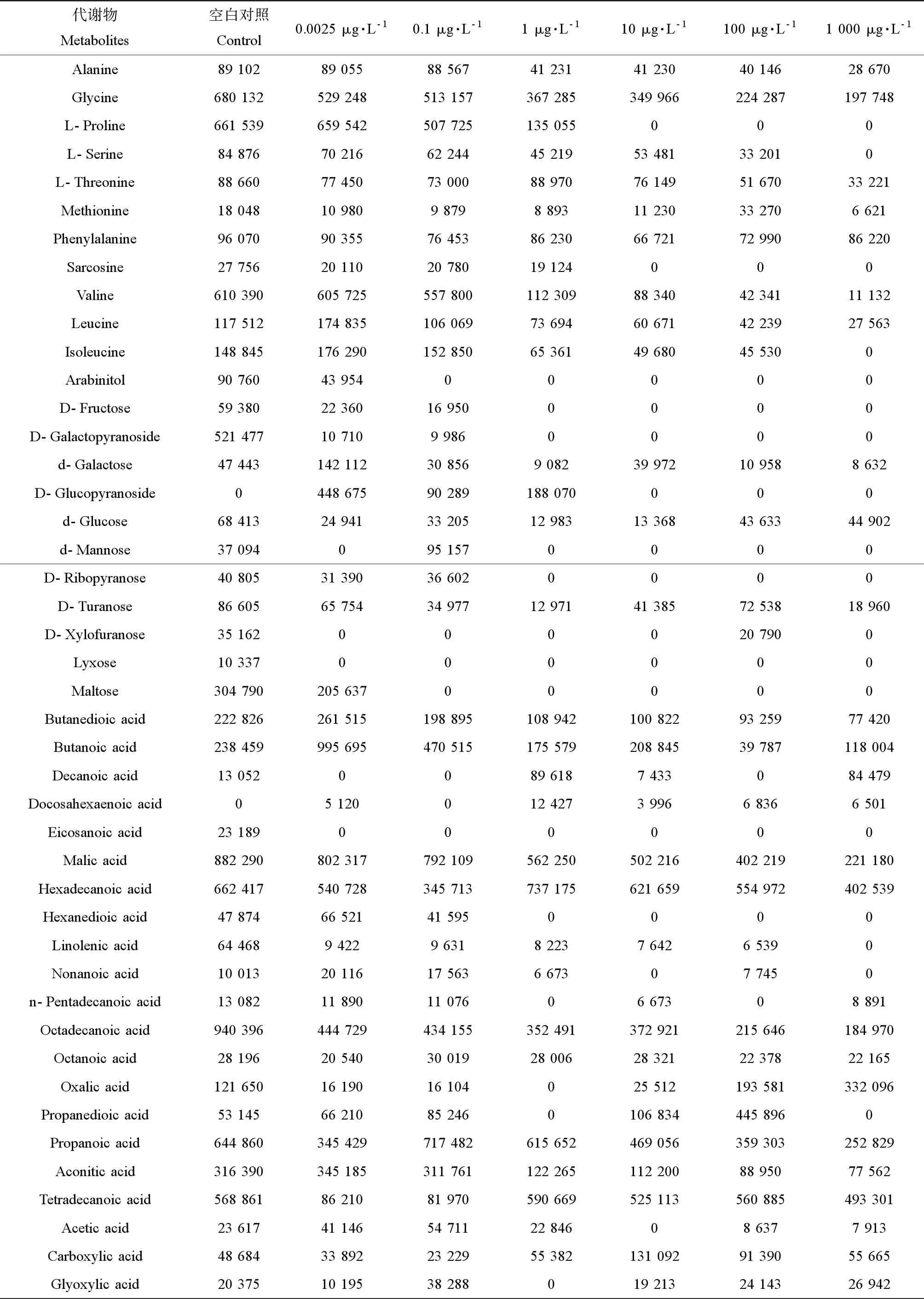
通过SPSS 2.0对TPhP处理组总代谢物、碳水化合物、氨基酸和脂肪酸含量与空白对照组含量进行显著性分析,结果如图4所示。当TPhP浓度为0.0025 μg·L-1时,总代谢物和各单类代谢物与空白对照组的差异水平P值接近1,表明0.0025 μg·L-1TPhP对斑马鱼代谢过程无显著影响。但是随着TPhP浓度增加,P值呈降低趋势,TPhP浓度越高,对斑马鱼幼鱼代谢过程影响越明显。当TPhP浓度为0.1~1 000 μg·L-1时,P碳水化合物 图3 代谢物层次聚类分析(a)和主成分分析(b)Fig. 3 Hierarchical clustering analysis (a) and principal component analysis (b) of metabolites 表1 不同处理组斑马鱼幼鱼体内代谢物的相对含量(a.u)Table 1 Metabolites of zebrafish larvae in different treatment groups (a.u) 为进一步确认与斑马鱼生长发育相关的代谢物的变化,本实验利用OPLS-DA进行差异代谢产物与畸形率相关性分析,Y变量是发育畸形率,X变量是代谢物,分析结果如图5。在54种代谢物中,12种代谢物与畸形率呈现正相关关系;其余42种代谢物与畸形率呈负相关关系。另外对代谢物进行了变量重要性投影,得到VIP>1的23种代谢物,在图5中用星号标出,OPLS-DA分析表明,TPhP胁迫下,此23种代谢物的变化与斑马鱼畸形相伴发生,代谢物的变化可能是TPhP引起斑马鱼胚胎畸形的分子机制。其中,与畸形率正相关且VIP>1的代谢物有3种,分别是甘油-硬脂酸酯(monostearin)、葡萄糖(d-glucose)和草酸(oxalic acid),表示这3种代谢物对畸形发生有显著的促进作用。与畸形率呈负相关且VIP>1的代谢物有18种,如胆固醇(cholesterol)、甘氨酸(glycine)、丝氨酸(L-serine)、亮氨酸(leucine)、异亮氨酸(isoleucine)、苏氨酸(L-threonine)、硬脂酸(octadecanoic acid)、辛酸(octanoic acid)和乳酸(lactic acid),表示这18种代谢物对畸形发生有显著的抑制作用。 进一步将差异代谢数据导入MetaboAnalyst 3.0进行代谢路径富集分析,结果如表2所示。TPhP显著影响斑马鱼胚胎发育过程的路径中,4条是与氨基酸相关的代谢通路,2条是与碳水化合物相关的代谢通路,其中对氨酰-tRNA生物合成通路,缬氨酸、亮氨酸和异亮氨酸代谢通路,甘氨酸、丝氨酸和苏氨酸代谢通路影响最显著,由表1可知,以上代谢通路中氨基酸水平在TPhP≥10 μg·L-1处理组均显著降低,表明TPhP抑制斑马鱼氨基酸代谢。 本实验将斑马鱼胚胎暴露于0.0025~1 000 μg·L-1的TPhP溶液7 d,结果发现,当TPhP浓度低于10 μg·L-1时,斑马鱼胚胎孵化率、心率、死亡率和畸形率与空白对照组相比无明显差异,表明低浓度TPhP对斑马鱼胚胎无显著毒性。当TPhP≥100 μg·L-1时,明显抑制了斑马鱼心跳速率和孵化率,增大斑马鱼胚胎的畸形率和死亡率。TPhP浓度为1 000 μg·L-1时,斑马鱼幼鱼死亡率为38.9%,这与之前报道的TPhP对斑马鱼胚胎的96 h半数致死浓度为1.53 mg·L-1大略一致[28]。中国科学院水生生物研究所周炳升教授团队研究发现,100 μg·L-1TPhP显著抑制斑马鱼心跳速率和游泳速度,引起斑马鱼胚胎发生明显的畸形[29]。 图4 TPhP处理组代谢物相对于空白对照组的显著性水平注:P值通过ANOVA方差分析中的Tukey’s检验获得。Fig. 4 Significance differences of comparing metabolites from TPhP exposed groups with the control Note: The significant level P at vertical axis is obtained by ANOVA with Tukey’s test. 图5 斑马鱼差异代谢物与畸形率的相关性分布图注:与斑马鱼畸形率成负相关且VIP值大于1的代谢物用黑色星号标出,与斑马鱼畸形率成正相关且VIP值大于1的代谢物用红色星号标出。Fig. 5 Relationships between differential metabolites and malformation rate of zebrafish Note: The metabolites labeled with red and black asterisks represent the metabolites with a VIP greater than one that positively and negatively contribute to the malformation rate, respectively. 表2 TPhP显著干扰的代谢通路Table 2 The metabolite pathways significantly disordered by TPhP 代谢组学研究发现,当TPhP浓度为0.1和1 μg·L-1时,轻微干扰斑马鱼代谢过程,此浓度对斑马鱼胚胎生长发育无影响,表明代谢物变化是污染物生物毒性研究中更加敏感的指标。当TPhP浓度为10、100和1 000 μg·L-1时显著干扰斑马鱼代谢过程,主要影响斑马鱼氨基酸代谢和碳水化合物代谢。KEGG通路分析表明,TPhP显著干扰斑马鱼氨酰-tRNA生物合成过程,该过程是将氨基酸合成为蛋白质的关键步骤,斑马鱼氨酰-tRNA生物合成过程受到干扰,会出现明显的脊柱弯曲和身体短小畸形[30],这2种畸形类型在TPhP≥100 μg·L-1的暴露组中出现频率均显著高于空白对照组。支链氨基酸(BCAAs)在生物体的骨骼肌肉发育和合成代谢过程中起关键作用,BCAA代谢受到影响将会对生物体身体产生危害[31-32]。本实验中,TPhP暴露组中斑马鱼体内3个重要BCAAs,缬氨酸(valine)、亮氨酸(leucine)和异亮氨酸(isoleucine)下调倍数为2~45倍(表1),OPLS-DA分析也表明,大多数下调的氨基酸与畸形发生有关(图5),因此,氨基酸代谢水平下调可能是TPhP引起斑马鱼畸形和死亡率升高的原因。葡萄糖是斑马鱼胚胎发育过程中主要能量来源,通过糖酵解生成乳酸来提供能量,本研究中TPhP暴露使斑马鱼体内葡萄糖含量升高和乳酸含量降低,表明TPhP引起斑马鱼体内糖酵解途径的紊乱。体内高含量葡萄糖会引起斑马鱼卵黄囊和头部畸形[33],由此可知,心包囊肿和卵黄囊肿畸形发生可能与体内糖代谢紊乱有关。同时,三羧酸循环的中间产物苹果酸(malic acid)、琥珀酸(butanedioic acid)和乌头酸(aconitic acid)含量在TPhP≥10 μg·L-1的3个处理组中均明显降低,表明三羧酸循环代谢通路发生障碍。斑马鱼线粒体膜电位分析表明,100和1 000 μg·L-1TPhP处理组斑马鱼幼鱼线粒体膜电位明显降低(图2),线粒体是斑马鱼进行三羧酸循环产生能量的场所,因此三羧酸循环发生障碍,可能与线粒体功能紊乱有关。 综上所述,环境当量浓度TPhP(<10 μg·L-1)对斑马鱼胚胎心跳、孵化、畸形和死亡无显著影响,但是轻微干扰了斑马鱼代谢过程,浓度大于10 μg·L-1TPhP显著引起斑马鱼胚胎心率、孵化率和线粒体膜电位的下降,引起胚胎死亡率和畸形率增加,同时显著干扰了斑马鱼的氨基酸代谢和糖代谢,降低支链氨基酸的含量,引起葡萄糖糖酵解过程和三羧酸循环代谢过程紊乱。代谢物的变化与生长发育毒性指标表现出很好的相关性,本文从内源代谢物角度阐述了TPhP引起斑马鱼胚胎发育毒性的分子机制,为今后深入开展TPhP水生生物毒性机制的研究提供新思路和技术支撑。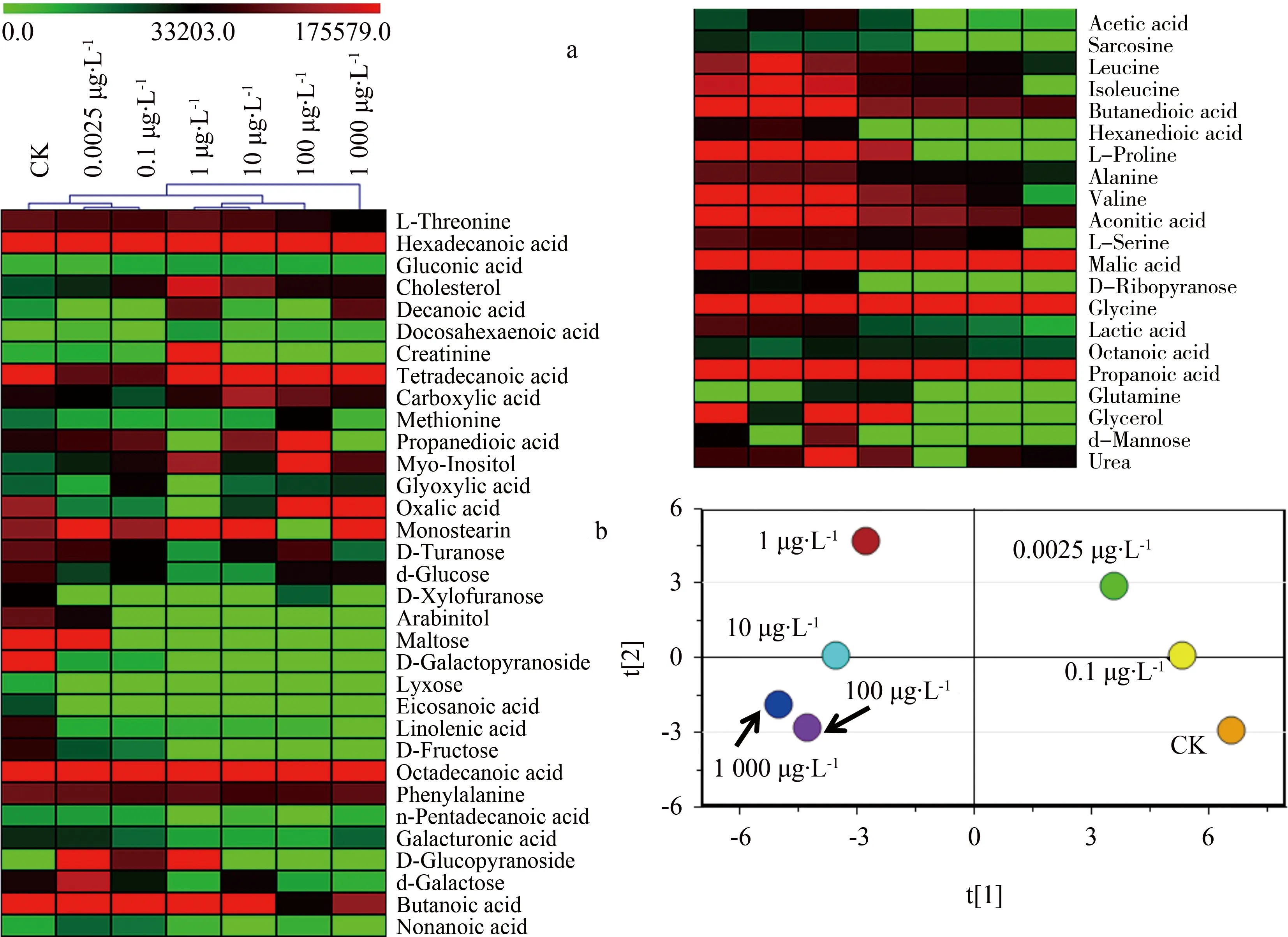
2.4 斑马鱼代谢成分的改变与发育毒性相关性分析
3 讨论(Discussion)