当归润肠膏的制备工艺和质量标准
牛婧娥,吴国泰,杜丽东,李 倩,史彦斌,*,任 远,*
(1.兰州大学药学院,甘肃兰州 730000; 2.甘肃中医药大学,甘肃省中药药理与毒理学重点实验室,甘肃兰州 730000)
当归润肠组方由当归、枳壳、干姜、大枣组成,具有养血温阳、润肠导滞的功能;主治血虚、寒凝、瘀滞之冷秘。课题组之前将其制成当归润肠茶,发现高剂量能显著缩短脾胃虚寒型便秘小鼠、慢传输型便秘小鼠、阴虚血瘀型模型小鼠的排便时间(p<0.05),并能显著增加脾胃虚寒型便秘小鼠、慢传输型便秘小鼠、阴虚血瘀型模型小鼠的排便量、粪便含水量和肠推进率(p<0.05)。按最高浓度最大给药容量灌胃后,当归润肠茶对小鼠未见明显急性毒性反应[1]。然而,当归润肠茶久置易出现浑浊,口感变差,质量不稳定。因此,尝试将其制成质量稳定的物理形态是本论文关注的核心内容。
煎膏剂是传统滋补型中药制备中的常用剂型。其服用口感好、体积小,渗透压高、不易发霉变质,适合长期服用及胃肠道不健全的病人,已成为保健食品的一种重要物理形态[2-8]。因此,将当归润肠方开发为煎膏剂(简称:当归润肠膏),稳定性应较茶剂有较大提升,市场前景更加乐观。
本论文拟以浸膏出膏得率、浸出物含量、多糖含量、阿魏酸含量为评价指标,采用三因素三水平L9(34)正交试验优选当归润肠膏的最佳提取工艺。通过炼蜜及煎膏剂的相对密度,确定清膏浓缩的程度,制备煎膏剂。通过影响因素和经典恒温法实验,考察其稳定性,以期为配方调整、贮存条件和保质期的制定提供理论参考。
1 材料与方法
1.1 材料与仪器
当归(RadixAngelicaeSinensis)、干姜(ZingibeaisRhizoma)、枳壳(AurantiiFrucrus)、大枣(JujubaeFructus) 甘肃陇西县百宝药业有限责任公司 均符合《中国药典》2015版I部对药材的质量要求;蜂蜜 甘肃景泰田金刚蜂业有限公司;阿魏酸对照品(批号:15121602)、齐墩果酸对照品(批号:wkq16051205)、6-姜酚对照品(批号:16081803)、新橙皮苷对照品(批号:wkq16041804) 四川省维克奇生物科技有限公司;葡萄糖 北京化学试剂工厂 分析纯;色谱甲醇 山东禹王实业有限公司 分析纯;娃哈哈纯净水 杭州娃哈哈集团有限公司;其他试剂 均为市售分析纯。
Bench Top6K型冻干机 美国VisTis公司;RE-52AA旋转蒸发器 上海亚荣生化仪器厂;UV-2501PC/2550紫外可见分光光度计 日本岛津;高效液相色谱仪系列 美国Waters公司;M-2-4可调式电热板 上海科恒实业发展有限公司;比重瓶 郑州赛克斯玻璃仪器有限公司;HH-2数显恒温水浴锅 国华电器有限公司;XK-80A快速混匀器 姜堰市新康医疗器械有限公司;TDL-5台式离心机 上海安亭科学仪器厂;NDJ/SNB数字显示粘度计 上海上天精密仪器有限公司;WD-A药物稳定性检查仪 天津药典标准仪器厂;101-2A型电热鼓风干燥箱 天津市泰斯特仪器有限公司;ZF-2型三用紫外仪 上海安亭电子仪器厂;玻璃点样毛细管 华西医科大学仪器厂;硅胶板 青岛海洋化工有限公司。
1.2 实验方法
1.2.1 提取工艺优化 取粉碎后过30目筛的药材当归、枳壳、干姜、大枣以处方量4∶1∶0.25∶4 (w/w)比例均匀混合。加入适量蒸馏水,采用热回流法进行提取。
1.2.1.1 单因素实验 参照中药和食材提取工艺的诸多文献[9-11],本实验以出膏得率为考察指标,分别对提取时间、提取次数及加水量3个因素进行了考察。固定提取次数为2次,提取时间为每次1.5 h的条件下考察加水量(水/药材,v/w)为4∶1、6∶1、8∶1、10∶1和12∶1对出膏得率的影响;固定加水量为8倍,提取时间为1.5 h,考察提取次数1、2、3、4和5次对出膏得率的影响;固定加水量为8倍,提取次数为2次,考察提取时间0.5、1.0、1.5、2.0和2.5 h对出膏得率的影响。
1.2.1.2 正交试验 根据单因素实验结果,确定提取时间、提取次数及加水量为影响因素,每个因素选择三个水平。考虑到随着提取的次数增多,滤渣中药物含量不断减少,为节约资源,基于前一次的提取条件,适当缩减后一次提取的加水量和提取时间,所以将加水量、提取时间设置3个递减值,采取梯度设计[12]。以出膏得率、浸出物含量、多糖量、阿魏酸含量的综合评分为评价指标,按三因素三水平L9(34)进行正交设计(表1),优选提取工艺。根据主成分权重系数大的原则,以阿魏酸含量为主(权重系数0.4),出膏得率、浸出物含量、多糖含量为辅(权重数依次为0.1、0.25、0.25),按公式(1)计算综合评分。
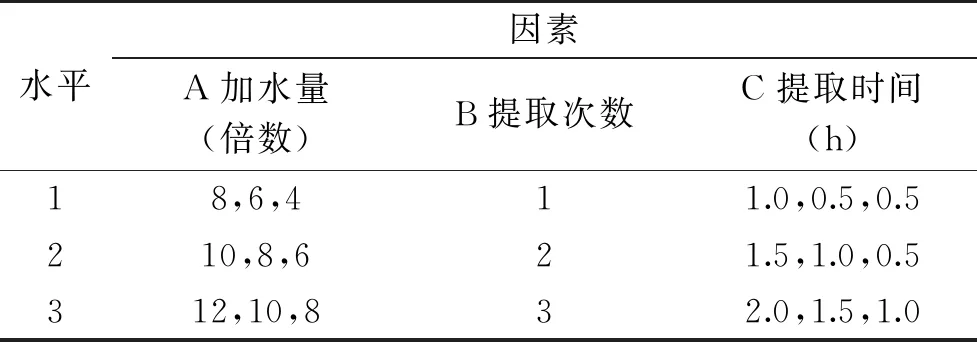
表1 正交因素水平表Table 1 Factors and levels of orthogonal design
M=b1×aij/s1+b2×bij/s2+b3×cij/s3+b4×dij/s4
式(1)
其中,aij、bij、cij、dij为第i项的第j个指标;s1、s2、s3、s4为样本标准差;b1、b2、b3、b4为权重系数。
称取三份处方量的当归润肠膏组方,分别按最佳提取工艺条件提取,分析魏酸含量、出膏得率、浸出物含量、多糖含量,计算综合评分。
1.2.1.3 出膏得率的测定 将提取液过滤,置于蒸发皿浓缩,真空冷冻干燥至恒重,取出置于干燥器中至室温,称量,出膏得率(%)=干膏重×100/药材重量。
1.2.1.4 浸出物含量的测定 取上述干膏,精密称定。按照2015年版《中国药典》第四部中关于浸出物的测定方法(2201,热浸法)进行测定。
1.2.1.5 多糖含量的测定 精密称取葡萄糖对照品57.0 mg,置于50 mL容量瓶中,加蒸馏水稀释至刻度,摇匀,即得114 μg/mL的葡萄糖对照品溶液,将其稀释为0、22.8、45.6、68.4、91.2、114.0 μg/mL质量浓度的对照品溶液。取各溶液1 mL,加入1 mL的苯酚,再立即加入5 mL的浓硫酸,冷却至室温,以蒸馏水为空白对照,于UV-1700可见分光光度计490 nm处测各溶液的吸光度[13]。以浓度(X)为横坐标,吸光度(Y)为纵坐标线性回归,即得回归方程Y=0.0091X-0.0099(R2=0.9991),葡萄糖在0~114.0 μg/mL范围内与吸光度成良好的线性关系。
取提取液25 mL,加入100 mL无水乙醇,搅拌均匀,使其含醇量达80%,静置5 min后,以5000 r/min的转速离心20 min,收集沉淀,真空冷冻干燥,即得干燥近白色的粗多糖,称重。准确称取3.0 mg粗多糖,转移于25 mL的容量瓶中,用蒸馏水定容至刻度,摇匀,即得供试品溶液[14]。取供试品溶液各1 mL,同上述测定法,求得多糖含量。
1.2.1.6 阿魏酸含量的测定 准确称取阿魏酸对照品3.5 mg于25 mL的容量瓶中,加甲醇定容至刻度,得140 μg/mL的对照品溶液,将其稀释到浓度为0.875、1.75、3.5、7.0、14.0 μg/mL的对照品溶液。精密吸取20 μL注入液相色谱仪测定。色谱柱为Diamonsil C18反相柱(250 mm×4.6 mm,5 μm);流动相为甲醇:0.1%磷酸(40∶60);柱温为35 ℃;检测波长为323 nm[15]。以浓度(X)为横坐标,峰面积(Y)为纵坐标,即得回归方程Y=121060X-9193.3(R2=0.9996)。阿魏酸在0.875~14.00 μg/mL浓度范围内与峰面积值成良好的线性关系。
取正交实验所得提取液1 mL,置25 mL的容量瓶中,加甲醇稀释至刻度。超声30 min,摇匀,用微孔滤膜(0.45 μm)滤过,即得供试品溶液,同上法测定。
1.2.2 制备工艺研究 按处方量称取6组药材,分别依照最优提取工艺操作,所得6组平行样品分别浓缩至用玻璃棒挑动有拉丝现象出现,测其相对密度,之后分别与原药材相同质量的炼蜜(相对密度为1.48,粘度为36117.0 cp)均匀混合,制得6批煎膏剂样品,分别测定样品的相对密度,并观察其流动性。
1.2.3 质量标准研究
1.2.3.1 薄层色谱(TLC)鉴别 按相同的制备工艺平行制备6组当归润肠膏,编号为3~8。参照2015年版《中国药典》第一部中的药材项下有效成分的鉴别方法[16],对当归润肠膏中当归、大枣、干姜、枳壳进行TLC鉴别。其中,阴性样品按上述相同制备工艺制备,只是处方中不含有对应检测的药材。
1.2.3.2 检查 结合6批煎膏剂样品的相对密度测定值,制定本煎膏剂的相对密度为1.32~1.37。其它应符合煎膏剂项下有关的各项规定(参照《中国药典》2015年版第四部附录通则0183)。
1.2.3.3 阿魏酸含量测定 测定方法同“1.2.1.6”项下的阿魏酸含量测定方法。分别对实验中6批样品进行含量测定,每批样品平行测定3次。
1.2.4 稳定性考察
1.2.4.1 影响因素试验 将按照最优工艺制备的样品分成两份,取适量分别装在棕色和透明磨口玻璃瓶中,置于20 ℃、4500 lx光照条件的药物稳定性检查仪中,于第0、5、10 d取样,按《中国药典》2015年版四部(通则)煎膏剂项下有关的各项规定进行检测,包括性状、相对密度、不溶物、阿魏酸含量。另取所制样品置于棕色玻璃瓶中,在60 ℃烘箱中放置10 d,于第0、5、10 d取样分析。
1.2.4.2 恒温加速试验 将按照最优工艺制备的样品分成两份,其中一份加入终浓度为0.4%(w/w)的NaHSO3和0.1%(w/w)的EDTA-2Na作为稳定剂,转移到棕色玻璃瓶中,分别放置在60、70、80、90 ℃的烘箱中,按设定时间取样,取出后迅速降温至室温,按供试品溶液的制备方法处理,测定样品中阿魏酸的含量。
1.3 数据处理
2 结果与分析
2.1 单因素实验
2.1.1 加水量的影响 由图1可知,出膏得率随加水量的增加而出现升高的趋势,但当加水量为原药材质量的8倍以上时,出膏得率基本维持稳定,且在前3个水平间出膏得率均具有显著性差异(p<0.05)。当加水量为10倍时出膏得率有所下降,很有可能是因为过多的水份导致浓缩过程中产生损耗。综合水的消耗量及出膏得率,选择加水量的中心水平为原药材质量的10倍。

图1 加水量对出膏得率的影响Fig.1 Effect of volume of water on extract yield
2.1.2 提取次数的影响 由图2可知,提取次数由1次增加到2次时,出膏得率显著(p<0.05)增加。当提取次数大于2次时,随提取次数的增加,出膏得率增加,但其增加幅度并不显著,基本维持在66%~70%之间。基于实际生产和成本角度考虑,确定提取次数的中心水平为2次。
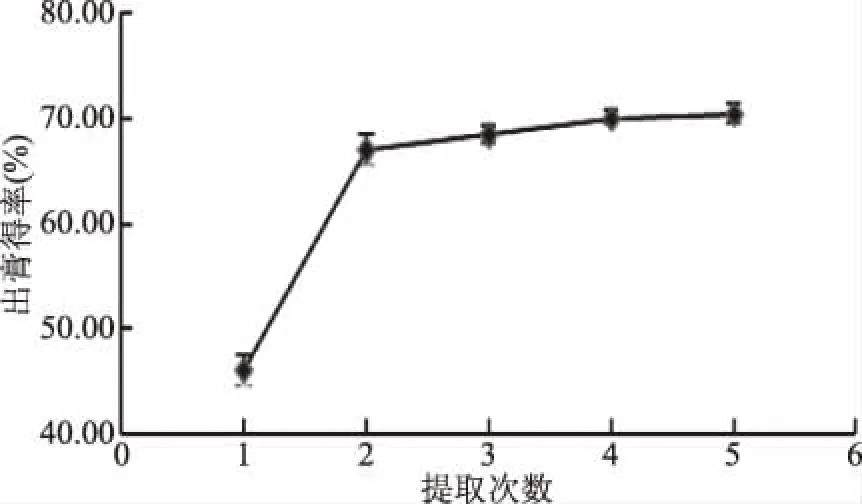
图2 提取次数对出膏得率的影响Fig.2 Effect of the number of extract on extract yield
2.1.3 提取时间的影响 由图3可知,随着提取时间的延长,出膏得率不断增加,且在前3个水平间出膏得率均具有显著性差异(p<0.05),这可能是因为提取不完全。之后随时间延长,出膏得率增加缓慢,基本保持不变。所以确定提取时间的中心水平为1.5 h。

图3 提取时间对出膏得率的影响Fig.3 Effect of extract time on extract yield
2.2 正交试验结果
对评价指标进行综合评分,具体结果见表2。由方差分析(表3)可知,A、B、C因素差异均不显著(p>0.05)。由表2直观分析可知,A、B、C均对综合评分有影响,极差B>A>C(R=4.08>2.47>1.99),故影响试验结果的主次因素顺序为B>A>C。A因素中A2>A3>A1,选择因素最好水平A2;B因素中B3>B2>B1,其中B2与B3相差不多,考虑到节能,选择因素水平B2;C因素中C3>C1>C2,选择因素最好水平C3。综合考虑,并结合生产实际,确定A2B2C3为最佳提取条件,即:第一次加水10倍量,浸泡1.25 h,回流提取2 h;第二次加水8倍量,回流提取1.5 h。
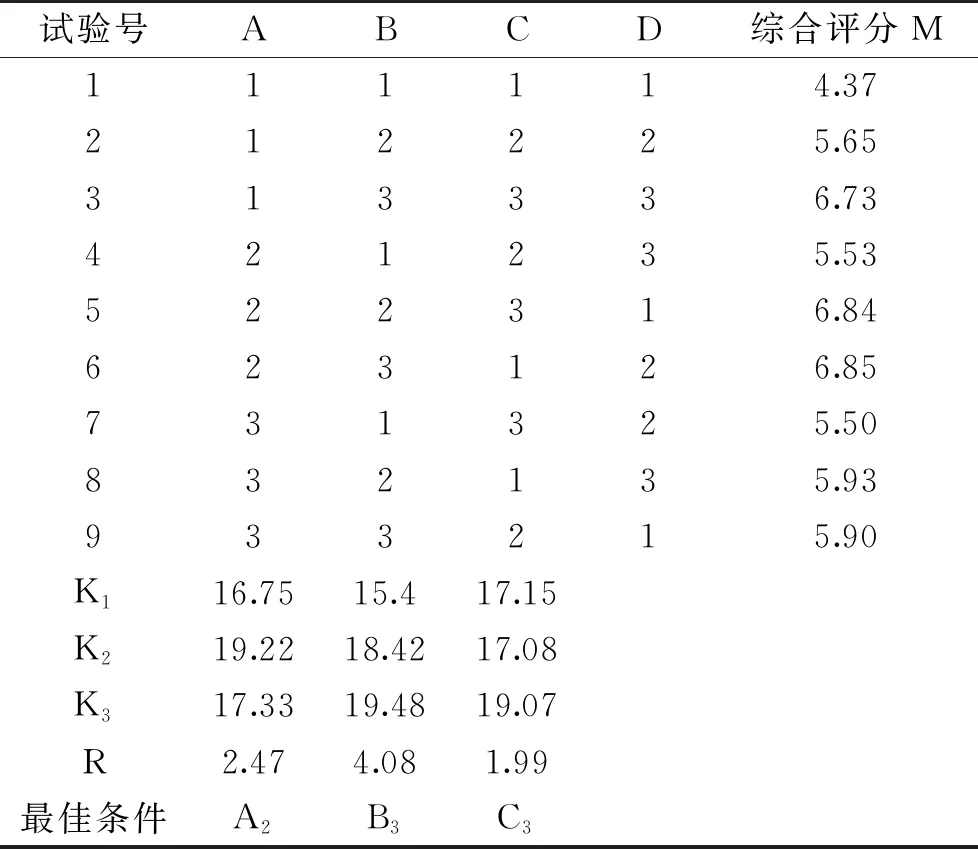
表2 正交试验结果Table 2 Results of orthogonal tests

表3 综合评分的方差分析Table 3 Analysis variance of comprehensive evaluation
2.3 最佳提取工艺验证
采用最佳提取工艺条件,平行操作,得到3批浸膏样品,其出膏得率、浸出物含量分别为64.24%±0.99%、21.43%±0.68%,多糖、阿魏酸含量分别为(7.78±0.03)、(4.05±0.24) mg/mL,综合评分M为7.13±0.25。
2.4 制备工艺结果
当浸膏浓缩至相对密度为1.207±0.008时,与炼蜜(相对密度为1.48,粘度为36117.0 cp)按原药材质量比1∶1 (w/w)混合。分别测定6批样品的相对密度,观察流动性,所得煎膏剂相对密度在1.32~1.37之间,其粘度适中,流动性较好。
2.5 质量标准
2.5.1 性状 本品为煎膏剂,均为棕褐色稠膏,气微,味微苦,无糖结晶析出。
2.5.2 薄层色谱(TLC)鉴别
2.5.2.1 当归TLC鉴别 供试品色谱中,与阿魏酸对照品相应的位置上(Rf=0.2289)显相同的黄色荧光斑点,在与当归对照药材相应的位置上显示2个相同的黄色荧光斑点,而阴性样品在对应处均无斑点(见图4)。

图4 当归润肠膏中阿魏酸的薄层色谱图Fig.4 Thin layer chromatogram of ferulic acid of DangguiRunchang paste注:1.阿魏酸对照品;2.当归对照药材; 3~8.当归润肠膏样品;9.不含当归药材制备的阴性膏。
2.5.2.2 大枣TLC鉴别 供试品色谱中,与齐墩果酸对照品相应的位置上(Rf=0.6184)显相同的褐色斑点,在与大枣对照药材相应的位置上显示2个相同的褐色斑点,而阴性样品在对应处均无斑点(见图5)。
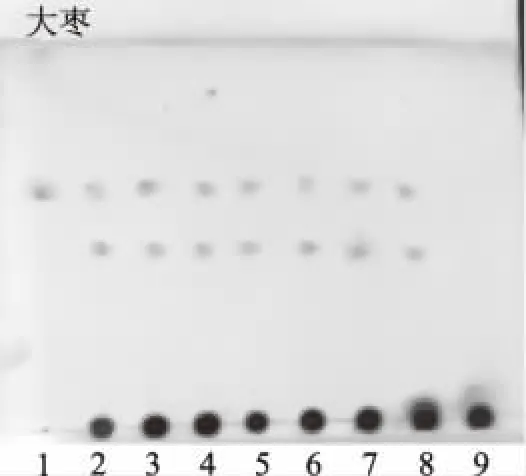
图5 当归润肠膏中齐墩果酸的薄层色谱图Fig.5 Thin layer chromatogram of oleanolic acid of DangguiRunchang paste注:1.齐墩果酸对照品;2.大枣对照药材; 3~8.当归润肠膏样品;9.不含大枣药材制备的阴性膏。
2.5.2.3 干姜TLC鉴别 供试品色谱中,与6-姜酚对照品相应的位置上(Rf=0.4150)显相同的褐色斑点,在与干姜对照药材相应的位置上显示1个相同的褐色斑点,而阴性样品在对应处均无斑点(见图6)。
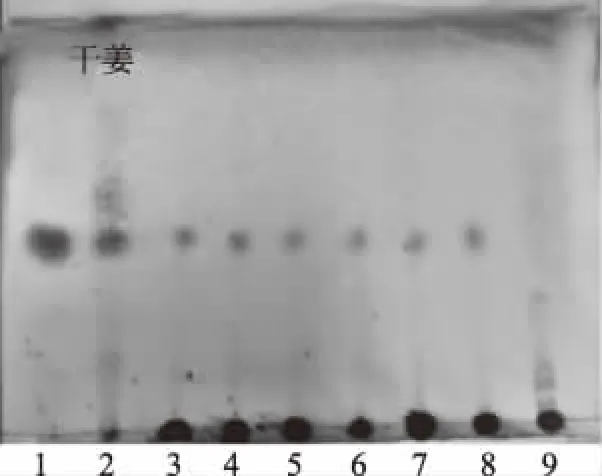
图6 当归润肠膏中6-姜酚的薄层色谱图Fig.6 Thin layer chromatogram of 6-gingerol of Danggui Runchang paste注:1.6-姜酚对照品;2.干姜对照药材; 3~8.当归润肠膏样品;9.不含干姜药材制备的阴性膏。
2.5.2.4 枳壳TLC鉴别 供试品色谱中,在与新橙皮苷对照品相应的位置上(Rf=0.3428)显相同的黄色荧光斑点,在与枳壳对照药材相应的位置上显示2个相同的黄色荧光斑点,而阴性样品在对应处均无斑点(见图7)。
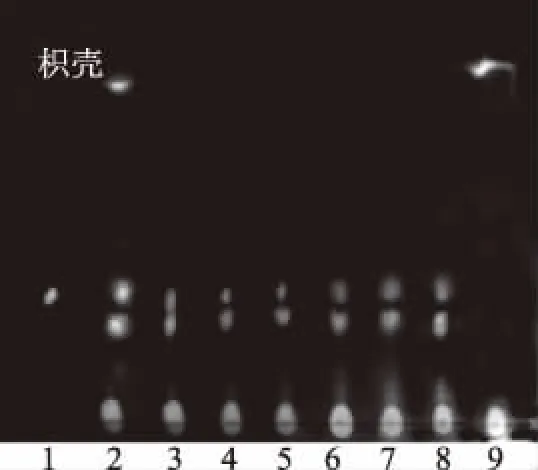
图7 当归润肠膏中新橙皮苷的薄层色谱图Fig.7 Thin layer chromatogram of hesperidin of Danggui Runchang paste注:1.新橙皮苷对照品;2.枳壳对照药材; 3~8.当归润肠膏样品;9.不含枳壳药材制备的阴性膏。
薄层色谱图中显示,在当归润肠膏中,当归、大枣、干姜、枳壳的分离效果和显色效果均良好,在对照品色谱相应的位置上,显相同颜色的斑点,而阴性样品均在对应处无斑点,表明该法对供试品中各成分有较好的分离,且灵敏度高,专属性好。
2.5.3 阿魏酸含量 由表4可见,6批当归润肠膏样品中,平均每g样品含阿魏酸(102±4.4) μg。参照2015年版《中国药典》当归药材项下有效成分最低限量的规定,阿魏酸的含量不得低于0.05%,则当归润肠膏中每g含阿魏酸理论上不得低于108 μg,结合本试验结果,加上制备过程中的转移率约为80%,暂定当归润肠膏中每g含阿魏酸(C10H10O4)不得少于90 μg。

表4 样品中阿魏酸含量Table 4 The content of ferulic acid in the sample
2.6 煎膏剂的稳定性
2.6.1 影响因素试验 强光照射下,透明瓶中的样品气味发生变化,阿魏酸含量减少,而在棕色瓶中的样品气味和阿魏酸含量基本无变化;高温环境下,煎膏剂的性状发生改变,气味变酸,阿魏酸含量随着时间的推移呈明显下降趋势(表5)。因此,当归润肠膏在强光和高温贮藏条件下不稳定,应低温、避光保存。
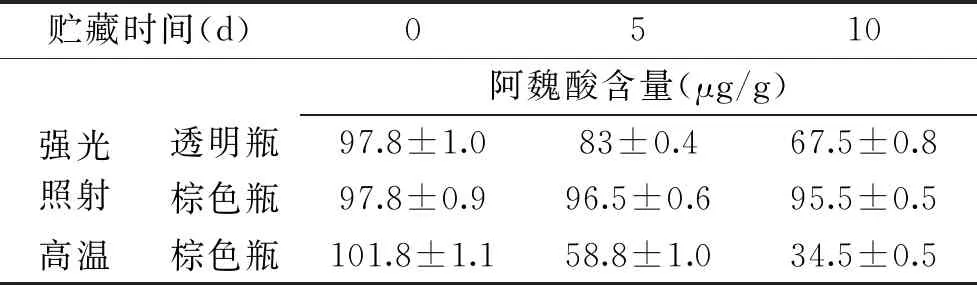
表5 当归润肠膏稳定性试验Table 5 Stability test of DangguiRunchang paste
2.6.2 恒温加速试验 用阿魏酸浓度的对数值(lgC)与取样时间(t,min)作图接近直线,拟合度(R2)接近0.99,所以按一级动力学方程(3)计算药物降解速率常数(K)。将摄氏温度改换为热力学温度T(T= ℃+273.15)(表6),可以看出随温度升高,药物降解速率常数(K)值越大,即可根据阿仑尼乌斯(Arrhenius)方程(2)拟合lgK和1/T[17],得未加稳定剂的直线方程为lgK=-5199.1/T+13.2(R2=0.9808),添加稳定剂的直线方程为lgK=-6612.61/T+17.0(R2=0.9974)。将室温25 ℃(T=298 K)分别代入上述直线方程,求出室温贮藏时的阿魏酸降解速率常数K,再根据一级反应方程式(3)计算药物降解10%所需的时间(t0.9)[18]。结果显示未添加稳定剂的当归润肠膏的预测保质期约3个月,而添加稳定剂的样品预测保质期延长至1.68年。由此可知,在当归润肠膏中加入0.4%的NaHSO3、0.1%的EDTA-2Na作为稳定剂,比不加稳定剂的保质期延长了近8倍,能基本满足生产储存的要求。

表6 试验温度与速率常数表Table 6 Test temperature and rate constants
lgK=-E/2.303RT+lgA
式(2)
其中:K是反应速率常数;A是频率因子;E是活化能;R为气体常数;T是绝对温度。
lgC=-Kt/2.303+lgC0
式(3)
其中:C0为t=0时的反应浓度,C为t时反应物的浓度。
3 结论
采用正交试验对当归润肠膏的提取工艺进行优化,以出膏得率、浸出物、多糖含量和阿魏酸含量四项参数为评价指标,确定了当归润肠膏的最佳提取工艺。本研究中,通过不同相对密度的提取物和不同程度的炼蜜进行混合,观察所制煎膏剂的黏稠性和流动性,结合实际生产和使用的便利性,进而选择提取物浓缩的程度和蜂蜜炼制的程度。经3批次的提取工艺验证和6批煎膏剂样品的制备,本文报道的提取和制备工艺科学合理,数据可靠,适宜于实际生产。
为了保证药物的安全性和有效性,以及生产流通、使用各个环节的影响,本实验参照2015年版《中国药典》煎膏剂项下的要求,对当归润肠膏进行了全方位的质量标准研究,确定了控制产品质量的项目和限度,制定了科学、合理、可行的并能反映产品特征的和质量变化情况的质量标准,有效的控制了产品批间质量的一致性及验证生产工艺的稳定性。
当归润肠膏在强光和高温环境下放置10 d后,阿魏酸含量呈明显下降趋势,可能是阿魏酸结构中酚羟基在高热和强光下均易发生氧化或分子间发生聚合,导致含量下降,这与文献报道的研究结果一致[19-21]。因此,在生产和贮存过程中应尽量采用避光措施,在低温环境下贮藏。
当归润肠膏在恒温加速试验中,浓度对数值与取样时间的拟合度(R2)接近0.99,提示其降解反应属于一级动力学过程;另外,温度越高,速率常数K值越大,提示降解速率与温度成正相关,由此可用Arrhenius定律处理。在当归润肠膏中加入0.4%的NaHSO3、0.1%的EDTA-2Na作为稳定剂,其预测保质期为1.68年,比不加稳定剂的样品保质期延长了8倍,说明稳定剂的加入有效抑制了阿魏酸含量的下降。本实验结果以阿魏酸为标志性成分得出的保质期仅为理论预测值,实际生产可暂定为1.5年。客观的保质期需要通过室温留样观察实验获得,该实验仍在进行当中。

