头孢唑林钠与胶塞相容性关系的探讨
崇小萌 董欣 姚尚辰 胡昌勤
(中国食品药品检定研究院,北京 102629)
头孢唑林钠是第一代半合成头孢菌素类抗生素,自20世纪70年代初上市以来,被广泛用于治疗呼吸道、皮肤、泌尿系统及胆道等各种细菌感染[1]。其存在无定型及多种水合物包括α型(含5分子结晶水)、β型(含3/2分子结晶水)和γ型(含1分子结晶乙二醇)等晶体[2]。深圳九新药业有限公司与中国食品药品检定研究院合作,在异丙醇-水体系中得到了一种全新的螯合头孢唑林钠水合物晶体—五水头孢唑林钠;该晶体中头孢唑林分子排列配成一个隧道式空腔,水分子和钠离子存在于空腔之内,螯合头孢唑林钠晶体的理化特性与α头孢唑林钠相似,较无定型头孢唑林钠具有更好的化学稳定性[3-5]。目前上市的注射用头孢唑林钠有冷冻干燥工艺生产的无定型产品、头孢唑林水合物(α型头孢唑林钠)和五水头孢唑林钠。
国家评价性抽验揭示,目前市场上的注射用头孢菌素,“溶液的澄清度与颜色”问题是突出的质量问题[6]。注射用头孢菌素“溶液的澄清度”(简称澄清度)问题由来已久,表现为样品溶解后溶液呈浑浊状态,且在贮存期澄清度逐渐变差。导致澄清度问题的主要原因和药物与胶塞的相容性有关[7-14],如胶塞中释放出的抗氧剂2,6-叔丁基-4-甲基-苯酚(BHT)与头孢曲松钠可形成不溶性的复合物[11]。药物的晶体状态可影响药物与胶塞的相容性。不同亚晶型结构的头孢曲松钠对BHT的吸附能力不同,对头孢曲松钠结晶工艺的控制可明显改善产品的澄清度[15]。注射用头孢唑林钠的国家评价性抽验揭示,由于澄清度不符合规定,2009年的合格率仅为74.1%,而同期抽验的注射用五水头孢唑林钠的澄清度全部符合规定;2011年的评价性抽验结果显示,选用覆膜胶塞替代普通胶塞,产品的澄清度全部符合规定[13];提示覆膜胶塞可以阻断胶塞迁移物与头孢唑林钠的相互作用。但究竟是何种物质可与头孢唑林钠发生相互作用,相容性实验如何合理的选择胶塞,不同生产工艺的头孢唑林钠原料与胶塞是否具有不同的相容性等问题仍为未知。为实现对药物-胶塞相容性的快速评价,我们建立了胶塞挥发性成分筛查数据库、加速相容性实验和模拟吸附实验等方法,在此基础上形成了一个较为完整的药物-胶塞相容性实验策略[16]。
本研究利用此策略,通过发现胶塞中与头孢唑林钠相互作用,导致其澄清度变浑浊的物质,对无定型头孢唑林钠和五水头孢唑林钠与胶塞的相容性进行评价。
1 材料与方法
1.1 样品与试剂
无定型头孢唑林钠和五水头孢唑林钠由深圳九新药业提供;八甲基环四硅氧烷、2,6-二叔丁基-4-甲基苯酚(BHT)均购自SIGMA-ALDRICH;胶塞为未覆膜的氯化丁基胶塞。实验用水经Millipores Milli-Q过滤。
1.2 气质联用(GC-MS)方法
顶空气相色谱仪Agilent7694-7890;气质联用仪Thermo Finnigan Trace GC-Polaris Q;色谱柱:5%苯基-95%甲基硅氧烷(DB-5MS,30.0m×0.25mm,0.25μm);载气:氦气;流速1.0mL/min;色谱柱程序升温:50℃维持10min,10℃/min升至170℃,维持20min;顶空条件:121℃维持30min;采用甲烷测定色谱系统的死时间(t0),BHT作为参比物质,挥发性成分的调整相对保留时间RART=[tR-t0]/[tR(参比物)-t0]。 质谱条件:离子源:EI,70eV;全扫描,扫描范围50~650Da。利用Xcalibur工作站NIST质谱库检索组分的结构。
1.3 胶塞中挥发物的测定
取胶塞1枚,剪碎后放入10mL顶空瓶中,加空白胶塞密封,采用顶空GC-MS法分别测定加速实验样品和对照样品,并利用胶塞挥发性成分筛查数据库确定药物中吸附的胶塞析出物成分。
1.4 加速相容性实验
称取药物粉末约200mg,与1枚剪碎的胶塞混合,放入10mL顶空瓶中,加空白胶塞密封后,置于摇床中以300r/min的转速振摇24h;将瓶中的药物粉末转移至另一顶空瓶中,用空白胶塞密封,得到加速实验样品。同法制备不混合胶塞仅含药物粉末的对照样品。采用顶空GC-MS法分别测定加速实验样品和对照样品,并利用胶塞挥发性成分筛查数据库确定药物中吸附的胶塞析出物成分。同时,采用比浊法测定加速实验样品的澄清度,分析样品中吸附的胶塞析出成分的量与样品澄清度的相关性。
1.5 模拟吸附实验
将药物粉末与挥发物对照品分别放入不同的开口称量瓶中,并置于同一干燥罐内中(图1),密封,室温(约25℃)放置;分别于第1、2、4、16和24h称取样品约500mg,放入10mL顶空瓶中,用空白胶塞密封后,采用顶空GC-MS法测定药品中释放出的挥发性成分。同时,另称取样品500mg,采用比浊法测定样品的澄清度化。
1.6 溶液的澄清度测定
采用HACH TL23台式浊度仪,比浊法测定样品溶液的澄清度。称取药物粉末,用水溶解,制成浓度为25mg/mL的样品溶液;测定时,以水为空白,先测定空白溶液,再测定样品溶液的浊度值。
2 结果与讨论
2.1 头孢唑林钠对胶塞析出物的吸附作用
根据文献[16],可以与头孢菌素发生吸附导致澄清度变差的胶塞析出物包括BHT、硅氧烷类化合物以及CS2,采用GC-MS方法结合筛查数据库,对10种不同种类胶塞(包括氯化丁基胶塞及溴化丁基胶塞)中挥发物进行测定,选取了同时含有BHT、硅氧烷类化合物以及CS2的一种胶塞作为加速相容性实验用胶塞。

图1 吸附模拟实验示意图Fig.1 The schematic diagram of simulated adsorption experiment
利用加速相容性实验筛查头孢唑林钠对胶塞析出物的吸附作用。利用GC-MS筛查加速实验后无定型头孢唑林钠和五水头孢唑林所吸附的胶塞析出物(图2),发现二者吸附的胶塞析出物的种类基本相同,但无定型头孢唑林钠的吸附量远高于五水头孢唑林钠;采用胶塞挥发性成分筛查数据库对胶塞析出物进行定性分析,确认其主要为环硅氧烷类和BHT(表1)。
2.2 模拟吸附实验确认导致样品变浑浊的原因

图2 无定型头孢唑林钠与五水头孢唑林钠气质总离子流图Fig.2 The total ion chromatograms of amorphous cefazolin sodium and cefazolin sodium pentahydrate
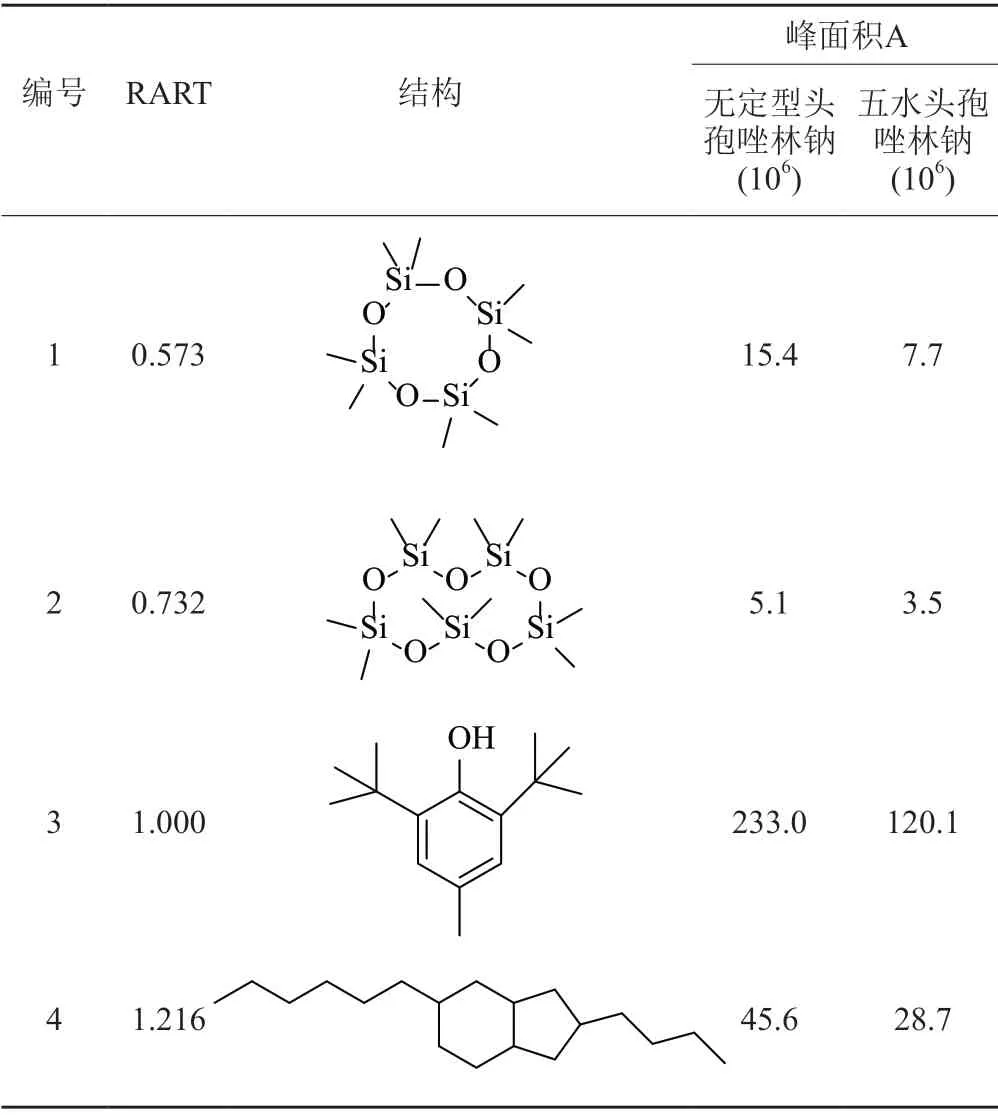
表1 头孢唑林钠吸附的主要胶塞挥发性成分Tab.1 Main volatile components of rubber closures adsorbed by cefazolin sodium
为进一步确认胶塞析出物对头孢唑林钠澄清度的影响,利用模拟吸附实验比较无定型头孢唑林钠和五水头孢唑林钠对八甲基环四硅氧烷和BHT的吸附作用及对澄清度的影响。结果显示,无定型头孢唑林钠较五水头孢唑林钠对八甲基环四硅氧烷的吸附作用更强,且溶液更易变浑浊(表2)。
对头孢唑林钠吸附八甲基环四硅氧烷量与溶液的浊度值进行相关性分析(图3),结果显示,二者吸附八甲基环四硅氧烷的量均与其浊度值呈良好的相关性。无定型头孢唑林钠得到的线性方程,斜率为0.1196,R2=0.8914;五水头孢唑林钠得到的线性方程,斜率为0.0701,R2=0.8738;提示二者对八甲基环四硅氧烷的吸附均是影响其澄清度的重要因素,且无定型头孢唑林钠对八甲基环四硅氧烷的吸附速率更快(斜率较大)。
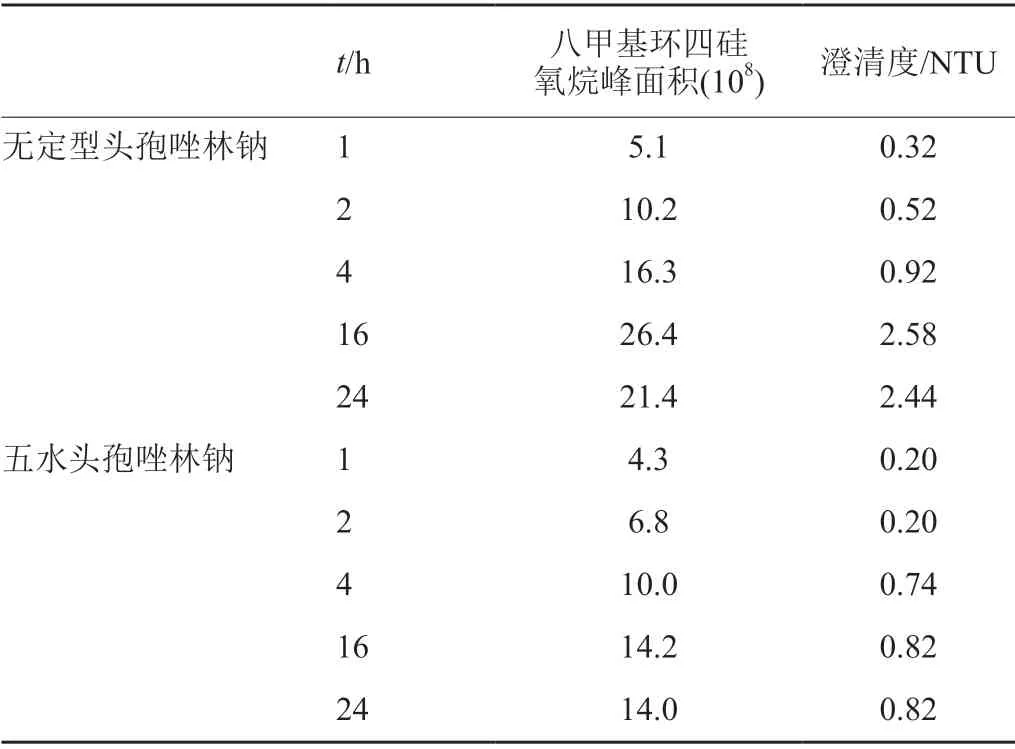
表2 头孢唑林钠对八甲基环四硅氧烷的吸附作用及对浊度值的影响Tab.2 The adsorption of cefazolin sodium on octamethylcyclotetrasiloxane and its effect on turbidity
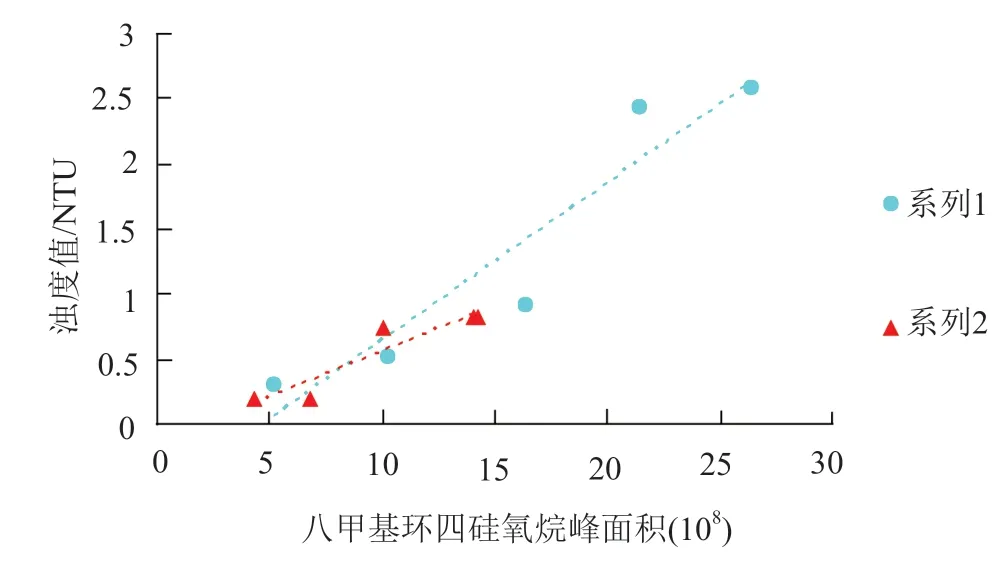
图3 无定型头孢唑林钠及五水头孢唑林钠吸附八甲基环四硅氧烷的量与浊度值的相关性Fig.3 The correlation between the quantity of adsorption on octamethylcyclotetrasiloxane and turbidity of amorphous cefazolin sodium and cefazolin sodium pentahydrate
头孢曲松钠吸附BHT形成不溶性复合物是导致头孢曲松钠澄清度变差的原因之一[11]。模拟吸附实验结果显示,头孢唑林钠虽然也较易吸附BHT,但随着BHT吸附量的增加,澄清度并未发生明显变化(表3),提示头孢唑林钠与BHT相互作用不能形成不溶性复合物,BHT不是导致头孢唑林钠澄清度变浑浊的物质。与八甲基环四硅氧烷的吸附作用相似,无定型头孢唑林钠较五水头孢唑林钠更易吸附BHT。

表3 头孢唑林钠对BHT的吸附作用及对浊度值的影响Tab.3 The adsorption of cefazolin sodium on BHT and its effect on turbidity
3 结论
头孢唑林钠可以吸附胶塞中析出的硅氧烷类物质、BHT等胶塞析出物,其对硅氧烷类物质的吸附作用是影响其溶液澄清度变差的主要原因。无定型头孢唑林钠较五水头孢唑林钠更易吸附胶塞析出物,因此,五水头孢唑林钠较无定型头孢唑林钠具有更好的胶塞相容性。利用GC-MS对胶塞进行筛查,可以对头孢唑林钠与胶塞的相容性进行快速评价。

