新型糖肽类抗生素B7011对细菌感染小鼠败血症的体内抗菌作用研究
朱珍真 郎丽巍 王红艳 朱姗薇 韩晓彤 张翠英 曹艳茹 魏振满,*
(1 中国人民解放军总医院第五医学中心药学部药物试验中心,北京 100039;2 成都雅途生物技术有限公司,成都 610041)
随着细菌耐药程度日趋上升,其中葡萄球菌及肠球菌都具有较高水平的耐药性[1-2],由其引起的败血症、急性肺炎以及皮肤和软组织感染等严重感染疾病,增加了患者的痛苦[3],针对此类感染,研发新型抗生素已经迫在眉睫。
目前,万古霉素、利奈唑胺、达托霉素等抗生素是临床上治疗耐药菌感染的常用药。但是随之而来的是细菌对这些药物的的敏感性呈逐年下降的趋势,再加之万古霉素、利奈唑胺等药物具有较大的毒副作用,使其在临床上的应用受到一定程度的限制[4-5]。
B7011是成都雅途生物技术有限公司自主研发的半合成第二代糖肽类抗生素,本研究的前期试验中,我们检测了B7011和万古霉素对目标菌株的体外抗菌活性,测得B7011对MSSA、MRSA、VRE的MIC值分别为≤0.125、≤0.125和0.015μg/mL,均显著低于万古霉素(1、1和>256μg/mL,表明B7011具有较好的体外抗菌活性。本研究以VRE、MSSA和MRSA感染败血症小鼠为动物模型,研究B7011对败血症小鼠的保护作用。
1 试验材料
1.1 试验药品
试验药:B7011,成都雅途生物技术有限公司研制;批号:121210-2,效价:97%;对照药:万古霉素(vancomycin),美国礼来制药公司研制;批号:c060864,效价:100%。
1.2 试验菌株
革兰阳性菌3株。其中MSSA为标准菌株,其菌号:ATCC29213;而MRSA以及VRE为临床分离的耐药菌株;以上菌株均由卫生部临床检验中心微生物室提供。
1.3 培养基与孵育条件[6-7]
葡萄球菌:恒温35℃,在M-H培养基中孵育18h;屎肠球菌:恒温35℃,在含有5%绵羊血的M-H培养基中孵育20~24h。
1.4 试验动物
ICR种小鼠,体重控制在18~22g,性别见具体实验方法,由北京市斯贝福试验动物有限公司提供;动物合格证号:SYXK(京)2011-0004;动物饲养地点:原中国人民解放军第三〇二医院实验技术保障研究中心动物实验室,实验室许可证号:SYXK(军)2012-0010。
1.5 保护剂
高活性干酵母,安琪酵母股份有限公司,生产日期:2013年4月8日。用纯化水配置成浓度为5%的混悬液,高压后放于4℃冰箱保存备用。
2 试验方法
2.1 增毒实验方法[6-8]
为了得到可导致实验动物80%~100%死亡的菌浓度,即最小致死剂量(minimum lethal dose,MLD)菌浓度,需要对致病菌进行增毒。增毒方法为:于试验前1d将试验用菌接种于10mL MH液体培养基中,按照“1.3项”所列要求进行培养。用保护剂将培养好的菌原液做10-1、10-2倍稀释,并对雄性ICR小鼠进行腹腔注射,注射剂量为每只0.5mL,注射后观察。在无菌条件下解剖感染后刚死亡或濒死小鼠,取心脏血涂于MH固体培养基上继续培养细菌,再以此菌继续感染小鼠,按此方法重复实验2~3次,得到MLD菌浓度。
2.2 免疫低下小鼠的建模[6-9]
由于VRE毒力较弱,故用腹腔注射VRE菌液造成小鼠急性败血症时,需在感染前先将试验小鼠制备成免疫低下小鼠,以提高感染的成功率。制备方法为:分别于第1天和第4天,对ICR小鼠进行一次皮下注射环磷酰胺,注射剂量为200mg/kg/次,通过此方法,可以使小鼠的白细胞值降至100~150×109/L,末次注射环磷酰胺16h后再腹腔注射感染VRE菌液,可以保证模型对照组的死亡率在80%以上。
2.3 药液稀释方法[10]
采用孙瑞元介绍的低比值系列稀释方法,即相临两个剂量组的药液以0.65~0.7倍进行稀释,一共稀释6~7个浓度。药物剂量可以通过预实验数据获得。在正式试验中,最高药物剂量应尽量保证感染鼠存活率达到70%~100%,最低药物剂量应尽量使得感染鼠的存活率低于30%。
2.4 ED50(50%有效剂量)动物保护试验[6-7]
将体重为18~20g的ICR种小鼠进行随机分组,每组10只,雌雄各半。禁食后,取5%高活性干酵母混悬液配制的MLD浓度的菌液,按每只0.5mL的剂量,以腹腔注射的方式建立感染模型。注射后1h,通过尾静脉注射给予不同浓度的药物,剂量为每只0.2mL。感染后连续观察7d,记录各给药组、阳性对照组以及MLD和0.1 MLD感染组小鼠死亡数,将给药剂量和对应的小鼠死亡数导入DAS 2.1.1软件进行半数有效剂量的运算,得到试验药和对照药的ED50、ED5、ED95,以及两药药效学参数比较P值结果。
3 结果
3.1 对MSSA致小鼠急性感染败血症模型的保护作用
B7011对MSSA-ATCC 29213致小鼠急性败血症模型的保护作用结果为:ED50、ED5、ED95值分别为0.722、0.468和1.115mg/kg。阳性对照药万古霉素对敏感菌所致败血症模型也有较好的保护作用,其ED50、ED5、ED95值分别为0.764、0.416和1.403mg/kg;比较两药的保护作用,统计结果P=0.645,提示差异无统计意义。表明B7011对MSSA所致小鼠急性败血症模型的体内保护作用与阳性对照药万古霉素相似。具体数值见表1~2。
3.2 对MRSA致小鼠急性感染败血症模型的保护作用
B7011对MRSA- C118致小鼠急性败血症模型的保护作用结果为:ED50、ED5、ED95值分别为0.193、0.045和0.82mg/kg,阳性对照药万古霉素组的感染动物死亡数量明显多于试验药组,其ED50、ED5、ED95值分别为:0.374、0.092和1.515mg/kg;比较两药的保护作用,统计结果P<0.05,差异有统计意义,由此可见,针对耐药菌感染所致的小鼠急性败血症模型,新型糖肽类抗生素B7011的体内保护作用明显优于万古霉素。具体数值见表1~2。
3.3 对VRE致小鼠感染败血症模型的保护作用
B7011对VRE-No.5所致小鼠急性败血症模型的保护结果为:ED50、ED5、ED95值分别为0.395、0.046和3.429mg/kg,而该致病菌对阳性对照药万古霉素产生了明显的耐药性,导致即使提高了万古霉素的给药剂量,但动物的死亡数量仍然较多。万古霉素对VRE的ED50、ED5、ED95值分别为1.547、0.079和30.168mg/kg;两药统计学处理P值<0.01,差异有统计意义。说明B7011对VRE所致小鼠急性败血症模型体内保护作用明显优于万古霉素。具体数值见表1~2。
4 讨论
B7011是成都雅途生物技术有限公司自主研发的半合成第二代糖肽类抗生素。与其他糖肽类抗生素相似,B7011的药理作用为:与处于分裂期的细胞壁肽聚糖前体末端的氨基酰-D-丙氨酰-D-丙氨酸结合,以此阻碍细胞壁的合成,从而起到抑制并杀灭细菌的作用[11-12]。不同的是,B7011在糖基侧链中加入了一条饱和烃基链,长度为11个碳原子,这一脂肪链的引入起到了大幅增加B7011半衰期的作用,而且还有利于药物分子与致病菌细胞膜的锚定,从而增加了B7011的抗菌活性。
前期的体外试验结果表明B7011抗菌谱主要为革兰阳性菌。本研究检测了B7011和万古霉素对目标菌株的体外抗菌活性,测得B7011对MSSA、MRSA、VRE的MIC值分别为≤0.125、≤0.125和0.015μg/mL,均显著低于万古霉素(1、1和>256μg/mL)。
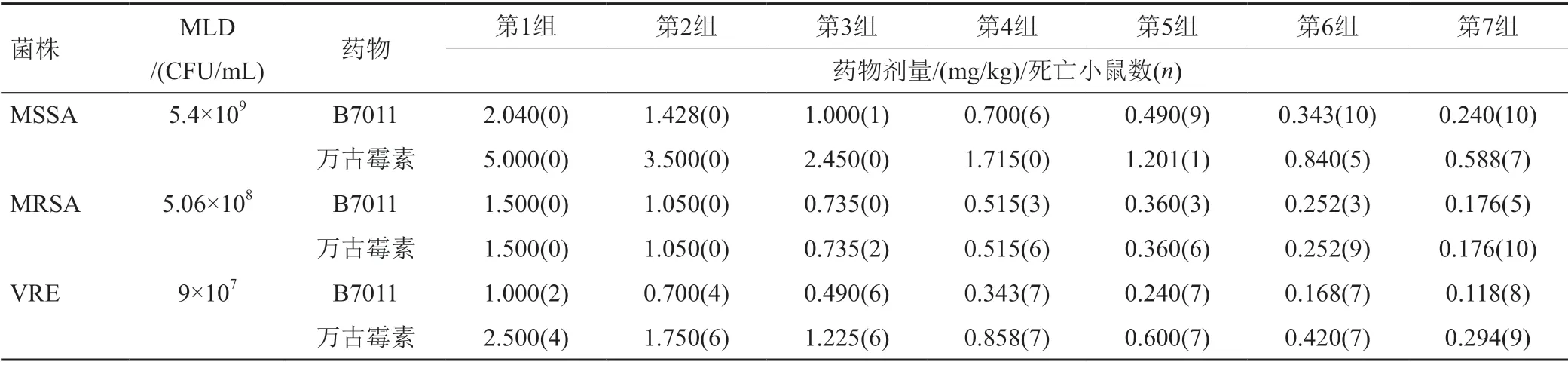
表1 对3株菌所致小鼠急性败血症模型各组给药剂量及给药后动物死亡数量表Tab.1 Drug dosage for acute septicemia induced by three strains of bacteria and mortality of animals after administration
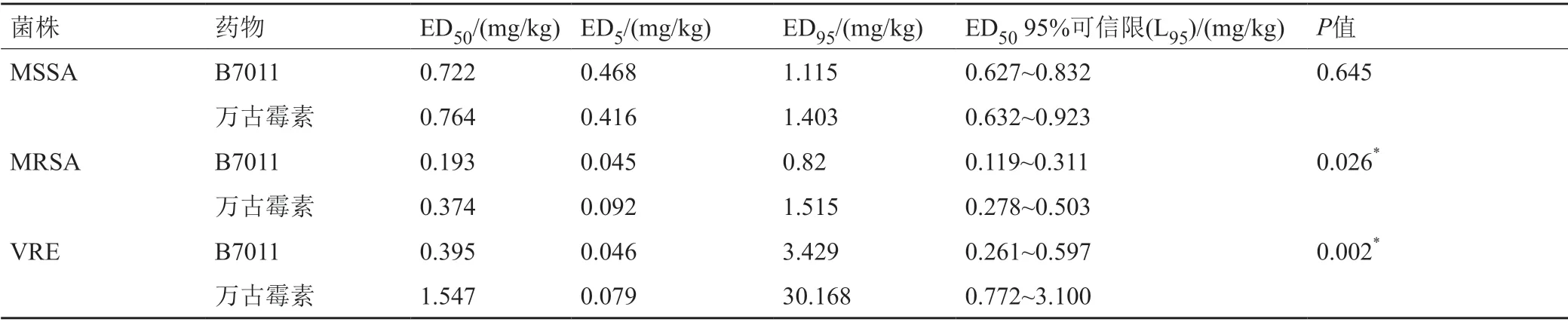
表2 B7011及万古霉素对革兰阳性球菌所致小鼠败血症模型保护作用的药效学参数Tab.2 Pharmacodynamic parameters of the protective effect of B7011 and vancomycin against systemic infections in mice caused by Gram-positive cocci
基于此,本研究开展了B7011体内抗菌作用研究。利用临床常见的革兰阳性菌急性感染ICR小鼠来制备败血症动物模型,给与不同剂量的药物,比较B7011和药性对照药万古霉素对败血症小鼠的保护作用。从已完成的ED50动物保护试验结果可以看出:B7011可以降低临床常见致病菌急性感染的败血症小鼠的死亡数量,特别是对万古霉素已经产生耐药的菌株,其保护作用尤为显著。结合体外试验数据,我们可以期待新型糖肽类抗生素B7011有望成为临床上应用于耐药菌感染的具有较好疗效的药物。目前该药已成功申请临床试验批件,将对其安全性、有效性和药动学特征等方面进行全面的研究与评估。

