正交试验法探究溴乙烷消去反应的最适条件
吴 晨 刘晓玲 黄水秀 盛寿日
江西师范大学化学化工学院(330022) 江西省上饶市上饶中学(334000)
1 背景
通过溴乙烷的消去反应去认识有机化合物官能团之间的转换是《普通高中化学课程标准》(2017年)的基本要求,然而不同版本教材涉及内容编排不尽相同。人教版教材只给出了溴乙烷的消去反应机理,并未设计演示或探究性实验;苏教版则提供了该反应的演示实验,但实验过于简单,副产物过多,收集到的乙烯量太少,定性检测不明显,往往导致课堂演示达不到预期的效果。我们在收集文献的基础上,设计了一套新的实验反应装置(如图1所示),并通过正交试验法,对溴乙烷消去反应的适宜条件进行了探究。
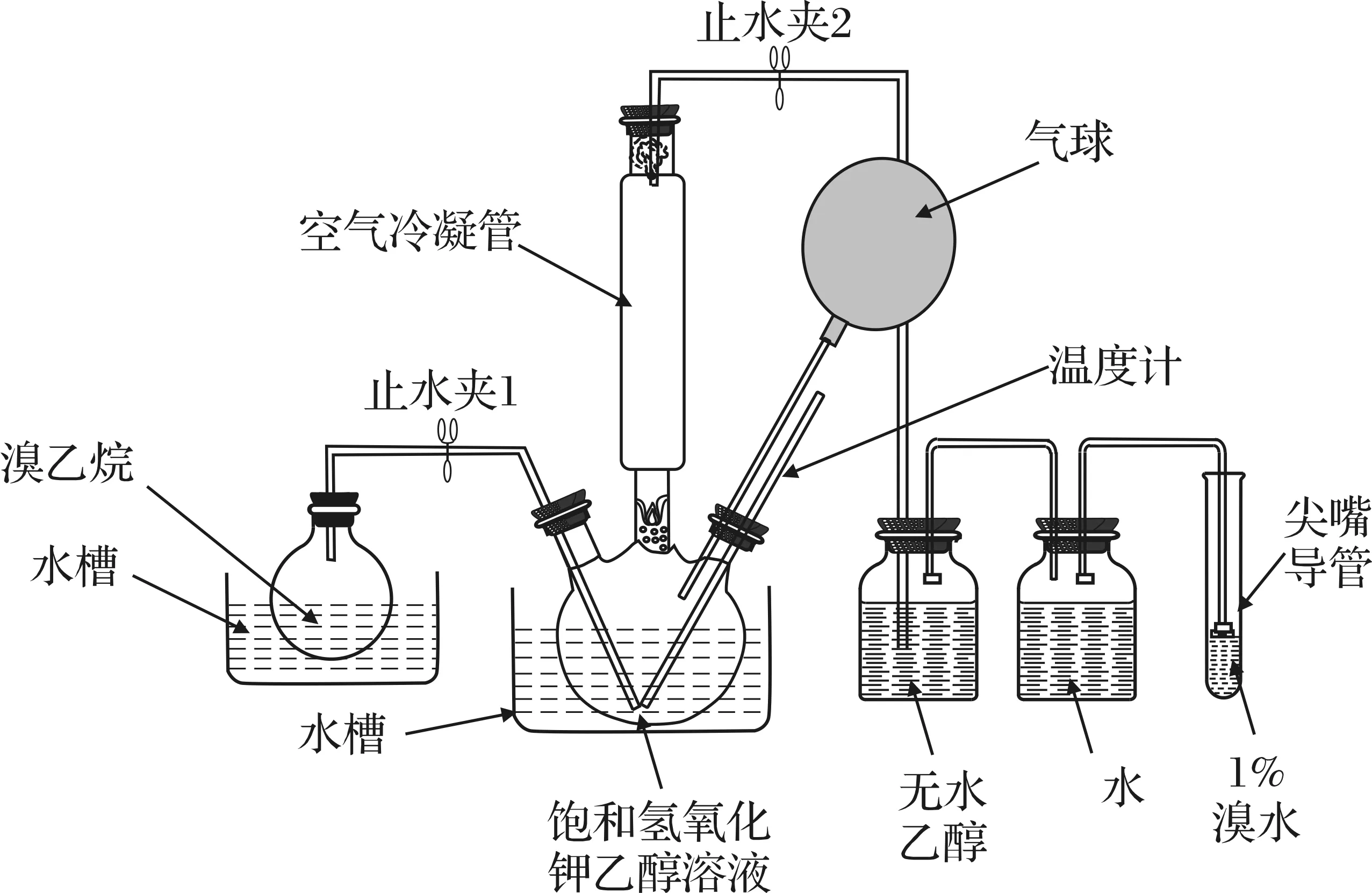
图1 实验改进装置图(验证乙烯)
由于该反应下,存在E2和SN2竞争反应,即溴乙烷消去反应与溴乙烷取代反应,所以反应中溶剂的极性以及温度都会影响乙烯的产率。为了提高该反应装置下乙烯的产率,本文将采用正交试验法,对溴乙烷消去反应的最适条件进行探究,以供同仁参考。选取反应物的量是:10 mL溴乙烷、10 mL饱和氢氧化钾、15 mL无水乙醇溶液,反应温度为90 ℃。在该装置与条件下,需要40 s时间使5 mL 1%溴水褪色。
2 因素、水平、指标的选择
溴乙烷消去反应是利用在强碱性条件下,溴乙烷脱去溴化氢,产生乙烯的过程,但溴乙烷发生消去反应是有局限性的。在溶剂极性较大、反应温度较低时,溴乙烷容易发生水解反应,由于中学实验室溶剂种类较少,所以不对溶剂种类进行探究,但可以对溶剂的用量探究。除温度与溶剂(无水乙醇)之外,原料溴乙烷与强碱氢氧化钾也是必然考虑的因素。综上,选取溴乙烷用量、反应的温度、饱和强氧化钾用量、无水乙醇用量作为正交试验的因素,每个因素选择三个水平,选择L9(34)正交试验表进行实验,见表1。

表1 溴乙烷消去反应正交试验表
3 实验装置选择
基于图1的实验改进装置,撤掉乙烯的定量检测与装有水的集气瓶装置,加入排水法收集乙烯装置,导管尾部依旧采取尖管,控制气体流速,以便除杂,如图2所示。

图2 实验改进装置图(收集乙烯)
4 实验步骤
(1)按照如图2所示装置组装仪器,检验装置气密性,按照表格要求,依次取溴乙烷于50 mL圆底烧瓶,取饱和氢氧化钾溶液于100 mL三口烧瓶,关闭止水夹1和2,在三口烧瓶下方水槽注入100 ℃热水,对氢氧化钾溶液进行预热处理。
(2)待氢氧化钾温度上升到目标温度时,取无水乙醇溶液于三口烧瓶中,当气球逐渐变大,温度计显示达到目标温度后,在圆底烧瓶下方水槽注入热水,并打开止水夹1,使溴乙烷蒸汽进入三口烧瓶中。
(3)当溴乙烷完全进入三口烧瓶中后,关闭止水夹1,反应过程,观察气球,待气球有变小的趋势时,打开止水夹2,收集气体,待气体量保持不变后,读取数值。
5 实验数据处理与分析
将获得的9组数据依次填入正交试验表中,对表中数据进行直观分析,见表2。

表2 溴乙烷消去反应正交试验表
在已选择的因素与水平中,根据均值k来确定反应的最适条件,在溴乙烷用量中,均值k2最大,即反应中溴乙烷选用8 mL;在温度大小上,均值k3最大,即反应温度为100 ℃;在强碱氢氧化钾饱和溶液用量中,均值k1最大,即反应中饱和氢氧化钾溶液选用8 mL;在无水乙醇用量上,均值k3最大,即反应中无水乙醇选用15 mL。综上所述,最适条件为A2B3C1D3(溴乙烷8 mL、饱和氢氧化钾溶液8 mL、无水乙醇15 mL、反应温度100 ℃),在此条件下,进行下一步实验,得到乙烯气体体积174 mL。
根据极差值R大小可以确定影响本实验的因素主次关系见图3。

图3 影响实验的因素主次关系图
对溴乙烷消去反应影响最大的因素是原料溴乙烷的量,但仅随其后的就是反应温度,而影响较低的是无水乙醇与饱和氢氧化钾溶液。
通过正交设计助手软件对表中数据做效应曲线图分析,如图4所示。
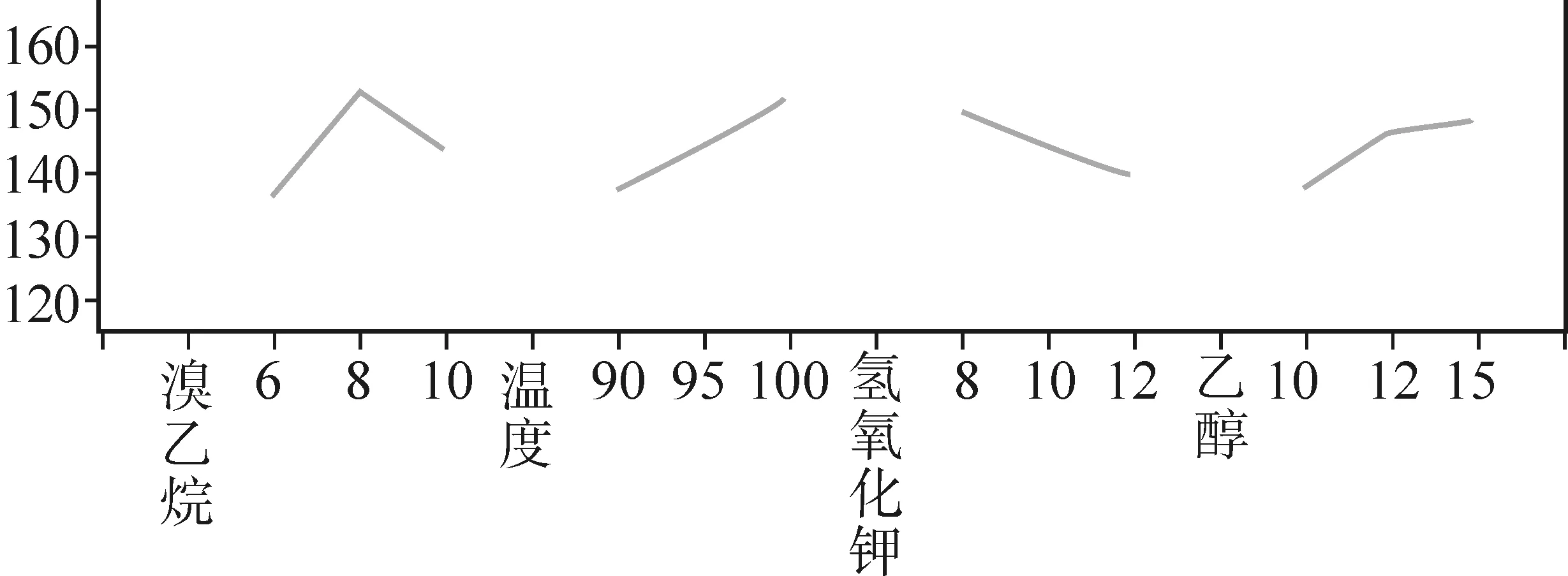
图4 效应曲线图
从效应曲线图可以看出,虽然溴乙烷的量对反应有较大的影响,但并不是投料越多越好,投料过多,反而效应偏低。其次,温度的选择和乙醇的量可以尽可能大一点。最后,氢氧化钾的量可以偏小,氢氧化钾越多反而效应越低。
6 总结
本文通过正交试验法对溴乙烷消去反应实验的最适条件进行探究,得出以下结论。
(1)在所选用的因素与水平中,最佳条件为溴乙烷8 mL、饱和氢氧化钾溶液8 mL、无水乙醇15 mL、反应温度100 ℃。
(2)4种因素对溴乙烷消去反应影响大小关系为:溴乙烷>温度>无水乙醇>饱和氢氧化钾。

