正中弓状韧带压迫腹腔干合并胰十二指肠下动脉瘤:附4例报告
毕国善 熊国祚 戴先鹏 申 昕 邓礼明 胡兵兵 罗东阳 陈 洁
(南华大学附属第二医院血管外科,衡阳 421000)
胰十二指肠下动脉瘤(inferior pancreaticoduodenal artery aneurysm,IPDAA)非常罕见[1],早期多无临床表现,一旦破裂病死率极高[2]。约有一半IPDAA合并腹腔干(celiac axis,CA)狭窄,而有30%的腹腔干狭窄是由正中弓状韧带(median arcuate ligament,MAL)压迫导致的[3]。对MAL压迫致腹腔干狭窄合并IPDAA的诊断和治疗报道较少。2017年3月~2018年6月,我院收治4例MAL压迫腹腔干合并IPDAA,本文对其进行回顾性分析,并结合文献探讨MAL压迫腹腔干伴发IPDAA的诊治策略。
1 临床资料
4例胰十二指肠下动脉瘤资料见表1。

表1 4例胰十二指肠下动脉瘤资料
CA:腹腔干;SMA:肠系膜上动脉;IPDA:胰十二指肠下动脉
例1,男,42岁,因突发上腹部疼痛、呕吐16小时入院。既往长期吸烟史,1包/天,少量饮酒,无胰腺炎、慢性腹痛、消瘦等病史。查体:脉搏(P)95次/min,血压(BP)127/86 mm Hg,上腹部压痛明显,局部存在反跳痛及肌紧张,其他无明显阳性体征。急诊腹部CTA提示:腹膜后血肿,腹腔积血;胰十二指肠下动脉(IPDA)后支动脉瘤破裂出血,大小约8 mm×6 mm,为假性动脉瘤;MAL压迫腹腔干起始部狭窄成钩形,狭窄率86%(图1A)。血红蛋白114 g/L。急诊在介入手术室行动脉造影及IPDAA弹簧圈栓塞术。以Seldinger技术穿刺右侧股动脉并置6F血管鞘,猪尾巴导管腹主动脉造影,示腹腔干起始部狭窄,IPDA后支见瘤样扩张,约12 mm×10 mm,伴造影剂外溢(图1B),腹腔干与肠系膜上动脉(superior mesenteric artery,SMA)之间可见丰富侧支动脉,RH导管(COOK,USA)选入SMA,微导管超选进入IPDA,于动脉瘤远近侧供瘤血管及瘤体内释放(2~4)mm×(4~6)cm微弹簧圈(COOK,TORNADO,USA)5枚,再次造影显示瘤体完全栓塞,无造影剂外溢,腹腔干狭窄未进行处理。术后腹痛缓解,手术时间75 min,术中未输血。术后2天排便,恢复进食,术后恢复顺利,术后10天出院。术后14个月复查CT未见动脉瘤复发。
例2,男,55岁,因上腹部疼痛5天,加重15小时入院。既往有高血压病史,最高血压182/100 mm Hg,未口服降压药物,血压控制不详;长期吸烟,10支/天,少量饮酒,无胰腺炎、慢性腹痛、消瘦等病史。于当地医院行CT检查考虑胰腺炎,治疗后未见好转,腹痛加重后转入我院。查体:P 105次/min,BP 116/72 mm Hg,贫血貌,腹肌紧张,全腹压痛、反跳痛。急诊腹部CTA提示:IPDA后支动脉瘤并破裂出血,腹膜后大量血肿,盆腔积液,腹腔干起始段狭窄,狭窄后动脉瘤扩张,狭窄率68%(图2A),大小约8 mm×6 mm,为真性动脉瘤。血红蛋白80 g/L。急诊行动脉瘤栓塞术(图2B),经SMA途径选入瘤体内,释放6枚弹簧圈栓塞动脉瘤(操作同例1)。手术时间65 min,术后腹痛腹胀缓解,术后第10天出现反复呕吐,CT提示局部血肿压迫导致十二指肠梗阻,给予胃肠减压、抗感染等对症治疗,呕吐缓解,逐渐恢复进食,术后20天出院。术后15个月复查CT未见动脉瘤复发。
例3,男,57岁,因黑便2天入消化内科,行增强CT检查发现IPDA前支动脉瘤。既往有肝炎、肝硬化、食管胃底静脉破裂出血史,无吸烟饮酒史。查体:P 85次/min,BP 132/72 mm Hg,腹部无明显阳性体征。腹部CTA提示:IPDA前支动脉瘤,大小约18 mm×15 mm,为假性动脉瘤;原发性肝癌,门静脉高压;腹腔干起始部狭窄,狭窄率92%(图3A)。血红蛋白92 g/L。行动脉瘤栓塞术(图3B),经SMA途径导管超选进入瘤体内,置入10枚弹簧圈(操作同例1)。手术时间105 min,术后腹痛腹胀逐渐消失,术后9天出院。术后13个月复查CT未见动脉瘤复发。
例4,男,81岁,因突发腹痛、恶心呕吐1天入院。既往有冠心病、高血压病史,最高血压176/90 mm Hg,长期口服尼群地平控制血压。无吸烟史,少量饮酒,既往无胰腺炎及慢性腹痛。查体:P 110次/min,BP 96/62 mm Hg,贫血貌,全腹腹肌紧张,上腹部压痛明显,有反跳痛,肠鸣音弱。腹部CT平扫提示腹膜后血肿,腹腔积液。腹部CTA提示:IPDA前支动脉瘤破裂出血,大小约13 mm×11 mm,为假性动脉瘤;腹腔干起始部狭窄,狭窄率90%(图4A)。血红蛋白60 g/L。急诊行动脉瘤栓塞术(图4B),经SMA突进无法选入瘤腔内,改为腹腔干途径置入9枚弹簧圈(操作同例1)。手术时间90 min,术中输血3单位浓缩红细胞。术后腹痛缓解,术后11天出院。术后18个月因突发心肌梗死死亡。
3 讨论
MAL是连接左右膈肌脚纤维的韧带,MAL一般位于第12胸椎水平,腹腔干上方,腹腔干发出位置过高或MAL过低均可能导致腹腔干受压,10%~24%的正常人MAL位置靠下,压迫腹腔干起始段,造成不同程度腹腔干狭窄,引起脏器缺血[4]。然而,由于腹腔干与SMA有丰富的侧支循环,绝大多数患者无不适。仅有1%的MAL压迫出现临床症状,如慢性腹痛、恶心呕吐、消瘦等,临床上称正中弓状韧带综合征(median arcuate ligament syndrome,MALS)[5]。MAL压迫还受呼吸运动的影响,当呼气时主动脉及分支向头侧移动,MAL对腹腔干的压迫会加重,而吸气时主动脉及其分支向尾侧移动,MAL对腹腔干压迫会减轻。CT血管成像(CTA)及磁共振血管成像(MRA)是MAL压迫的主要诊断依据,典型影像表现为腹腔干起始段管壁上缘锐利的“V”形凹陷,程度较重时表现为“钩状”结构。
胰十二指肠动脉由腹腔干分出的胰十二指肠上动脉和SMA分出的IPDA组成,两支动脉分成前弓和后弓相互交通,主要供应胰头和十二指肠。IPDAA在临床极为少见,早期往往无明显临床症状,多在检查中偶然发现,或发生破裂出血而就诊,约60%的IPDAA因破裂后首次就诊,一旦破裂,病死率可高达40%[6]。Shukla等[7]统计分析261例内脏动脉瘤,认为胰十二指肠动脉瘤较其他内脏动脉瘤更容易破裂,瘤体破裂直径更小。Ruhnke等[8]的研究显示,胰十二指肠动脉瘤的大小与破裂风险不成正比。因此,胰十二指肠动脉瘤一经发现,应早期积极治疗。
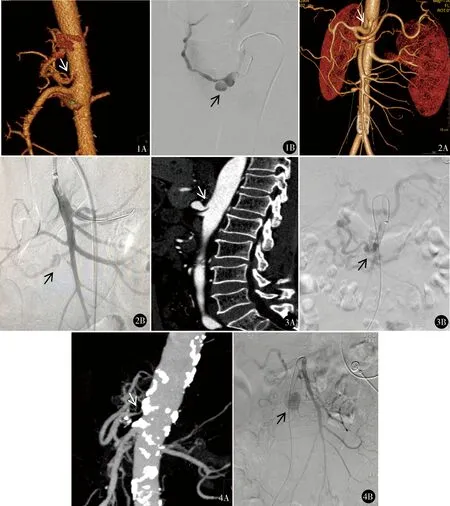
图1 例1影像学资料:A.术前CTA示腹腔干起始部明显受压狭窄,狭窄率86%;B.术中造影示动脉瘤位于胰十二指肠下动脉后支 图2 例2影像学资料:A.术前CTA示腹腔干起始部明显受压狭窄,狭窄率68%;B.术中造影示动脉瘤位于胰十二指肠下动脉后支 图3 例3影像学资料:A.术前CTA示腹腔干起始部明显受压狭窄,狭窄率92%;B.术中造影示动脉瘤位于胰十二指肠下动脉前支 图4 例4影像学资料:A.术前CTA示腹腔干起始部明显狭窄,狭窄率90%;B.术中造影示动脉瘤位于胰十二指肠下动脉前支
MAL合并IPDAA临床上极为罕见,目前国内外仅少量病例报告[7~9]。MAL压迫腹腔干导致IPDAA的原因为:由于MAL压迫导致腹腔干狭窄,血流灌注减少,SMA与腹腔干之间的侧支动脉会代偿性扩张增加血供,这些小动脉慢性持续的血流增加形成局部动脉高压,进而引起动脉壁变薄及扩张,导致动脉瘤的发生。腹腔干狭窄后胰十二指肠动脉瘤可位于侧支循环的任何部位[10]。
MAL压迫腹腔干导致的IPDAA可采用手术或介入治疗,手术包括动脉瘤切除、MAL松解和血管重建等,介入治疗包括动脉瘤栓塞、腹腔干支架植入等。开放手术MAL松解联合血管重建是治疗MAL压迫腹腔干的标准术式。韧带松解联合血管重建可明显缓解MAL综合征远期症状,但手术死亡率高达19%[11]。IPDAA介入栓塞治疗的创伤小,病死率低,尤其适用于高龄无法耐受手术者,但介入栓塞没有解除腹腔干狭窄,是否增加动脉瘤复发的风险,以及栓塞载瘤血管是否会引起内脏缺血的发生,尚不确定。因此,Nishiyama等[12]主张同期或分期重建腹腔干,避免动脉瘤复发及内脏缺血。从理论上讲,松解MAL解除腹腔干狭窄,可防止动脉瘤复发,但到目前为止,关于MAL压迫腹腔干导致胰十二指肠动脉瘤的患者,仅行动脉瘤栓塞,未进行血管重建,并未出现动脉瘤复发及内脏缺血。Sgroi等[13]认为,胰十二指肠动脉瘤是在SMA与腹腔干建立足够侧支动脉之前形成的,在动脉瘤缓慢形成的过程中,腹腔干与SMA之间有时间建立足够的侧支动脉保证肠管的血液供应,因此,仅处理动脉瘤术后一般不会出现动脉瘤复发和肠管缺血。本组4例因为术前无慢性内脏缺血表现,仅行动脉瘤栓塞,未行MAL松解及血管重建,栓塞后造影可见有足够侧支血管从SMA逆行供应肠管,术后短期随访未见动脉瘤复发,未出现内脏慢性缺血表现。这与许多文献报道一致[14,15]。
综上,MAL压迫腹腔干合并IPDAA临床少见,IPDAA破裂与动脉瘤直径不成正比,因此,一经发现应早期积极处理。结合文献报道及本组病例,MAL压迫腹腔干合并IPDAA单独处理动脉瘤是安全有效的。目前关于MAL压迫腹腔干合并IPDAA的治疗尚无共识。是否处理MAL压迫导致的腹腔干狭窄应取决于临床表现、腹腔干压迫程度和侧支循环情况。本文仅为4例的回顾性研究,仍需进一步积累病例并进行长期随访。

