新型环孢素眼用制剂的研究进展
薛 松,刘正平, ,陈倩倩,李大伟, ,王 萍
(1.山东省药学科学院,山东 济南 250101;2.山东福瑞达医药集团有限公司 山东省黏膜与皮肤给药技术重点实验室,山东 济南 250101;3.山东医药技师学院,山东 泰安 271016)
环孢素是从丝状真菌、驻孢霉菌等真菌的代谢产物中提取出来的一种环状多肽,它由11个氨基酸残基组成[1],结构见图1。环孢素的水溶性差,几乎不溶于水,易溶于氯仿、乙醚、甲醇等有机溶剂。1976年瑞士山德士公司的Borel发现环孢素具有免疫抑制作用,它可与环孢素亲和素结合成复合物从而抑制钙调神经磷酸酶。它能特异性地抑制淋巴细胞的反应和增生。对T细胞,尤其辅助T细胞(TH细胞)有选择性的抑制作用;另外环孢素还能通过抑制B细胞的增殖过程来抑制抗体的产生,从而抑制免疫系统的反应。因环孢素具有上述优异的免疫抑制作用,现为器官移植后的首选免疫抑制剂[2-4]。
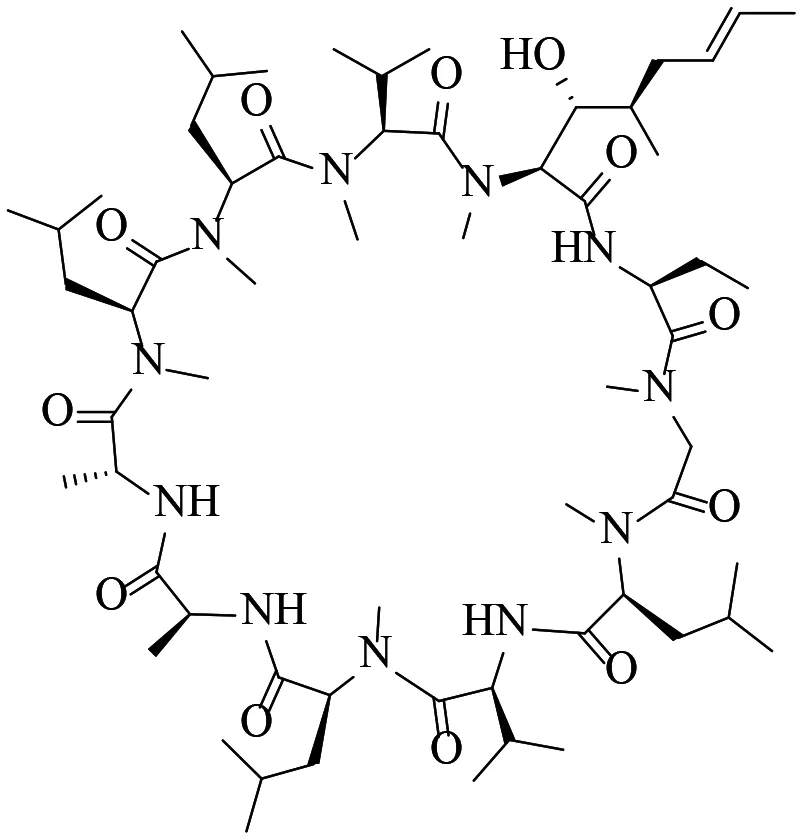
图1 环孢素结构式
环孢素主要经小肠吸收,其吸收因人而异,达峰时间为1~6 h,血液半衰期为19 h,该药物在肝脏中的分布最大,也在肝脏中经P-450催化代谢,代谢产物主要由胆汁排泄[5]。另外,由于环孢素具有较强的脂溶性,而高脂食物会增加胆汁的分泌,所以环孢素与高脂食物同服时会增加该药物的吸收。
1 环孢素眼用制剂存在的挑战
在眼部疾病的治疗中,环孢素具有广泛的应用,可用于治疗干眼症、单纯疙疹病毒性角膜炎、增殖性玻璃体视网膜病变、Behcet氏病、角膜移植后的免疫排斥反应及增殖性视网膜病变等。虽然环孢素应用广泛,但环孢素的分子量大、疏水性强(logP=3.0),生理条件下的溶解度低于10 mg/ml(0.001 %)。眼角膜有一层亲水性的基质层,所以角膜是影响环孢素生物利用度的屏障之一。
常见的环孢素制剂虽然可解决环孢素的溶解性问题,但这些制剂的生物利用度较低。目前环孢素的眼用制剂主要有环孢素油滴眼液和环孢素微乳。这类滴眼液使用时模糊感强,临床用药的顺应性差。且油制剂的辅料如花生油、蓖麻油等氧化后对眼部的刺激性大,反复使用会引起葡萄膜的反应,在眼内免疫性疾病的治疗中,该葡萄膜的反应会削弱治疗效果。油滴眼液虽能增加环孢素对角膜上皮细胞的穿透能力,但亲脂性的环孢素却难以透过亲水性的角膜基质,所以其生物利用度低,需高频次给药。
2 新型环孢素眼用制剂
为提高环孢素的生物利用度,研究者开发了多种新型眼用给药系统,其主要优缺点见图2[6]。

图2 环孢素的新型眼用制剂及其优缺点[6]
2.1 环孢素脂质体的研究
脂质体作为一种优良的载体材料,将其应用于环孢素的包载引起了人们的广泛关注。有研究表明,环孢素脂质体可使角膜移植后的存活率提高至77 %,而普通油制剂的存活率仅为45 %[7]。虽然环孢素脂质体对眼部的刺激性低于普通油制剂[8],但脂质体所能包载的环孢素较少,且在角膜表面的停留时间较短。另外脂质体的半衰期短、稳定性差[9],使用环孢素脂质体时需频繁给药。且脂质体的制备技术复杂,生产成本大,不利于实际大生产[10]。
为改进环孢素脂质体的缺点,研究者相继开发了表面阳离子化的环孢素脂质体,以提高其在角膜的停留时间,有研究发现经壳聚糖修饰的脂质体因其表面带有正电荷,能与角膜表面带负电荷的黏膜作用而延长停留时间。但随着阳离子化度的提高,载体的毒性也随之提高[11]。因此表面带有正电荷的脂质体需在载体的毒性和生物利用度之间达到一个平衡,在尽量低的毒性下实现最大的生物利用度。
2.2 环孢素纳米制剂
近年,环孢素的纳米制剂引起了人们的广泛关注。相比于传统的油滴眼液和微乳制剂,纳米制剂具有以下优势:(1)具有较好的黏膜黏附能力和穿透能力,可减少眼睛的屏障系统对药物转运的阻碍;(2)可包载疏水药物,解决药物的溶解性问题[12];(3)可实现药物的缓控释,减少给药频次;(4)在纳米制剂的表面修饰一些功能基团可帮助提高药物的生物利用度;(5)纳米制剂一般属水性清亮溶液,用药顺应性能得到极大的提高[13]。
通过溶剂挥发法制备的环孢素聚丙交酯纳米粒子载药量可高达11 %~16 %,并且环孢素的释放时间可达65 d之久[8]。Liu等[14]制备了聚乳酸-葡聚糖包载的环孢素纳米制剂,并将苯硼酸修饰至纳米制剂表面。苯硼酸可与角膜黏膜上的羟基形成硼酸酯键,从而增加该制剂在角膜表面的停留时间。实验表明修饰后的环孢素纳米制剂明显增加药物的停留时间,一周用药一次便可缓解眼部炎症。有研究将苯扎氯铵通过物理混合修饰于环孢素聚己内酯纳米粒子表面来增加其对角膜的穿透能力。经表面修饰后,该载体的生物利用度是传统的油滴眼液的10~15倍,但苯扎氯铵潜在的刺激性限制了该纳米粒子的进一步应用[15]。
2.3 环孢素胶束给药系统
最近印度太阳制药研制的全球首款环孢素纳米胶束滴眼液Cequa®通过了FDA的认证[16]。该胶束型滴眼液属于清透水剂,不含防腐剂,可提供FDA所允许的最大环孢素浓度(0.09 %),每日用药两次便可改善干眼症状。相比于目前广泛应用的环孢素滴眼液,该制剂起效早,对眼睛的刺激性小、耐受性好,用药顺应性大大提高。
2.4 环孢素原位凝胶
原位凝胶因其用药方便,能有效地提高药物的生物利用度而受到人们的关注。在眼部给药系统中,原位凝胶可借助眼部生理环境的刺激如pH、离子、温度等,发生溶胶-凝胶的转换,形成半固体状的凝胶。Ganetal等[17]制备了包载环孢素的普兰多糖原位凝胶,该原位凝胶在接触泪液后黏度迅速增大,能在眼角膜上形成一层凝胶,使得药物在角膜的停留时间大大延长,生物利用度得到了提高。聚异丙基丙烯酰胺是一种温敏性聚合物,其溶胶凝胶的转换温度为32 ℃左右。Wu等[18]将透明质酸接枝在聚异丙基丙烯酰胺上,得到了包载环孢素的原位凝胶,该原位凝胶滴到眼角膜上会在温度的改变下发生溶胶凝胶转换,形成的凝胶具有优异的生物相容性,也能提高环孢素的生物利用度。
2.5 环孢素水凝胶
水凝胶因其使用方便,也被广泛地应用于眼科药物的递送系统。在凝胶给药系统中,药物的包载是将凝胶浸泡在药物的溶液中实现的,因此在实际应用中容易产生前期药物释放过快的问题[19-20]。通过选择合适的水凝胶材料,使药物与水凝胶材料之间具有良好的相容性可解决这个问题。有研究发现硅基水凝胶材料包载的环孢素可保持两周的药物释放,而普通的水凝胶材料仅能维持几天的药物释放[21]。环孢素的水凝胶给药剂型虽能持续地释放药物,但其在眼睛表面失水变干后存在不适感,这限制了水凝胶制剂的应用。
3 结语
得益于泪膜屏障、角膜屏障、巩膜屏障等生理屏障的保护,眼球可避免外来异物的入侵。但通过局部给药的方式来治疗眼部疾病时,药物又需克服上述的屏障系统发挥药效。另外,眼睛对外界的刺激非常敏感,在开发眼部给药系统时还应当考虑所用材料对眼睛的刺激性。环孢素作为一种疏水性药物,其眼用制剂的开发除了需克服上述困难外,还需解决环孢素的溶解性问题。因此环孢素的局部眼用制剂开发更具挑战性。随着新型载体的不断涌现和制剂技术的日益提高,将能大大提高环孢素的生物利用度,实现环孢素在眼内的高效递送。

