对“比较过氧化氢在不同条件下的分解”实验的释疑及优化
张 云林 凡
(1福建教育学院理科研修部 福建福州 350001 2福建中医药大学中西医结合学院 福建福州 350122)
1 问题提出
“比较过氧化氢在不同条件下的分解”是人教版《生物·必修1》“分子与细胞”中的探究实验。该版教材沿用了传统的设计思路,以各反应体系中气泡产生数量、点燃卫生香燃烧程度,比较H2O2分别在室温、90℃、滴加2滴3.5%FeCl3溶液,以及滴加20%肝脏研磨液条件下的分解速度[1]。在教学实践中,有教师提出以下2点质疑。
①用带火星的卫生香检测90℃反应体系中生成的气体,卫生香不复燃,也不发亮,且蒸馏水在加热过程中,容器底部及壁上也能观察到大小不一的气泡。因此有教师认为:90℃反应体系中观察到的气泡不是O2气泡,而是水气泡[2]。
②在滴加FeCl3溶液的反应体系中,观察到的是细小的单气泡,气泡数量多,且以线形排列的方式出现在溶液中,而滴加肝脏研磨液的反应体系中,则在液面上方形成体积较大的群聚泡沫。不同反应体系生成的气泡大小、状态并不相同,以相同时间内气泡产生数量,作为判断O2生成速率快慢的依据是否合适?
目前,我国多省市已将数字化探究实验系统列为普通高中教育装备标准之一。该设备操作简便,能迅速检测O2浓度并转化为数字信号,使得中学阶段对氧浓度的准确测定成为可能。本文拟借助此系统对上述质疑进行释疑,并以此为基础,对原实验方案提出优化建议。
2 材料、用具及试剂
2.1 材料 新鲜的质量分数为20%猪肝研磨液、新鲜的质量分数为20%土豆研磨液。
2.2 用具 计算机、数据采集器、氧气传感器、数字化信息系统实验室软件(山东远大朗威教育科技股份有限公司)、传感器连接线、USB连接线、250 mL锥形瓶、硅胶O型圈、恒温水浴锅、电子天平、移液器及移液器吸头。
2.3 试剂 3%H2O2、0.1 mol/L FeCl3、0.1 mol/L过氧化氢酶(3 500 U/mg)。
3 实验方法
3.1 蒸馏水与3%H2O2溶液中气泡的生成 取4支洁净的试管编号(表1),分别加入蒸馏水及3%H2O2溶液,再分别置于90℃水浴与室温25℃环境中,5 min后观察试管中气泡的生成情况。
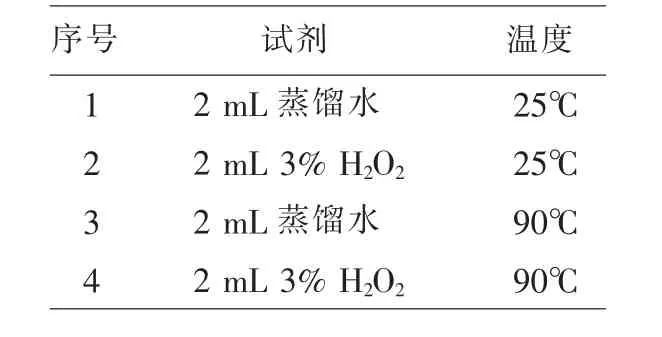
表1 蒸馏水与3%H2O2溶液中气泡的生成
3.2 H2O2在不同条件下的分解 取锥形瓶若干,编好序号(表2),依次设置反应体系(反应温度设定为25℃),用传感器连接线、USB连接线连接好氧气传感器、数据采集器及计算机,设置每间隔1 min自动采集数据。加入催化剂、研磨液(或蒸馏水),迅速将氧气传感器接于锥形瓶瓶口,并用硅胶O型圈将瓶口密封,采集数据。实验重复3次。
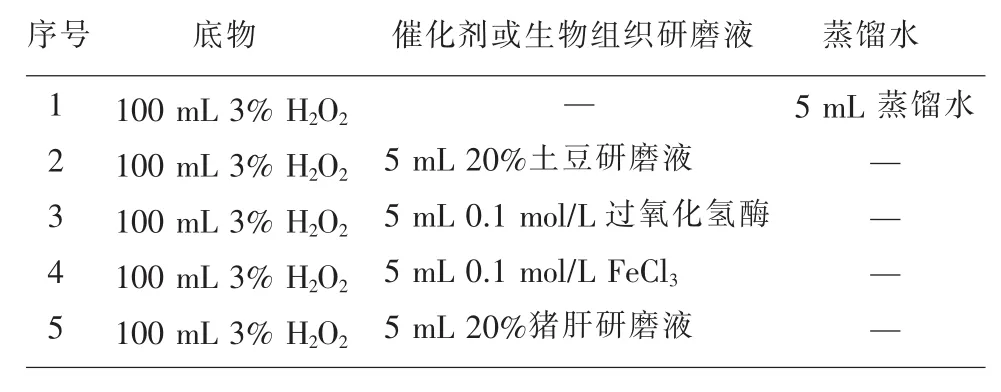
表2 H2O2在不同条件下的分解
3.3 氧浓度变化曲线的制作 以表2序号1的反应体系为对照,取3次实验平均值,用Excel软件作不同条件下氧浓度的变化曲线。
4 结果分析
4.1 蒸馏水与3%H2O2溶液中气泡的生成 表1中的1号、2号试管没有观测到明显气泡,表明在25℃条件下,1号、2号反应体系中的物质没有发生明显的物化变化;3号试管为90℃水浴中的蒸馏水,管壁上有气泡附着(图1a),与蒸馏水中溶解有部分空气、且水浴过程中部分水分子形成水蒸气有关。由此推断,4号试管(图1b)中附着于管壁上的气泡也一定含有空气或水蒸气成分。但仔细观察发现,4号试管底部另有一串体积更为细小的气泡生成,显然这才是H2O2在90℃水浴条件下分解生成的O2。为了便于观察,通常观察者会将4号试管脱离水浴环境,导致反应体系温度降低,而H2O2只有在较高的温度下才会有比较明显的分解[3],因此串珠状的O2气泡的生成会在较短的时间内变缓甚至消失,而容易造成没有O2生成的错觉。可见,认为90℃反应体系中观察到的气泡不是O2气泡,是由于仅观察到了附着于管壁的气泡而做出的错误判断。
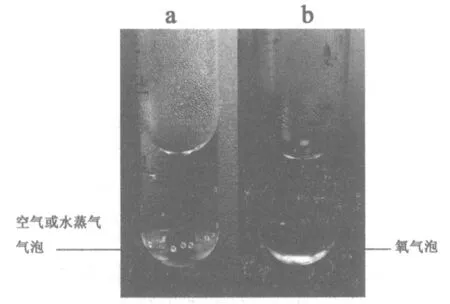
图1 90℃水浴中的H2O2与蒸馏水生成的气泡
4.2 H2O2在不同条件下的分解 如图 2,3%H2O2溶液加入含有过氧化氢酶的生物组织研磨液(2、5号)或纯酶液(3号)后,各锥形瓶中液面上均有明显的群聚泡沫生成,而加入FeCl3的4号锥形瓶液面上仅出现少量聚集气泡,同时4只锥形瓶溶液中均可见不断生成的细小气泡,这些现象显然与上述反应体系中的H2O2分解生成了O2有关。从泡沫生成多寡来看,反应10 min时,5号(猪肝研磨液)生成的最多,3号(0.1 mol/L 过氧化氢酶)、2号(土豆研磨液)次之,最少的则是 4号(0.1 mol/L FeCl3)。 但以氧气传感器收集的数据分析,此时锥形瓶中氧气浓度最高的并非5号(猪肝研磨液,平均 O2浓度为 27.8%),而是 4号(FeCl3,平均O2浓度为 29.6%),且泡沫量次之的3号(0.1 mol/L 过氧化氢酶)平均 O2溶度(28.6%),也高于泡沫量最多的5号(猪肝研磨液)。有报道表明,蛋白质是一种助泡物,其吸水后能形成水凝胶性质的表面膜,有助于溶液中泡沫的生成与稳定[4]。上述各实验组反应体系中的蛋白质组分不同,对泡沫现象的影响不可忽视,即反应体系中O2生成量并非决定泡沫量的唯一因素。因此,相同时间内反应体系中可见泡沫的多寡不足以说明体系中O2生成速率的快慢。

图2 H2O2在不同条件下的分解(反应10 min)
此外,在教学实践中,由于溶液内部生成的气泡处于上升状态,导致观察者无法从数量上对其作出准确判断,因此会仅以液面上方已经形成的泡沫量为观察指标,而略去了对上升气泡的数量统计。但从图3可见,在反应开始的60 min内,生成的泡沫量并不同的3、4、5号锥形瓶,O2浓度变化曲线却基本吻合,可见上升气泡所携带的O2量也是不容忽视的关键因素。因此,在H2O2分解过程中,试图通过视觉观察而对O2生成量的多寡做出大致判断是无法实现的,以“气泡产生数量”为本实验观测比较的指标,科学性不够充分。

图3 不同条件下氧浓度变化曲线
5 实验优化的必要性及可行性
此外,原实验设计中另一个观测指标“点燃卫生香的燃烧程度”,易受卫生香干燥程度、反应温度、肝脏研磨液新鲜程度等因素的影响[5],加之反应体系中有H2O生成,引起反应体系上层空间湿度增加,点燃的卫生香通常并不容易燃烧[6]。可见,此指标受无关变量影响的可控性较差,实验现象不稳定。因此,以传统实验思路进行的“比较过氧化氢在不同条件下的分解”,实验设计存在缺陷,无法很好地帮助学生达成对相关概念的生成与理解。
2018年教育部颁布了 《普通高中生物学课程标准(2017年版)》,新课程标准在“加强和完善生物学实验教学”的实施建议中明确指出:教师应注意实验设计多样化;在重视定性实验的同时,也要重视定量实验,让学生在量的变化中了解事物的本质[7]。已有研究表明,在中学生物学教学中设计一些定量实验,不仅可帮助学生树立“量化”意识,学会用数据表达实验结果的科学方法和严谨的科学态度,还可探寻各因素之间的量化关系,进行逻辑思维的训练[8]。同时,伴随着数字化探究实验系统在基础教育领域的推广与运用,使得在高中阶段以定量实验的思路优化该实验成为可能。
6 优化的建议及方案
综上分析,建议在教学实践中,结合数字化探究实验系统实施“比较过氧化氢在不同条件下的分解”实验。表3是笔者提出的实验方案,以供参考。

表3 “比较过氧化氢在不同条件下的分解”实验方案

