2型糖尿病对Ⅳ期肺癌患者生存期的影响研究
程小龙,韩一平,叶建花
目前肺癌是全球范围内发病率及肿瘤相关死亡率均最高的恶性肿瘤,占所有癌症相关死亡人数的27%,估计每年有220万例新发病例和160万例死亡病例[1]。随着经济的高速发展,生产、生活方式及饮食结构的改变,近30多年来我国糖尿病(DM)的发病率显著上升,1994年为 2.4%[2],2007—2008年上升到 9.7%[3],2013年已经达10.9%,DM前期状态更是达到了35.7%[4],其中绝大部分为2型糖尿病(T2DM)。肺癌和DM发病率均随年龄增长而升高,随着人口老龄化进程加剧,临床上两病共存的现象越来越常见。有研究表明T2DM可能通过高糖血症、慢性炎性反应以及高胰岛素/胰岛素样生长因子1(IGF-1)等机制促进肿瘤细胞增殖及转移[5-6]。然而也有研究表明,血管基底膜细胞外基质经DM所致的糖基化终产物修饰后可阻碍肺癌细胞的侵袭性转移,从而延缓肺癌进展[7]。本研究旨在探讨T2DM对Ⅳ期肺癌患者生存期的影响,以期为此类患者的综合健康管理提供参考。
1 对象与方法
1.1 研究对象 检索海军军医大学附属长海医院病案管理系统,选取2011—2015年海军军医大学附属长海医院呼吸内科收治的Ⅳ期肺癌合并T2DM患者52例作为观察组,同期Ⅳ期肺癌不合并T2DM患者63例作为对照组。纳入标准:观察组患者需满足以下条件中的(1)~(8),对照组患者需满足以下条件中的(1)~(6):(1)年龄≥18岁;(2)通过组织或细胞学标本,明确肺癌诊断;(3)根据第八版肺癌TNM分期系统[8],明确肿瘤分期为Ⅳ期;(4)接受一线含铂类双药联合方案化疗;(5)既往无其他肿瘤病史;(6)既往未接受过放化疗;(7)肺癌确诊时间晚于T2DM确诊时间;(8)T2DM患者为内分泌科专家诊断明确者。本研究经海军军医大学附属长海医院伦理委员会审核,所有患者及其家属对本研究知情同意并签署知情同意书。
1.2 观察指标 收集两组患者性别、年龄、吸烟史、其他慢性疾病(如高血压、高脂血症、心脑血管疾病等)史、病理类型〔包括小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC)〕。
本研究意义:
肺癌和2型糖尿病是两大常见的慢性非传染性疾病,随着人口老龄化现象的加剧,目前临床上两病共存的现象越来越普遍。大多数肺癌被诊断时已属晚期,失去了根治性手术的机会。已有部分研究表明,合并糖尿病可能对肺癌等恶性肿瘤的预后产生影响,但结论仍存在争议。本研究通过对接受标准方案化疗的Ⅳ期肺癌患者进行预后分析,旨在探讨合并2型糖尿病对Ⅳ期肺癌患者预后的影响,以期为此类患者的综合健康管理提供新的思路。
1.3 治疗及随访 两组患者均接受一线含铂类双药联合方案化疗并对两组患者进行电话随访,每3个月随访1次,随访截止时间为2018-01-30。记录两组患者无进展生存期(PFS)和总生存期(OS),其中PFS指从肺癌确诊时间至出现疾病进展(PD)时间或死亡时间或最后一次随访时间或随访截止时间;PD指靶病灶最大径之和至少增加≥20%,其绝对值增加≥5 mm,或出现新病灶,需经至少1名呼吸科专家或影像学专家确认。OS指从肺癌确诊时间至患者死亡时间或最后一次随访时间或随访截止时间。
1.4 统计学方法 采用SPSS 21.0软件进行统计学分析,符合正态分布的计量资料以(x±s)表示,两组间比较采用两独立样本t检验;计数资料分析采用χ2检验;Ⅳ期肺癌患者生存期的影响因素分析采用Kaplan-Meier法和多元Cox回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较 观察组患者男性比例、有吸烟史及其他慢性疾病史者所占比例高于对照组,年龄大于对照组,差异有统计学意义(P<0.05);两组患者病理类型比较,差异无统计学意义(P>0.05,见表1)。
2.2 T2DM对Ⅳ期肺癌患者PFS的影响 对照组患者PFS为13〔95%CI(9,17)〕个月,观察组为8〔95%CI(6,9)〕个月;两组患者PFS比较,差异无统计学意义(χ2=2.23,P=0.14,见图1)。以PFS为因变量,以性别(赋值:男=1,女=2)、年龄(实际值)、吸烟史(赋值:有=1,无=2)、其他慢性疾病史(赋值:有=1,无=2)、病理类型(赋值:SCLC=1,NSCLC=2)、T2DM(赋值:有=1,无=2)为自变量进行多元Cox回归分析,结果显示,性别、年龄、吸烟史、其他慢性疾病史、病理类型、T2DM不是Ⅳ期肺癌患者PFS的影响因素(P>0.05,见表2)。

表1 两组患者一般资料比较Table 1 Comparison of general information between the two groups
2.3 T2DM对Ⅳ期肺癌患者OS的影响 对照组患者OS为36〔95%CI(28,43)〕个月,观察组为18〔95%CI(15,22)〕个月,对照组患者OS长于观察组,差异有统计学意义(χ2=14.95,P<0.01,见图2)。以OS为因变量,以性别(赋值:男=1,女=2)、年龄(实际值)、吸烟史(赋值:有=1,无=2)、其他慢性疾病史(赋值:有=1,无=2)、病理类型(赋值:SCLC=1,NSCLC=2)、T2DM(赋值:有=1,无=2)为自变量进行多元Cox回归分析,结果显示,其他慢性疾病史、T2DM是Ⅳ期肺癌患者OS的影响因素(P<0.05,见表3)。
3 讨论
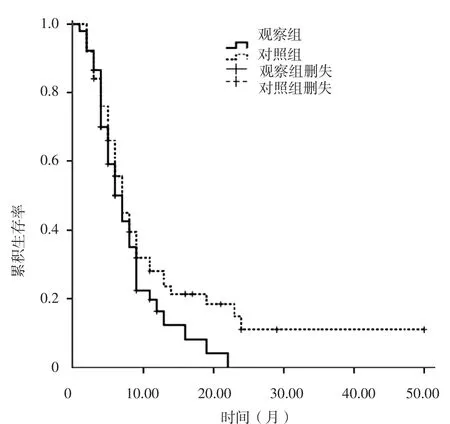
图1 两组患者PFS的生存曲线比较Figure 1 Comparison of survival curve for PFS between the two groups

表2 Ⅳ期肺癌患者PFS影响因素的多元Cox回归分析Table 2 Multivariate Cox regression analysis on influencing factors of PFS in patients with stage Ⅳ lung cancer

表3 Ⅳ期肺癌患者OS影响因素的多元Cox回归分析Table 3 Multivariate Cox survival regression analysis on influencing factors of OS in patients with stage Ⅳ lung cancer
早在1932年WILSON就注意到T2DM可能增加多种恶性肿瘤发病风险[9],但直到最近10多年才有较多的流行病学资料显示合并DM可以增加肝癌、胰腺癌、子宫内膜癌、结直肠癌、乳腺癌及膀胱癌等多种恶性肿瘤发病风险[10],但目前有关T2DM与肺癌预后之间关系的研究资料相对较少,且结论缺乏一致性。

图2 两组患者OS的生存曲线比较Figure 2 Comparison of survival curve for OS between the two groups
本研究通过对115例接受一线含铂类双药联合方案化疗的Ⅳ期肺癌患者(其中合并T2DM者52例,不合并T2DM者63例)进行预后分析,结果显示,T2DM是Ⅳ期肺癌患者OS的危险因素,但T2DM与Ⅳ期肺癌患者PFS无显著相关性。本研究结论与近期一项Meta分析[11]结论相一致,该研究共纳入16 354例肺癌患者,其中14 643例患者用于研究DM对患者OS的影响,1 711例患者用于研究DM对患者PFS的影响,结果显示合并DM明显缩短肺癌患者的OS,而对患者的PFS无明显影响。LUO等[12]和IMAI等[13]研究也表明合并DM可降低肺癌患者的长期生存率。
虽然部分流行病学资料提示DM可能促进肺癌的发生发展[9-13],增加患者的死亡风险,但确切的生物学机制尚未完全明确。高糖血症、高胰岛素血症、慢性炎性反应以及肿瘤细胞的代谢异常等被认为是促进肺癌发生发展的潜在生物学机制[14-15]。恶性肿瘤的代谢特点为以无氧酵解为主的高葡萄糖代谢率,即Warburg现象[16],而DM患者能满足恶性肿瘤快速生长所需的高糖环境,高糖状态诱发氧化应激反应,产生过氧化物,导致小血管及大血管并发症,同时可损伤DNA结构,增加基因突变率或肿瘤相关基因的表达。HAN等[17]研究表明,高血糖还可以通过增加表皮生长因子(EGF)表达并反式激活EGF受体(EGFR)而促进肿瘤细胞增殖。DE ROSA等[18]进一步研究发现,EGF旁路与肿瘤细胞代谢相关,抑制该旁路与针对性降糖治疗可通过逆转NSCLC的Warburg现象及再激活氧化磷酸化反应而产生协同抗肿瘤效应。WILKY等[19]研究发现,高糖血症与肿瘤细胞代谢异常均可加速肿瘤细胞的增殖。
绝大多数DM为T2DM,以胰岛素抵抗为其主要病理特点,进而导致胰岛素反馈性分泌增多,血液中胰岛素浓度增高。胰岛素可干扰胰岛素样生长因子结合蛋白在肝脏的合成,从而使血液循环中游离的具有生物活性的胰岛素样生长因子1(IGF-1)水平升高,并促进IGF-1受体(IGF-1R)表达,胰岛素与IGF-1被认为是促进肿瘤发生发展的重要因素,胰岛素受体与IGF-1R激活有促进细胞有丝分裂、抑制细胞凋亡、诱导新生血管形成等效应[16,20]。DM或肥胖相关的慢性炎性反应在肿瘤的形成到转移的每一个环节中均起作用。DM相关的炎性反应由肿瘤坏死因子α(TNF-α)、核因子κB(NF-κB)、信号传导及转录激活因子3(STAT3)和脂肪因子等炎性细胞或炎性因子介导[10,14,21-22],特别是STAT3被认为是NSCLC患者预后的预测指标,STAT3与NSCLC细胞系对细胞毒性药物的敏感性有关,STAT3 mRNA高表达预示肿瘤细胞对铂类化疗药物耐药性高,相反STAT3 mRNA表达沉默提示肿瘤对治疗反应性良好,因此STAT3可能是肺癌对一线化疗敏感的良好预测因子[23]。此外,合并DM患者产生化疗相关毒副作用的风险可能明显升高,如中性粒细胞降低、感染等[24]。MELLEMGAARD等[25]研究发现,合并其他慢性疾病的肺癌化疗患者预后较差,且合并症越多影响越大(P=0.002)。本研究结果显示,观察组患者中有其他慢性疾病史者所占比例高于对照组,且多元Cox回归分析结果提示其他慢性疾病史是Ⅳ期肺癌患者OS的独立危险因素之一。
本研究结果显示,两组患者PFS比较无统计学差异,且多元Cox回归分析结果显示T2DM不是Ⅳ期肺癌患者PFS的影响因素,与 HANBALI等[26]、ZHU等[11]研究结果一致,这可能与晚期接受化疗的肺癌患者PFS常较短,而T2DM的各种病理机制对肺癌病程进展的影响需要一定时间的积累才能完全体现出来有关。
需要注意的是,目前T2DM对肺癌患者预后影响的研究结论并不一致,另外一部分学者发现合并DM的肺癌患者生存期与未合并DM者相当甚至更长[26-27]。BARTLING等[28]认为,DM血管病变可能是肺癌细胞迁移及侵袭性生长的屏障,可延缓其转移。在一项纳入55例合并DM的肺癌患者及111例非DM肺癌患者的研究中发现,DM组患者20个月生存率高于非DM组,而两组患者60个月生存率比较无统计学差异。出现上述差异的原因可能与未统一研究人群、治疗方案、终点事件不明确等因素有关。
综上所述,T2DM及其他慢性疾病史是一线含铂类双药联合方案化疗的Ⅳ期肺癌患者OS的影响因素,但T2DM并非此类患者PFS的影响因素,因此对于Ⅳ期肺癌患者,需全面评估其整体健康状况,制定合理的个体化治疗与管理策略,注重对T2DM及其他慢性疾病的管理,以延长患者生存期;但本研究尚存在一些不足:第一,本研究是一项小样本量、单中心回顾性研究;第二,未评估T2DM病程、血糖控制情况及降糖药物使用情况对预后的影响;第三,可能存在选择偏倚,因为部分潜在的T2DM患者未被确诊。
作者贡献:程小龙进行文章的构思与设计,数据收集及整理,统计学处理,结果的分析与解释,撰写论文;叶建花进行研究的实施与可行性分析,负责文章的质量控制及审校,对文章整体负责,监督管理;韩一平进行论文修订。
本文无利益冲突。

