健阴栓微生物限度检查方法适用性试验及体外抑菌作用研究
张明君,哈丽旦·苏莱曼,李海芳
(新疆维吾尔自治区食品药品检验所药理与微生物检验室,新疆 乌鲁木齐830004)
中成药健阴栓主要由没食子、石榴花、枯矾、儿茶和石榴皮等5种药材组成,按照维吾尔医学理论,该药具有清除异常黏液质、消炎、收敛、燥湿和清热解毒的功效,临床拟用于治疗女性宫颈炎、湿性白带增多、宫颈肥大、滴虫阴道炎及细菌性阴道病等病症。中药栓剂是以中药饮片为原料,经现代化工艺提取而成,与适合的基质混合而成,专供腔道用药的固体制剂,具有携带方便、质量稳定、安全有效和药效持久等特点[1]。为了加强对健阴栓的质量控制,本研究进行了该药的微生物限度检查方法适用性试验及体外抑菌作用研究,为其临床应用提供可靠的理论依据。
1 材料
1.1 仪器
LDZX-50KBS型立式压力蒸汽灭菌器(上海申安医疗器械厂),EL500S型电子天平(常州市天之平设备有限公司),WDP-9272型电热恒温培养箱(上海安亭科学仪器有限公司),QS-PY150型智能生化培养箱(上海奇珊电子科技有限公司),一次性接菌环、一次性L涂布棒(BIOLGIX公司)等。
1.2 药品与试剂
健阴栓(新疆维吾尔自治区维吾尔医药研究所,规格:3 g/个,批号:170960、170961及170962)。pH 7.0氯化钠-蛋白胨缓冲液(批号:20160723)、胰酪大豆胨液体(批号:20170504)、胰酪大豆胨琼脂(批号:20170623)、沙氏葡萄糖液体(批号:20160921)、沙氏葡萄糖琼脂(批号:20170523)、甘露醇氯化钠琼脂(批号:20150804)、溴化十六烷基三甲胺琼脂(批号:20151216)、梭菌增菌培养基(批号:20170215)、哥伦比亚琼脂(批号:20161103)、念珠菌显色培养基(批号:20160723)及硫乙醇酸盐流体培养基(批号:20160817)均购于青岛高科园海博科技有限公司;0.9%氯化钠溶液(自配);上述培养基与试剂均经过121 ℃高压灭菌后,冷却至45 ℃左右备用。
1.3 菌株
大肠埃希菌[菌号:CMCC(B)44102]、金黄色葡萄球菌[菌号:CMCC(B)26003]、枯草芽孢杆菌[菌号:CMCC(B)63501]、铜绿假单胞菌[菌号:CMCC(B)10104]、生孢梭菌[菌号:CMCC(B)64941]、白色念珠菌[菌号:CMCC(F)98001]和黑曲霉[菌号:CMCC(F)98003],均购于中国食品药品检定研究院,菌株均为第3代。
2 方法与结果
2.1 菌株活化及菌液制备
将冻存于-80 ℃冰箱中的菌株取出,放至室温(25 ℃)下融化,将大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌及铜绿假单胞菌均各取1环,接于胰酪大豆胨液体中,放入33 ℃培养20 h;生孢梭菌接于硫乙醇酸盐流体培养基中,放入33 ℃培养箱中20 h;白色念珠菌取1环接于沙氏葡萄糖液体中,放入23 ℃培养箱20 h。取出活化好的菌株,用0.9%氯化钠溶液制成含菌数<100 cfu/ml的菌悬液,备用。取经25 ℃培养5 d的黑曲霉斜面培养物,制成含孢子数<100 cfu/ml的孢子悬液备用。
2.2 微生物限度检查方法适用性试验
2.2.1 供试液的制备:取样品10 g,加入至含2%吐温80的pH为7.0的氯化钠-蛋白胨缓冲液100 ml中,得到1∶10供试液备用。
2.2.2 需氧菌总数、霉菌及酵母菌总数计数方法适用性试验:(1)平皿法。取1∶10的供试液10 ml,加入制备好的菌液0.1 ml,混合均匀。取含菌的供试液1 ml置于平皿中,注入相应琼脂培养基,置规定温度中培养48 h,观察结果。(2)薄膜过滤法。取1∶10的供试液10 ml过滤,用pH为7.0的氯化钠-蛋白胨缓冲液500 ml分5次冲滤膜,在最终1次冲洗液中加入≤100 cfu/ml的菌株1 ml过滤,取出滤膜,菌面朝上,贴于琼脂培养基平板上,至规定温度中培养48 h观察结果。
2.2.3 控制菌检查方法适用性试验:(1)金黄色葡萄球菌。取1∶10的供试液10 ml,用薄膜过滤法冲洗500 ml/膜,再接种至100 ml胰酪大豆胨液体中,33 ℃培养18 h,取胰酪大豆胨液体培养物,划线接种于甘露醇氯化钠琼脂平板上,33 ℃培养18 h。(2)铜绿假单胞菌。取1∶10的供试液10 ml,接种至100 ml胰酪大豆胨液体培养基中,33 ℃培养18 h,取胰酪大豆胨液体培养物,划线接种于溴化十六烷基三甲胺琼脂平板上,33 ℃培养18 h。(3)梭菌。取1∶10的供试液10 ml,接种至100 ml梭菌增菌培养基中,33 ℃厌氧培养48 h,再划线接种于哥伦比亚琼脂平板上,33 ℃厌氧培养48 h。(4)白色念珠菌。取1∶10的供试液10 ml,加至100 ml沙氏葡萄糖液体培养基中,33 ℃培养3 d,划线接种于沙氏葡萄糖琼脂平板上,33 ℃培养24 h,挑取菌落至念珠菌显色培养基上,33 ℃培养24 h,符合《中华人民共和国药典:四部》(2015年版)的要求。
2.2.4 结果:测定健阴栓的需氧菌总数、霉菌和酵母菌总数计数的回收比,进行3次平行试验(见表1—2),回收比均在0.5~2之内。表明健阴栓需氧菌总数计数可采用1∶10的供试液按照平皿法测定,霉菌及酵母菌总数计数可采用薄膜过滤法冲洗液500 ml/膜测定;控制菌检查均可采用常规法。
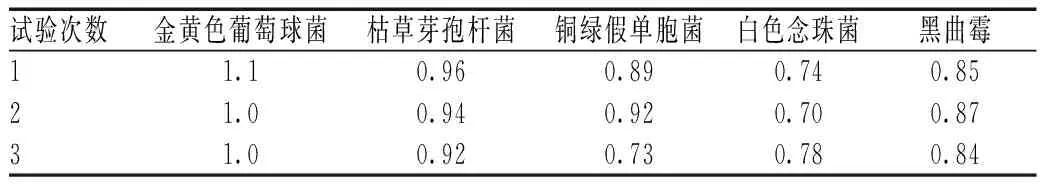
表1 健阴栓微生物限度检查法需氧菌总数回收比(1∶10供试液)Tab 1 Recovery ratio of aerobic bacteria count in the microbial limit test (1∶10 test solution) of Jianyin suppository

表2 健阴栓微生物限度检查法霉菌及酵母菌总数回收比(1∶10供试液)Tab 2 Recovery ratio of mold and yeast count in the microbial limit test (1∶10 test solution) of Jianyin suppository
2.3 体外抑菌作用
2.3.1 供试液的制备:取样品20 g,加入至pH为7.0的氯化钠-蛋白胨缓冲液20 ml中,充分溶解并混匀,得到供试液(1 g/ml)备用。
2.3.2 最低抑菌浓度(MIC)的测定:采用试管二倍稀释法[2]分别测定样品对大肠埃希菌、金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌和白色念珠菌的MIC。即在无菌条件下,取小试管11支,按照1—11编号,排列于试管架上;2—10号的试管分别加入胰酪大豆胨液体或沙氏葡萄糖液体1 ml,取制备好的供试液2 ml,加至1号试管中混匀,从1号试管中吸取1 ml放入2号试管中,同样混匀后吸出1 ml放入3号的试管;同法进行,稀释至8号的试管。从8号试管中,取出1 ml于11号的空试管中作为空白对照;第10号的试管中,加胰酪大豆胨液体或沙氏葡萄糖液体0.5 ml与pH为7.0的氯化钠-蛋白胨缓冲液0.5 ml作为稀释剂对照;第9号的试管不加供试液,作为阳性对照。在第1—10号的试管中,分别加入含菌数为103~105CFU/ml菌悬液0.1 ml,连同第11号的试管一同放入培养箱,培养24 h。再从每个试管中,各取1接菌环,划线接种于胰酪大豆胨琼脂或沙氏葡萄糖琼脂平板上,放入培养箱,培养24 h。观察琼脂平板上菌落的生长情况。在划有阳性对照与稀释剂对照的琼脂平板上的菌落应生长良好;而空白对照管的琼脂平板上无菌落生长的前提下,观察划有第1—8号的试管琼脂平板上菌落生长的情况,以无菌落生长的最低供试液浓度为该样品的MIC[3-4]。
2.3.3 最低杀菌浓度(MBC)的测定:于健阴栓供试液有效抑菌浓度的试管(即有菌生长的试管)中,供试液与对照组对应的试管培养基中,分别取溶液0.1 ml,涂布至相应胰酪大豆胨琼脂或沙氏葡萄糖琼脂平板上,用L涂布棒均匀轻推供试液,再将平板培养24 h。观察琼脂平板上有无菌落生长,以平板上计数<5个的菌落供试液浓度作为该样品的MBC[5]。
2.3.4 结果:健阴栓供试液0.007 8~1.000 0 g/ml对大肠埃希菌和白色念珠菌均无抑菌作用,划线平板上均有菌落生长。而该供试液对其余3种菌株均显示出不同程度的抑菌作用,其中对金黄色葡萄球菌的MIC为0.25 g/ml,MBC为0.5 g/ml;对铜绿假单胞菌的MIC和MBC均为0.25 g/ml;对枯草芽孢杆菌的MIC和MBC均为0.25 g/ml,见表3—4。

表3 健阴栓体外抑菌作用结果Tab 3 Results of bacteriostasis in vitro of Jianyin suppository
注: “+”表示有菌落生长,“-”表示无菌落生长,“①”表示MIC;“②”表示MBC
Note: “+” means colony growth, “-” means no colony growth, “①”indicates MIC; “②”indicates MBC
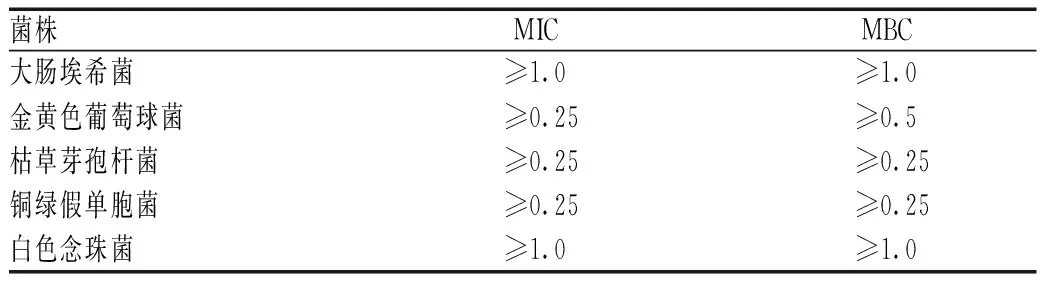
表4 健阴栓对各菌株的MIC和MBC(g/ml)Tab 4 MIC and MBC values of Jianyin suppository against each strain (g/ml)
3 讨论
参考相关研究结果,本研究进行了健阴栓微生物限度检查方法适用性试验,并初步测定了体外抑菌作用的相关数据,以确保该药在临床应用上更加准确、有效[6-7]。本研究结果显示,健阴栓对金黄色葡萄球菌、枯草芽孢杆菌和铜绿假单胞菌均有抑制作用,对大肠埃希菌和白色念珠菌无抑制作用,且其对铜绿假单胞菌和枯草芽孢杆菌的抑制作用优于金黄色葡萄球菌。
体外抑菌作用试验方法包括试管二倍稀释法、平板打孔法及纸片扩散法等。本研究采用试管二倍稀释法及琼脂平板法结合,更为准确可靠。中成药大多含有多种中药材,成分较为复杂,其供试液的颜色一般较深且浑浊,影响试验结果观察,无法准确判断试管中有无菌落生长[8-9];在药品的处理方法中,有机溶剂的使用可能会影响药品的真实抑菌作用,因此,本研究联合2种方法进行体外抑菌作用试验,可有效避免药物成分被破坏,保证健阴栓抑菌作用结果的准确性。微生物的污染监控是药品质量与安全的重要指标[10-12],应建立准确可靠的微生物限度检查方法,有效地消除其抑菌的成分[10]。
引起宫颈炎、阴道炎的病原体除了淋球菌、支原体、衣原体、滴虫和念珠菌等外,还有金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌及白色念珠菌等病原微生物[13]。健阴栓拟用于细菌性阴道病等病症。本研究结果表明,健阴栓对以上部分病原微生物的生长均有一定的抑制作用,说明其具有良好的抑菌及杀菌作用,但具体作用机制还有待于进一步的研究。

