急诊经胸心脏超声对A型急性主动脉综合征诊断价值的临床研究
练 睿,闫圣涛,张素巧,高 文,张国强
(中日友好医院 急诊科,北京 100029)
急性主动脉综合征(acute aortic syndrome,AAS)又称为急性胸痛综合征,它包括一组有相似临床症状的异质性疾病:主动脉夹层(AD),壁内血肿(IMH),穿透性动脉粥样硬化性溃疡(PAU)。该组疾病由Vilacosta和San Roman于2001年首先提出[1],这是一组严重威胁生命的主动脉疾病,按照经典主动脉夹层Stanford分型,有学者提出将累及升主动脉的 AD、PAU、IMH统称为A型AAS。强调这一分型的原因在于此类主动脉疾病起病凶险,预后极差[2],有研究表明在没有治疗的最初48h内每小时的病死率高达l%,2周的病死率高达80%[3]。目前常用的诊断方法包括CT血管成像(computed tomography angiography,SCTA),磁共振成像(magnetic resonance imaging,MRI)等,均具有较高的诊断价值,但部分危重患者转运至放射科具有较高医疗风险或部分患者对CT造影剂过敏或体内带有金属植入物,无法进行MRI检查,目前临床迫切需要一种无创、快速、可重复的床旁检查手段。床旁超声就是在这种环境下应运而生的。随着超声影像技术的发展,床旁急诊经胸心脏超声(transthoracic echocardiography,TTE)作为AAS的诊断初筛工具已成为可能。床旁快速经胸腹超声探查具有安全、便捷、不受状态和环境影响且易被急诊医师所掌握等优势,已逐渐成为国内外急诊疑似患者的首选检查方法[4]。本文通过连续观察181例疑诊A型AAS患者的经胸腹超声影像特点,探讨超声影像检查在AAS诊断中的应用价值。
1 对象与方法
1.1 研究对象
本研究实施单位中日友好医院为三级甲等综合医院,年急诊量170000人次,影像科24h均开展CTA检查,心血管外科中心具备AAS救治能力。以2013年3月~2017年4月就诊于急诊并收治于急诊抢救室的疑诊A型AAS的患者为研究对象,纳入标准参照2010年美国心脏病协会/美国心脏病学院共同发布的胸主动脉疾病诊断治疗指南关于主动脉夹层风险(aortic dissection detection,ADD)的定义(每项 1 分,共计 12 分)[5],>1分为疑诊患者纳入研究:①高度风险基础疾病或情况:马凡综合征(或其他结缔组织疾病史)、主动脉疾病家族史、已知主动脉瓣疾病、已知胸主动脉瘤、近期行主动脉操作(包括外科手术);②高度风险的胸背腹部疼痛性质:突发疼痛、疼痛剧烈、撕裂样/尖锐性疼痛;③高度风险体征:脉搏短绌或四肢收缩压差>20mmHg、局部神经病变体征(伴随疼痛)、主动脉反流性杂音(新发或伴随疼痛)、低血压或休克。排除标准:年龄<18岁、病情危重或短时间死亡未能完成检查(包括床旁超声及CTA)。
1.2 研究方法
在不妨碍患者接受紧急救治的前提下,对于入抢的符合上述条件的患者在30min内行床旁超声检查(根据实际检查情况,单个超声流程检查<5min),超声检查由3位受过超声培训的固定急诊科医师完成,采用Sonosite M-Turbo型超声机和2~5MHz相控阵探头,患者取平卧位及左侧卧位,探测部位及切面分别为胸骨旁左室长轴、心尖区及肋下至脐上区。所有探查均在心脏舒张期进行。A型AAS超声探查下直接征象定义为:主动脉内膜分离呈带状或线状回声漂浮摆动或主动脉壁内血肿征象(主动脉壁呈环形或新月形增厚>5mm)。A型AAS超声探查下间接征象定义为:升主动脉根部增宽,直径>4mm或心包积液/心脏填塞征象或彩色多普勒提示主动脉瓣反流。所有患者在24h内完成主动脉 CTA检查(Aquilion TSX-101A,日本东芝公司)并均签署检查知情同意书。由同一位影像科医师给出诊断结果。以CTA结果作为诊断A型AAS的金标准。
根据最终临床诊断将列纳入患者分为A型AAS组和非A型AAS组,比较2组患者超声影像上的差异;因A型AD累及升主动脉根部,病情进展迅速,死亡率极高,对急诊医师要求诊断的时效性最高,故特别分析每个特征性的超声影像(包括直接征象及间接征象)以及床旁超声总体诊断A型AD的敏感性、特异性、阳性预测值、阴性预测值和准确性。
1.3 统计学方法
采用SPSS15.0软件进行统计学分析,所有计量资料均用±s表示,组间比较采用t检验;计数资料比较采用卡方检验。敏感性=真阳性/(真阳性+假阴性);特异性=真阴性/(真阴性+假阳性);阳性预测值=真阳性/(真阳性+假阳性);阴性预测值=真阴性/(真阴性+假阴性);诊断准确率=(真阳性+真阴性)/(真阳性+真阴性+假阳性+假阴性)。
2 结果
2.1 病例资料
共收治疑诊A型AAS患者193例,其中7例患者因体型及体位配合欠佳等原因无法获取清晰超声影像,5例患者入抢后短时间死亡未能完成床旁超声或CTA检查,以上患者均被排除在外。最终纳入181例患者,其基线资料和临床特征见表1。A型AAS组患者46例,男29例、女17例;非A型AAS组135例,男79例、女56例。A型AAS中,39例(21.5%)为典型Stanford A型主动脉夹层,2例(1.1%)为升主动脉IMH,5例(2.7%)为升主动脉PAU。非A型AAS组包括:未累及升主动脉的B型AAS 48例、急性冠脉综合征26例、消化系统疾病29例、大动脉炎3例、心包积液6例、肺栓塞4例、肺炎5例、肌肉骨骼疼痛6例、神经系统疾病8例。2组患者在年龄、主动脉疾病家族史、剧烈疼痛、3个高风险体征及ADD风险评分上差异有统计学意义(P<0.05,P<0.01)

表1 入选患者的基线资料和临床特征
2.2 A型AAS组与非A型AAS组超声影像比较
超声检查的直接征象包括:主动脉内膜分离呈带状或线状回声漂浮摆动或主动脉壁内血肿;超声间接征象:升主动脉根部增宽、心包积液/心脏填塞和主动脉瓣反流。其诊断A型AD的效能见表2。
A型AAS组患者中8例可见直接征象,其中7例经典A型AD患者和1例累及升主动脉的PAU患者;非A型AAS组3例患者见直接征象,2组比较有显著性差异(P=0.001)。超声间接征象的升主动脉根部增宽可在33例A型AAS组及21例非A型AAS组患者中探查到;2组均有17例患者有心包积液/心脏填塞征象;A型AAS组29例患者有主动脉瓣反流征象,非A型AAS组15例患者见此征象,以上3个征象2组间比较均有显著性差异(均 P<0.01)。
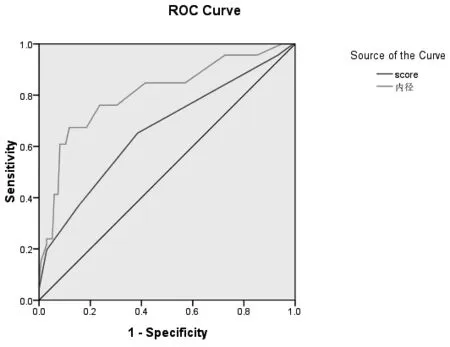
图1 ADD风险评分及升主动脉内径诊断A型AD的ROC曲线

图2 确诊A型AAS 46例患者超声各征象出现比例

表2 床旁超声各征象诊断A型AD的诊断效能 %(n/n)
此外,升主动脉内径诊断A型AD的ROC曲线下面积为80.7%,最佳临界值为40.9mm,而ADD风险评分用于诊断A型AD的ROC曲线下面积为66.3%,最佳临界值为2.5分(图1)。确诊A型AAS的46例患者中以超声探查出现升主动脉增宽征象出现比例最高,达72%(图2)。
对于表现为低血压/休克的重症疑诊患者进行床旁经胸心脏超声,以明确超声是否可以在短时间内提供初步诊断倾向,结果显示在11例表现为低血压/休克的疑诊A型AAS患者中,超声直接征象(主动脉内膜分离呈带状或线状回声漂浮摆动或主动脉壁内血肿征象)的敏感性、特异性、阳性预测值、阴性预测值分别为45.5%(5/11)、100%(9/9)、100%(5/5)、60%(9/15)。
3 讨论
3.1 经胸心脏超声的临床应用优势
AAS是一种发病率逐年升高且死亡率极高的心血管疾病,症状和体征多变且多为非特异性,初诊漏诊率可高达40%,有相当比例的患者是在死后才确诊的。很少有其他疾病像此类一样,需要如此迅速的诊断和治疗。早期进行外科介入治疗,可大大提高此类患者的生存率,所以对此类患者进行早期诊断相当重要。而经胸超声心动图具有方便、快捷、安全、不受状态和环境影响等特点,可以实时观察、重复使用。经胸超声心动图诊断AAS的意义不仅仅在于对主动脉夹层进行分型,更重要在于对患者心脏功能的整体评价、以及主动脉瓣反流的定性定量诊断,可以对AAS患者选择治疗方案及预后提供更多的帮助;另外经胸超声心动图还可以观察心包腔、胸腔是否存在积液以及积液量多少,对危重患者的检查可以在床旁进行,因而经胸超声心动图在对AAS的早期诊断中发挥着越来越重要作用。目前已逐渐在国内外急诊室甚至院前急救中开展[6]。
3.2 经胸心脏超声的总体诊断价值
目前文献报道的由不同专科医生操作经胸心脏超声对AAS诊断的敏感性为57%~88%,特异性为65%~96%。笔者前期对经胸心脏超声对AAS的诊断价值Meta分析结果表明,TTE用于诊断A型急性主动脉夹层的汇总敏感性为79%,汇总特异性可达95%[7]。目前由急诊医师操作经胸心脏超声探查AAS的研究较少,多数研究仍为心脏或超声专科医师探查,这类操作者经验相对丰富[8~11],这也解释了为何与其他已报道文献相比,本研究显示超声直接征象的敏感性(20.5%)偏低,可能与超声检查由受过短期培训的急诊医师完成,其经验及操作技能对检查结果有一定影响有关。本研究中对经胸心脏超声漏诊病例分析,考虑漏诊原因与患者体位受限、A型PAU/IMH患者难以探查到漂浮内膜,而穿透性溃疡或壁内血肿征象难以在床旁超声下探及有关。
本研究中AAS疑诊患者最终有48例诊为B型主动脉综合征,B型主动脉综合征应用超声诊断敏感性明显下降,主要原因与声窗的限制有关,降主动脉胸段位于后纵隔心脏的后方,位于远场,由于纵隔内结构和肺气的干扰,通常导致主动脉显示不清,熟练操作者能够部分显示降主动脉胸段长轴,但仍难以显示短轴,更难显示其撕裂的内膜回声。而对于降主动脉腹腔段,往往由于进食后或腹胀所产生的肠气影响到超声检查结果。此外,本研究提示:单纯依据ADD风险评分用于诊断A型AAS的诊断效能并不满意,ROC曲线下面积仅有66.3%,强烈提示首诊医师仍需要借助其他手段,如D二聚体等[12]帮助快速诊断。
3.3 经胸心脏超声的准确性
我们对表现为低血压/休克的重症疑诊患者进行床旁经胸心脏超声的准确性进行研究,结果提示对于此类患者超声直接征象(主动脉内膜分离呈带状或线状回声漂浮摆动或主动脉壁内血肿征象)的特异性可达到100%。这表明对于重症疑诊患者床旁经胸心脏超声一旦探及直接征象及可在短时间内得出初步诊断倾向并高度提示转运高风险,此类患者应避免转运至CT室,可考虑直接急诊手术或床旁TEE检查[13],可明显降低医疗风险及患者死亡风险。
目前可用于诊断主动脉夹层的各种方法包括主动脉CTA、经胸超声心动图检查及经食管超声心动图检查,就诊断精度、速度、方便、风险、成本而言各有优缺点,没有一种方法在所有情况下都适用。经胸心脏超声检查是无创性检查,是诊断主动脉夹层的首选方法,但其阴性结果并不能作为排除标准。主动脉CTA是目前诊断主动脉夹层的金标准,它既可以显示主动脉夹层的累及范围,同时也可以部分显示血流动力学状态。但由于是有创性检查,具有转运风险并且造影剂的放射性对人体也有损害,不宜作为诊断重症疑诊AAS患者的首选[14]。本研究结果亦提示,由急诊医师操作的经胸心脏超声可以作为疑诊AAS患者的快速初筛工具,广泛开展床旁TTE检查同时结合ADD风险评分可以提高AAS的快速诊断效能,选择及时正确的治疗。
——以渤海A 油藏为例

