中耳胆脂瘤听小骨骨质侵犯研究
陈龙云魏兴梅高志强王晓喆宋雯洁孙慧颖冯国栋
1中国医学科学院北京协和医学院北京协和医院病理科(北京100730)
2中国医学科学院北京协和医学院北京协和医院耳鼻喉科(北京100730)
全球共有超过两千万人患有中耳炎,其中1/4(约500万)是中耳胆脂瘤患者[1]。胆脂瘤的典型特征为骨质破坏[2],对于中耳胆脂瘤目前主要采取乳突根治及鼓室成形术清理病变,大部分患者可以获得良好的效果。从病理机制分析,如果胆脂瘤彻底切除至中耳乳突无胆脂瘤成分,将会减少胆脂瘤复发的机会。但是胆脂瘤术后复发一直是学者们努力避免而尚未解决的问题,包括术中已经“彻底清除胆脂瘤”的患者,仍然存在一定的复发率。本研究拟通过观察胆脂瘤患者的听骨残体标本破坏和浸润情况,寻找胆脂瘤术后复发的原因,为正确的制定中耳胆脂瘤手术方案提供依据。
1 材料和方法
因中耳胆脂瘤于我院行手术治疗的20例患者,手术时间为2018年5月至2019年1月。其中男性11例,女性9例,年龄最小3岁,最大57岁。术前颞骨CT均显示有胆脂瘤破坏听骨或鼓室壁的影像学改变(如图1),术中及术后病理均证实中耳及乳突腔内病变有胆脂瘤上皮存在。术中将听骨或听骨残体取下后,在显微镜下观察听骨大体情况,并将听骨表面上皮组织及肉芽组织去除。立即在10%中性福尔马林溶液中固定,约3d。然后置入由5.5g EDTA和10%福尔马林组成的溶液中进行脱钙,周期为1d,直到听骨组织可以取材,将标本脱水、透明、浸蜡和包埋,制成蜡块,将蜡块切成4μm厚的切片,进行标准的苏木素/伊红染色,在光学显微镜下检查标本以确定是否存在角蛋白。
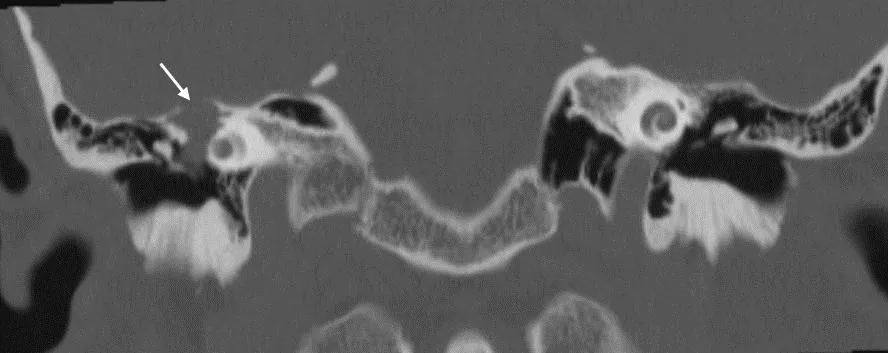
图1 胆脂瘤颞骨CT改变。图中白色箭头所示胆脂瘤破坏中颅窝脑板,并有听骨及迷路的破坏。Fig.1 The CT scan image of temporal bone with cholesteatoma.The white arrow points to the invasion of cholesteatoma to middle cranial fossa plate as well as the damage to ossicles and labyrinths.
2 结果
所取标本中,砧骨残体+锤骨头12(60%)例,砧骨残体(40%)8例。病理确认存在角蛋白的7(35%)例,未发现角蛋白的13(65%)例。胆脂瘤破坏听骨的镜下表现均可见胆脂瘤侵及或包绕听骨,经脱钙处理后可见局部骨小梁碎片,下层含局灶淋巴细胞。如图2中所示胆脂瘤破坏听骨表面可见H&E染色为蓝色的斑片状骨组织,胆脂瘤鳞状上皮菲薄,可见突出的颗粒状细胞层内的角化蛋白。图3表示鳞状上皮间囊性扩张区,内含角化物及坏死,角化物紧邻周围骨质,部分可见骨质破坏,上皮层下的纤维结缔组织与骨表面直接接触,周围纤维结缔组织中炎细胞浸润。
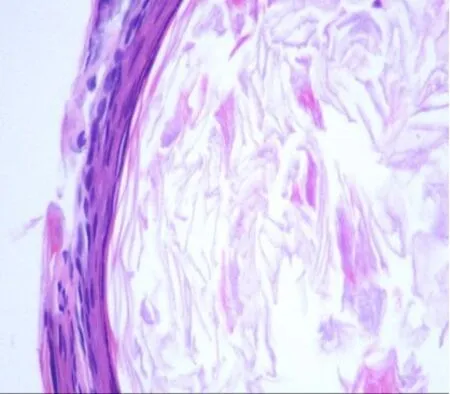
图2 典型的胆脂瘤表现(×10),可见大量角蛋白及鳞状上皮。Fig.2 This is a typical case of cholesteatoma(×1),with a largeamount of keratin and squamousepithelium.
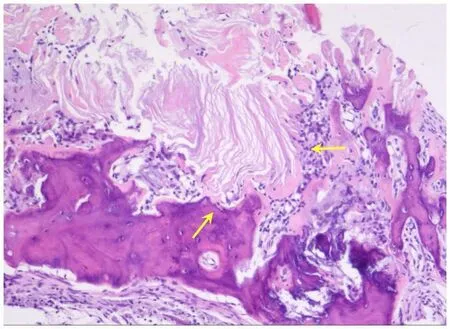
图3 光镜下听小骨受胆脂瘤侵犯病例切片(×10)。黄色箭头所指表示角蛋白紧邻周围骨质,局部浸润。Fig.3 Section of ossicle invaded by cholesteatoma under light microscope(×10).The yellow arrows indicate that keratin isadjacent to the surrounding bone and is locally infiltrated.
3 讨论
中耳胆脂瘤是在中耳腔呈肿瘤样生长的角质化鳞状上皮。胆脂瘤大体表现为白色、质脆的,在完整的情况下外边包有一层薄薄的壁,通常为卵圆形,从病理层面看,包含有许多层,病理特征为可见鳞状上皮,颗粒组织和角化物[3]。胆脂瘤的成分包括外膜层,基质和囊壁。外膜层是胆脂瘤最外边的一层,主要有大量的颗粒组织和纤维结缔组织组成;此层与病变年龄有关,先天性胆脂瘤含有更多的颗粒组织,而成年人含有更多的结缔组织,认为此层具有侵蚀骨质的作用[4]。基质层主要含有角蛋白和鳞状上皮,鳞状上皮角化是胆脂瘤形成的重要步骤,研究认为在这一过程中一些促进分裂的细胞因子和免疫成分产生,改变了正常的信号通路,导致角质细胞生成过多并且侵袭性生长[5],如细胞角蛋白和Ki-67等[6]。其中细胞角蛋白是上皮细胞特有的中间丝蛋白,它的表达在上皮细胞化生过程中发挥重要作用[5]。通常角蛋白聚集在基质层的中心,在其作用下,胆脂瘤体积逐渐增大。囊壁层包含一个腔状区域由大量脱落的、无核的角蛋白组成,囊壁层侵蚀组织是通过与角质碎片发生异物巨细胞反应产生的[7]。研究发现若术后内陷袋内仍含有角蛋白则可以导致胆脂瘤再次发生[8],可能是由于炎性细胞释放的促生长成分,如环氧合酶-2、白介素-8等,促进血管再生,角蛋白或角化细胞沿着再生的血管网迁徙入中耳腔导致复发[9,10]。而正常表皮中角化细胞与胆脂瘤细胞的不同在于,胆脂瘤细胞就有侵袭性并不断扩张造成骨质破坏还是其具有复发倾向的根源[11]。
很多学者认为难以判断胆脂瘤是残留还是复发,有学者提出根据病变产生的部位来判断,若是病变来源于锤骨周围肌肉则考虑为残留,若来源于鼓膜则考虑为复发[12]。也有学者认为若随访6年后胆脂瘤未再发生,则认为前次手术无病变残留,再发生的胆脂瘤称之为复发[12],但从胆脂瘤的发生机理上分析,如果没有胆脂瘤成分残留和胆脂瘤形成的原因,则不应该有胆脂瘤发生,而去除胆脂瘤和胆脂瘤形成的原因(主要是通过手术建立正常的中耳颞骨通气引流),是目前中耳乳突手术可以实现的。在“彻底清除胆脂瘤”后,目前比较公认的文献报道开放式乳突根治术后胆脂瘤残留的概率在4%[13]到6%[14,15]之间。除还有少部分胆脂瘤上皮残留因素,大部分可能为角蛋白残留所致,由于角蛋白在肉眼下不可见,所述“彻底清除胆脂瘤”事实上为“彻底清除胆脂瘤白色上皮”,而非彻底清理胆脂瘤成分。胆脂瘤复发不仅会影响听力,甚至可能破坏面神经、迷路、脑膜等引起面瘫、迷路炎、脑膜炎甚至威胁生命[16]。尤其对于前次手术已经裸露的面神经或脑膜,若胆脂瘤复发再次手术显著增加了手术风险。所以首次手术力求胆脂瘤清除干净非常重要。
本研究中所取听骨标本均包含砧骨或砧骨残体,这可能是由于砧骨位于鼓窦入口,血运较差,更容易受到侵犯[17,18]。而且研究发现位于鼓室窦的胆脂瘤更容易侵犯听骨[19],其中首先受累及的亦是砧骨[20]。另外有研究取160例听骨链完整的上鼓室胆脂瘤患者的砧骨进行病理学检查,发现砧骨中被炎性组织侵犯的概率达67.5%,因此建议对于此类患者手术中要去除听小骨[21]。1972年,Hildmann和Steinbach等[22]进行组织病理学研究发现,胆脂瘤术中取下的同于听骨链重建的听小骨中约有50%有潜在的炎症,指出这种听骨缺乏稳定性,建议原则上不应使用胆脂瘤以及慢性中耳炎处理后的听骨重建听骨链。国内学者蔡秋颖等[23]也做过类似研究,发现42例听骨中,20例有炎症反应,5例听骨表面有鳞状上皮覆盖。张安全等[24]报道对11例中耳胆脂瘤患者行颞骨切片,发现胆脂瘤对听骨链及周围骨质均有不同程度吸收破坏,可观察到胆脂瘤侵入区域有肉芽粘连组织、炎性渗出液和炎性细胞浸润。该研究还发现中耳胆脂瘤主要侵犯听骨链区,侵入前半中耳腔的概率非常小(不足30%),国外此类研究亦得出相似结论[25]。但以往的研究主要着眼于听骨中存在的炎性反应,其问题在于炎性反应可能会在中耳通气功能改善后得以改善,并非一定会引起中耳炎或胆脂瘤复发。本实验中进一步着重于研究听骨中存在角化蛋白的概率,发现高达35%。由于角化蛋白是促进鳞状上皮化生的重要物质,进一步证明中耳胆脂瘤中即便肉眼所见听骨表面无胆脂瘤上皮,听骨内存在浸润的概率亦较高。另外本实验只观察了听小骨受胆脂瘤侵犯的情况,是因为听骨取材方便。但可以推论,胆脂瘤周围非听小骨的骨质,如中颅窝脑板、迷路周围间隙等骨质也存在类似的角蛋白浸润,在显微镜或耳内镜下不能发现。提示我们胆脂瘤型中耳炎手术要彻底清除可见的胆脂瘤上皮外,还应去除周围受炎症侵犯的骨质而不是仅仅将胆脂瘤去除即可,因为浸润于骨质中的胆脂瘤上皮及角蛋白亦可能导致胆脂瘤复发。本研究仅针对胆脂瘤中耳炎听骨中存在角蛋白浸润可能导致复发,术腔引流、咽鼓管功能持续不能改善等因素也是导致胆脂瘤复发和/再发的因素,实际临床工作中相关因素都需处理到位,方能取得良好效果。
4 结论
中耳胆脂瘤的患者中,听骨内浸润胆脂瘤成分的比例高,即便肉眼所见正常的听骨亦可能有角蛋白浸润而导致复发。提示此类手术中除去除胆脂瘤上皮外,也应去除胆脂瘤周围可能受侵犯的骨质,以减少复发。

