先天性心脏病介入治疗术中及围术期严重并发症分析
王忠超 王琦光 张端珍 韩秀敏 张坡 崔春生 盛晓棠 朱鲜阳
自20世纪80年代我国开展先天性心脏病(先心病)介入治疗以来,介入技术的不断进步以及临床经验的不断积累,特别是以国产器材为代表的介入材料的不断改进,使先心病介入诊疗水平得到显著提高[1-2]。但由于介入治疗适应证选择不当、患者解剖类型特殊以及技术操作、应用材料等问题所引起的相关并发症仍应引起临床医师的足够重视。近年来儿童先心病患者死亡率逐年降低,增加了成人先心病患者的比例,且间接增加了经导管介入检查或治疗的并发症风险[3]。本文回顾性分析了北部战区总医院近5年来经导管介入治疗的先心病患者术中或围术期严重并发症的发生情况,总结相关经验,为先心病介入诊疗相关并发症的防治提供借鉴。
1 对象与方法
1.1 研究对象
回顾性研究2013年1月至2017年12月4704例于北部战区总医院接受经导管介入治疗的常见先心病患者(男1656例,女3048例),年龄21 d~76岁。其中,动脉导管未闭(patent ductus arteriosus, PDA)组1219例(男388例,女831例)、房间隔缺损(atrial septal defect,ASD)组2170例(男706例,女1464例)、室间隔缺损(ventricular septal defect,VSD)组948例(男402例,女546例)、卵圆孔未闭(patent foramen ovale, PFO)组103例(男45例,女58例)、肺动脉瓣狭窄(pulmonary valve stenosis,PVS)组240例(男100例,女140例)、主动脉瓣狭窄(aortic valve stenosis, AVS)组6例(男5例,女1例)、主动脉缩窄(coarctation of aorta,CoA)组14例(男8例,女6例)以及肺动脉狭窄(pulmonary stenosis,PS)组4例(男2例,女2例)。
1.2 研究方法
局部麻醉或全身麻醉(年龄≤10岁)下行股动脉和(或)股静脉穿刺,成功后按100 U/kg剂量给予肝素化,术中全程行心电图、压力和经皮血氧饱和度监测。PDA、ASD、VSD、PFO封堵术采用上海形状记忆有限公司、北京华医圣杰有限公司、深圳先健科技有限公司和美国雅培公司生产的不同型号封堵器;经皮球囊肺动脉瓣成形术(percutaneous balloon pulmonary valvuloplasty,PBPV)、经皮球囊主动脉瓣成形术(percutaneous balloon aortic valvuloplasty,PBAV)采用法国Balt聚乙烯球囊及Inoue球囊;CoA采用美国NUMED公司生产的覆膜支架。严重并发症如心脏压塞、封堵器移位/脱落等由症状、体征、X线影像、经胸超声心动图诊断;三度房室传导阻滞(atrioventricular block,AVB)等心律失常由心电图及心电监护诊断;股动静脉瘘、假性动脉瘤和股动脉血栓由下肢血管超声诊断;血小板减少由血常规检测结果得到。
1.3 统计学分析
所有数据采用SPSS 19.0统计软件进行数据分析。计数资料采用率或百分比表示,组间比较采用卡方检验,对并发症发生率进行组间比较分析,并采用Bonferroni校正方法调整检验水准。以P<0.0167为差异有统计学意义。
2 结果
本研究共发生术中或围术期严重并发症46例,发生率0.98%。其中PDA组12例,发生率0.98%;ASD组12例,发生率0.55%;VSD组19例,发生率2.00%;PVS组1例,发生率0.42%;AVS组1例,发生率16.67%;CoA组1例,发生率7.14%(表1)。VSD组严重并发症发生率显著高于ASD组(P<0.001),且明显高于PDA组,但差异无统计学意义(P=0.047)。PDA组与ASD组严重并发症发生率比较,差异无统计学意义(P>0.0167)。
以并发症类型进行分类统计,共7例患者发生封堵器脱落或移位,其中PDA组2例、ASD组4例、VSD组1例,VSD组患者同时合并重度三尖瓣关闭不全;5例发生三度AVB,其中ASD组2例、VSD组3例;2例发生心脏压塞,ASD组及PVS组各1例;AVS组1例发生急性左心功能衰竭;8例出现重度血小板减少,均为PDA组;VSD组1例发生反射性低血压;CoA组1例发生股动脉栓塞;ASD组1例发生股动脉假性动脉瘤;共19例患者封堵不成功,其中PDA组2例、ASD组4例、VSD组13例(表2)。
本研究1例患者死亡,死亡率为0.02%。16例接受急诊手术治疗,急诊手术率为0.34%。其中6例封堵器脱落或移位、4例三度AVB、1例急性心脏压塞患者行开胸手术治疗,1例封堵器脱落通过介入方法取出封堵器,1例术后股动脉栓塞患者行股动脉切开及补片成形术治疗,1例术后股动脉假性动脉瘤患者行超声引导下局部注射凝血酶封闭治疗,3例三度AVB(其中2例行开胸手术治疗)及1例死亡均先行临时起搏器植入治疗。不同类型并发症处理方法见表2。上述患者中,除死亡患者外,其余患者经积极治疗后均预后良好。
3 讨论
根据文献报道,先心病介入治疗相关并发症严重程度分为5级:其中,1级和2级,无需特殊处理或仅需轻度干预;≥3级为严重并发症[3-4]。本研究仅统计严重并发症患者。
3.1 并发症发生率分析
回顾性分析4704例接受经导管介入治疗的先心病患者,共发生各类严重并发症46例,总发生率为0.98%,包括1例死亡病例,死亡率为0.02%;16例需急诊手术,急诊手术率为0.34%。蒋世良等[1]曾回顾性分析其单中心2318例常见先心病介入治疗术后严重并发症情况,其并发症总发生率为1.47%,急诊手术率为0.35%,死亡率为0.09%。其他类似研究并发症发生率亦高于本研究[5-8]。Varrica等[9]于近期发表的一项单中心研究表明,常见先心病介入治疗术后早期并发症外科补救手术率为0.69%,术后晚期并发症外科补救手术率为0.37%。
VSD组并发症发生率为2.00%,显著高于ASD组,这一结果与前期研究相符[1]。VSD因其特殊的解剖学特征以及可选择封堵器类型相对较少,手术难度大,心律失常及瓣膜关闭不全等严重并发症发生率高[10]。本研究中VSD组共发生19例严重并发症,ASD及PDA组各12例,上述并发症均与病变解剖条件、封堵器类型及术中操作密切相关,术者更应严格把握介入治疗适应证,充分评估,术后严密观察,及时处理。
3.2 不同类型并发症分析
封堵器脱落或移位是先心病封堵术常见严重并发症之一,最常见于ASD封堵术,发生率为0.25%~1.44%[11],也可见于VSD及PDA封堵术,常因封堵器过小、病变解剖位置特殊及适应证选择不当所致。发生该并发症的ASD患者中,约80%为下腔缘不足所致[12]。本研究4例封堵器脱落或移位的ASD患者中,3例为下腔缘不足,1例为测量误差。因此,局部解剖条件不确切时应进一步评估,尤其下腔型ASD患者应提高超声心动图诊断准确率,必要时行经食管超声心动图检查,同时,释放封堵器前应反复推拉并反复确定位置和形状。导管室要常备各类异物钳,根据病理解剖、脱落部位等因素决定处理方法,可先用异物钳抓取,不成功时立即外科手术,避免延误病情。

表1 各组患者严重并发症发生率比较[例(%)]
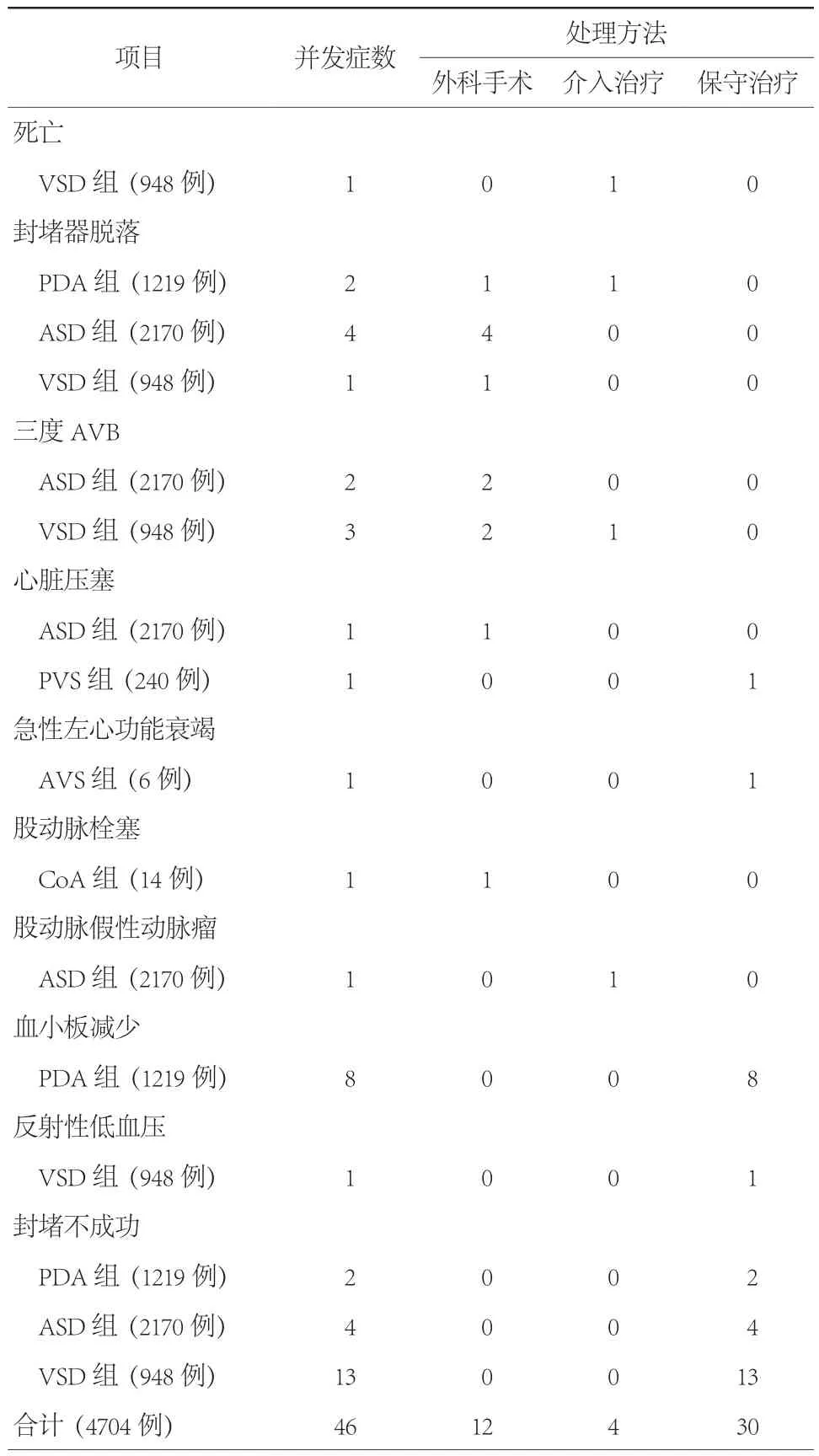
表2 各组患者发生严重并发症的处理方法(例)
瓣膜关闭不全常见于VSD封堵术,包括主动脉瓣和三尖瓣关闭不全,前者主要在右冠状动脉瓣,后者多在隔瓣[13],多与缺损距瓣膜过近、膜部膨出瘤、瓣膜或腱索受损、封堵器放置不当等有关。 应注意,VSD距主动脉瓣≥2 mm,距三尖瓣隔瓣≥3 mm是介入治疗的最佳条件,应根据VSD大小、位置及与瓣膜距离选择合适封堵器。建立轨道时,注意导管及导丝畅通,避免穿过右心室腱索和乳头肌。释放封堵器前,应反复确认瓣膜情况及封堵器形状、位置。术中出现该并发症时应及时撤回封堵器,释放后出现时应行外科手术,轻度反流者仅需随访观察。
三度AVB 多见于VSD封堵术中或术后2~7 d甚至数年,发生率0.1%~3.0%,与导管刺激、封堵器压迫、局部水肿及VSD靠近传导束有关[11]。本研究3例VSD及2例ASD出现三度AVB。该类患者应操作轻柔,封堵器不宜过大,首选对称型封堵器以减少不均衡压迫所致水肿及传导障碍。术后延长住院时间,常规应用激素减轻心肌水肿。临时起搏器植入后21 d仍未恢复者应行外科手术。ASD封堵术后发生三度AVB多与封堵器过大有关,发生该并发症应立即回收并更换较小封堵器。若发生于儿童患者,应尽早外科手术。
心脏压塞多见于ASD封堵术,发生率为0.12%~0.47%,多因导管、导丝或鞘管穿破房壁 、封堵器过大磨蚀心房壁所致[11]。患者出现心率快、血压低时,首先判断有无心脏压塞,有心脏压塞则应立即心包穿刺,抽出血液后自体回输,并给予升血压、补充容量等对症治疗。病情稳定者2~3 d后拔出引流管。病情重、血压持续下降者尽快转外科手术。
急性左心功能衰竭多发生在重度瓣膜狭窄、大ASD合并肺高压、左心室舒张末期内径≤35 mm者,ASD封堵后,左心室不能承受体循环压力负荷,出现呼吸急促、发绀、肺部啰音、咯血色泡沫样痰等表现[14],早期发现及时处理,预后较好。
血小板减少常见于PDA封堵术后,尤其是婴幼儿较大PDA者,多与封堵器较大或残余分流致血小板聚集、破坏有关。本研究中,血小板减少的8例均是PDA患者,6例为婴幼儿,2例为成年女性。对于重度肺动脉高压、PDA较大者,应选择国产封堵器,因其内缝有多层聚酯纤维膜,能够完全阻断血流,减少残余分流,避免大量红细胞和血小板的聚集与破坏,减少溶血、血红蛋白尿或血小板减少的发生。发生血小板减小时,可给予激素、碱化尿液、控制血压、保护肾功能等治疗,情况严重时由外科处理。
19例患者封堵不成功。应注意术前准确判断介入治疗可行性,观察封堵器置入后残余分流及瓣膜反流情况,合并肺动脉高压时,行心导管检查评估血流动力学,判断预后情况,以此决定能否行介入治疗。
1例患者死亡,死亡率为0.02%,低于其他同类型研究[1]及成人获得性心脏病介入治疗死亡率[14-15]。该例患者VSD紧靠主动脉瓣下,选用国产偏心封堵器封堵后,出现主动脉瓣中度反流而放弃封堵。患者术后出现意识淡漠,呼之不应,紧急抢救无效死亡,考虑死因为主动脉内膜撕脱所致夹层。应注意术中操作规范、轻柔,切忌暴力牵拉导管及输送鞘,避免损伤动脉内膜,对于手术难度大、时间长的患者,应严密观察患者状态及术中监测指标,一旦发现问题及时对症处理。
股动静脉瘘或假性动脉瘤是先心病介入治疗常见血管并发症[11]。应注意穿刺时患者下肢外展,股静脉穿刺位点不应过低,避开股动脉,术后观察患者穿刺点情况,有无血管杂音,可行下肢血管超声明确诊断,必要时行介入或外科治疗。局部血栓形成主要与血液高凝状态及血管内膜损伤有关,尤以股动脉栓塞最常见。应注意选择合适型号导管及鞘管,避免损伤血管内膜;充分抗凝,密切观察术侧肢体足背动脉搏动、颜色及皮温变化。
国内经导管介入治疗先心病历经20年,积累了丰富的临床诊治和操作经验,尤其是《常见先天性心脏病介入治疗中国专家共识》[16-20]的发表,系统规范了先心病介入治疗操作技术,早期操作所致血栓、气栓、严重心律紊乱等并发症发生率逐渐减少,成功率显著提高,加之介入治疗创伤小、恢复快、费用低,已成为多种先心病首选治疗方案。但是,临床医师在确定治疗方案前应充分评估手术适应证,避免盲目扩大介入治疗范围,尤其对于婴幼儿或VSD等风险较高的先心病,患者术前应精准诊断,术中规范操作,术后严密观察,一旦发现异常及时正确处理,进一步降低先心病介入治疗并发症发生风险,提高治愈率。

