复发/难治性淋巴瘤免疫治疗的研究进展
冯佳,彭敏,章必成
(武汉大学人民医院肿瘤中心,武汉 430060)
淋巴瘤是原发于淋巴结或淋巴组织的恶性肿瘤,发病率和死亡率均较高,10%~30%患者对初始治疗耐药或治疗后复发[1-2]。即使在低风险患者中,仍有超过60%的霍奇金淋巴瘤(Hodgkin Lymphoma,HL)患者经自体干细胞移植(autologous stem-cell transplantation,ASCT)治疗后再次出现失败[3-4],完全缓解(complete response,CR)率仅12%[4]。同样,非霍奇金淋巴瘤(non-Hodgkin Lymphoma,NHL)经ASCT治疗后复发率仍较高,预后不良[5-6]。在ASCT治疗失败的复发/难治性(ralapsed/refractory,R/R)HL患者中,本妥昔单抗(brentuximab vedotin,BV)疗效有限,中位无进展生存期(progression-free survival,PFS)仅5,6个月[7]。Rituximab的问世改变了NHL的治疗模式,但仅对部分复发性NHL有效(20%~50%)[8-9]。因此,对于ASCT或分子靶向治疗失败后的R/R HL或NHL,尚无标准治疗。近年,多项研究探讨免疫检查点抑制剂(immunological checkpoint inhibitors,ICIs)或嵌合抗原受体T细胞(chimeric antigen receptor T-cell,CAR-T)免疫疗法用于治疗复发/难治性(R/R) HL或NHL的疗效。笔者在本文将综述R/R HL或NHL免疫治疗的最新研究进展,并对目前存在的问题进行探讨,对其未来进行展望。
1 R/R HL
经典型霍奇金淋巴瘤(classical Hodgkin Lymphoma,cHL)为HL最常见组织学类型,约占所有HL的90%。研究显示初诊cHL几乎均可检测到9p24.1异常,包括多体性(5%),PD-L1、PD-L2的拷贝数增加(58%)或扩增(36%)[10]。因此,基于9p24.1的高频率改变和PD-1配体的表达增加,PD-1/PD-L1成为治疗cHL的独特靶标。
1.1Nivolumab Ⅰ期(CheckMate 039)研究评估了Nivolumab治疗23例R/R HL(BV和ASCT治疗后复发进展)的疗效,结果显示疾病控制率(disease control rate,DCR)高达100%,其中客观缓解率(objective response rate,ORR)为87%,CR率为17%[11]。鉴于这些令人鼓舞的初步研究结果,后续的多中心、单臂临床Ⅱ期CheckMate-205 研究进一步评估了Nivolumab的临床疗效。该研究纳入经活检确认的auto-HCT失败后的R/R cHL患者,在中位随访18个月时,仍有40%患者持续用药;总体ORR为69%,各队列的ORR为65%~73%;总体的中位持续反应(duration of response,DoR)时间为16.6个月,PFS为14.7个月;患者耐受性良好,只有7%患者因治疗相关不良反应而停止治疗[12]。基于CheckMate-039和CheckMate-205研究B队列研究的总响应率数据,FDA于2016年5月批准Nivolumab用于治疗患有复发性或在HSCT治疗后使用BV出现疾病进展的cHL患者。在Nivolumab作为单一疗法取得令人鼓舞的结果后,有研究进一步探讨了Nivolumab联合其他疗法的临床疗效。一项Ⅰ/Ⅱ期、开放、多中心临床试验纳入61例可评估疗效的R/RcHL患者,给予Nivolumab联合BV的初始补救治疗。所有接受治疗的患者的CR为61%,ORR为82%。在可进行疗效评估的60例患者中,有54例患者接受了ASCT,其中42例患者在接受Nivolumab联合BV治疗后,直接接受了ASCT;17例患者接受了挽救治疗,1例达到CR的患者接受了巩固性放疗[13]。由此可见,作为R/R HL的第一次挽救治疗,Nivolumab联合BV是ASCT的一种可耐受且有效的过渡,它取代大多数患者对化疗的需求。与既往单独使用Nivolumab或BV治疗的数据相比,更高比例的患者获得了CR,这是ASCT疗效的关键预后因素。
1.2Pembrolizumab 多中心、开放性Ⅰb期KEYNOTE-013临床研究评估了Pembrolizumab在R/R cHL患者中的安全性和有效性。该研究招募31例经BV治疗失败的患者,Pembrolizumab治疗后ORR达58%,中位PFS为11.4个月,6个月和12个月的PFS率分别为66%和48%;中位OS尚未达到,6个月和12个月的OS率分别为100%和87%。KEYNOTE-013研究证实了Pembrolizumab在复发性cHL中具有高抗肿瘤活性[14]。之后,KEYNOTE-087研究(单臂Ⅱ期)共纳入210例复发/难治性cHL患者,结果显示,ORR可达69%,9个月的OS率和PFS率分别达到97.5%和63.4%[15]。2016年4月,基于正在进行的KEYNOTE-013研究和KEYNOTE-087研究的数据,FDA授予Pembrolizumab治疗R/R cHL的突破性药物资格。2017年3月,基于KEYNOTE-087研究的应答率和应答持续期数据,FDA批准Pembrolizumab用于治疗难治性或三线及以上治疗后复发的成人或儿童cHL。然而,作为一项单臂临床研究,KEYNOTE-087无法证实不同疗法在R/R cHL患者中是否存在疗效差异。最近,KEEPING等[16]报道Pembrolizumab与传统标准疗法之间的疗效比较,展示了Pembrolizumab在治疗R/R cHL方面的优势作用。
1.3Sintilimab 2018年12月27日,国家药品监督管理局批准我国自主研发的肿瘤药物Sintilimab(商品名:达伯舒,全人源抗PD-1单克隆抗体)用于治疗难治性或三线及以上治疗后复发的cHL,标志着抗肿瘤免疫治疗进入了“中国创新时代”。之后,石远凯教授牵头开展的Sintilimab治疗R/R cHL的研究(ORIENT-1),登上《柳叶刀·血液病学》2019年第一期封面。研究结果显示,Sintilimab治疗R/R cHL的ORR高达80.4%,安全性良好,有望成为R/R cHL患者一种新的治疗选择[17]。
1.4Camrelizumab Camrelizumab(SHR-1210)是我国自主研发另一种PD-1抑制剂。在2018年ASCO年会上,韩为东教授展示了Camrelizumab治疗R/R cHL的Ⅰ/Ⅱ期临床研究成果。结果显示,SHR-1210 联合地西他滨的ORR高达89%,CR 率高达 67%[18]。由此可见,SHR-1210 联合地西他滨不仅可以显著提高CR率,也可以有效地逆转HL对PD-1抑制剂的耐药性,且安全性良好。在第11届霍奇金淋巴瘤国际研讨会(ISHL11)上,朱军教授汇报了关于SHR-1210治疗R/R cHL的Ⅱ期研究成果。研究结果显示,ORR约为84.8%,CR率达30.3%,且毒副反应可控[19]。
2 R/R NHL
2.1ICIs NHL分型众多,主要包括B细胞淋巴瘤(B-cell lymphoma,BCL)和T细胞淋巴瘤(T-cell lymphoma,TCL),不都具备对ICIs敏感的遗传学特征;仅少数NHL类型常见9p24.1遗传性改变,而导致PD-L1和PD-L2表达增加。
2.1.1BCL 原发纵隔大B细胞淋巴瘤(primary mediastinal large B-cell lymphoma,PMBCL)是一种特殊类型的弥漫大B细胞淋巴瘤(diffuse large B-cell lymphoma,DLBCL),却具有许多与cHL类似的组织学和遗传学特征,通常存在9p24.1染色体变异(扩增和异位)[20-22]。ZINZANI等[23]评估Pembrolizumab治疗R/R PMBCL的安全性和抗肿瘤活性,在纳入疗效分析的17例患者中,ORR为41%,显著高于既往蒽环类方案的ORR 0%~25%[24-25]。在安全性方面,仅1例出现3级中性粒细胞减少症,1例出现4级静脉闭塞性肝病。KEYNOTE-170研究进一步证实了Pembrolizumab对既往接受过强化治疗的R/R PMBCL患者的临床有效性。该研究入组53例患者,中位随访9.7个月时,ORR为45%。在24例对治疗有应答的患者中,中位DOR尚未达到(1.1~19.2+个月),实现客观缓解的DOR为2.8个月(2.1~8.5个月)。安全性方面,因不良反应中断或停止Pembrolizumab治疗比率分别为15%,8%[26]。2018年6月13日,基于KEYNOTE-170的数据,FDA批准Pembrolizumab用于治疗难治性或既往二线及以上疗法治疗后复发的PMBCL。原发性中枢神经系统淋巴瘤(primary central nervous system lymphomas,PCNSL)和原发性睾丸淋巴瘤(primary testicular lymphomas,PTL)也具有高频率的9p24.1 / PD-L1 / PD-L2 拷贝数改变及基因易位,与PMBCL共有同种免疫逃逸的结构基础[27]。NAYAK等[28]观察Nivolumab在4例R/R PCNSL患者和1例中枢神经系统复发的PTL患者中的疗效。结果显示,4例CR,1例PR,中位PFS为9个月(7~11个月)。滤泡型淋巴瘤(follicular lymphomas,FL)对非特异性细胞因子和ASCT治疗均有较高反应率[29-30],因此,FL可能是一种固有的免疫敏感性恶性肿瘤。Nivolumab在治疗R/R FL患者的ORR为40%[31]。一项关于Nivolumab治疗R/R FL的第二阶段试验研究(CHECKMATE 140)正在进行中。尽管FL可能对ICIs有反应,但反应率明显低于cHL。在CD20阳性的R/R FL患者中,Atezolizumab联合obinutuzumab(第二代抗CD20单抗)的ORR为57%[32],而Rituximab联合Pembrolizumab的ORR为80%[33]。此外,多项临床研究正在进行中,包括ICIs联合放疗、化疗或其他免疫调节药物等。
2.1.2TCL TCL是一种难治性疾病,以全身化疗为主,有研究显示ICIs对其有效。一个最近的回顾性分析报告了7例复发/难治性男性NK/T细胞淋巴瘤,经Pembrolizumab治疗后,5例达CR,2例达PR。中位用药7周期(范围2~13周期)时,5例CR的患者均处于无病生存状态。在一项关于Nivolumab治疗R/R BCL、TCL和多发性骨髓瘤的研究中,TCL亚组的ORR为17%(4/23),其中皮肤蕈样肉芽肿ORR为15%(2/13),外周T细胞淋巴瘤为40%(2/5)[31]。
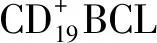
3 结束语
首先,ICIs单药治疗HL有效率很高,而在NHL中表现不佳;而CAR-T细胞更适合于治疗NHL,而对HL疗效不佳。几乎所有的HL中的RS细胞均表达PD-L1,表达率高达95%~100%,使其成为ICIs治疗的优势人群。同时,由于HL肿瘤细胞数目并不多,而以微环境的细胞构成和表达异常为主,且不表达B细胞表面相关的标志物。但目前CAR-T作用靶点主要是CD19,使得CAR-T细胞在HL的治疗应用受限。对于NHL,仅少数类型具备9p24.1遗传性改变,而不都高表达PD-L1。因此,除了PD-L1以外,需要寻找其他可预测疗效的标志物,以筛选出免疫治疗潜在获益人群。其次,要确定免疫治疗的最佳时机、最佳组合和持续使用时间。目前免疫治疗主要被批准用于R/R患者的后线治疗,是否可用在疾病的早期阶段仍需进一步探讨,如作为移植前的抢救方案或作为初始诱导治疗的一部分。经PD-1抑制剂获得CR患者中,是否可停止治疗?何时停止治疗?若停止治疗后再次复发的患者,用PD-1抑制剂是否仍有效?这些问题均有待深入了解。第三,应关注免疫治疗相关不良反应。ICIs通过激活自身免疫系统发挥抗肿瘤作用,其药物相关不良反应会呈现多系统性、多样性及复杂性,可累及多种器官和组织,如皮肤反应、免疫相关肠炎、肝炎、肺炎、肾炎和内分泌毒性(下丘脑炎、垂体、甲状腺、肾上腺功能异常等)。CAR-T与TAA具有高度的亲和性,易因识别失误而攻击正常细胞,导致误伤现象,即“脱靶效应”,可导致细胞因子释放综合征,甚至可引起死亡。最后,要制定适宜的免疫疗效评价标准。虽然,目前监测恶性淋巴瘤患者疾病活动的标准依赖于PET/CT,但其对指导临床医生评估ICIs反应具有局限性。2007和2014修订版恶性淋巴瘤的疗效评价标准,仅适用于传统治疗模式。2016年提出“不确定反应”的反应标准,如假性进展和超进展。如何识别疾病进展与假性进展,仍是免疫治疗的一难点。目前,正在研究的循环肿瘤DNA(ct DNA)的分析有望成为监测患者肿瘤负荷的新方式。

