阿帕替尼联合多西他赛二线以上治疗对晚期非小细胞肺癌患者CEA、SCC及CA125的影响
尚 可 胡若洋 胡继德
非小细胞肺癌(NSCLC)是临床发病率最高的恶性肿瘤之一,其早期阶段常无明显症状,故多数患者确诊时已为晚期阶段,无法接受外科手术治疗[1-2]。目前,临床针对无法手术的晚期NSCLC患者常采取靶向治疗、化疗及放疗等手段进行治疗,其中含铂双药化疗是临床最常用的一线标准化疗方案,尽管该方案具有一定的效果,但治疗过程中多数患者可出现耐药,造成化疗效果逐渐下降,最终导致治疗失败,而多数二线或三线化疗的治疗效果更差,故如何积极探讨疗效显著的化疗方案是临床急需解决的一大问题[3-4]。为此,笔者采用阿帕替尼联合多西他赛治疗晚期NSCLC,疗效较好,现报告如下。
1 资料与方法
1.1 一般资料
将2016年1月至2018年1月本院收治的62例晚期NSCLC患者纳入本研究,并将上述对象随机分为观察组及对照组,每组31例。观察组中,男性19例,女性12例;年龄29~67岁,平均(56.1±6.2)岁;病理类型包括鳞癌4例、腺癌27例;按第7版肺癌分期标准,临床分期包括Ⅲb期21例,Ⅳ期10例。对照组中,男性20例,女性11例;年龄32~65岁,平均(54.3±6.0)岁;病理类型包括鳞癌5例、腺癌26例;按第7版肺癌分期标准,临床分期包括Ⅲb期22例,Ⅳ期9例。2组上述资料均基本一致(P>0.05)。
1.2 纳入标准
①根据《2010中国肺癌临床指南》[5]中相关标准,结合影像学及病理学检测结果,诊断为晚期NSCLC的患者;②年龄为18~70岁、KPS评分>70分、预期生存时间≥6个月的患者;③无法接收手术治疗,且一线化疗效果不佳的患者;④我院伦理委员会批准,本人同意参与并签署相关知情同意书的患者。
1.3 排除标准
①存在出血风险、不可控制的高血压、严重药物过敏史、严重凝血障碍、严重感染等多西他赛及阿帕替尼治疗禁忌症的患者;②存在严重精神疾病、心脑血管疾病、自身免疫性疾病及肝肾功能损伤的患者;③不配合治疗工作的患者;④EGFR、ALK基因突变患者。
1.4 治疗方法
对照组患者均采用多西他赛化疗:多西他赛静脉滴注,滴注时间为1 h,给药剂量75 mg/m2/次,1次/3周,3周/疗程。患者于治疗前1 d均口服给予地塞米松7 mg,12 h/次,连续服用3 d;同时给予常规保肝、护肝、止吐及预防过敏等对症支持治疗。观察组在对照组的治疗基础上另口服给予阿帕替尼,250 mg/次,逐步增量至500 mg/次,1次/d。两组患者均治疗4个疗程。
1.5 近期疗效评价[6]
治疗后,通过观察2组患者的有效率及控制率来评价近期疗效,疗效等级分别为完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD),其中有效率=(CR+PR)/总数×100%;控制率=(CR+PR+SD)/总数×100%。
1.6 2组生活质量评价
治疗前后,采用恶性肿瘤患者生活质量核心问卷(QLQ-C30)[7]对2组患者的生活质量进行评价,主要项目包括情绪功能、躯体功能、社会功能、认知功能及角色功能,各项目分值越高表示患者生活质量越好。
1.7 2组肿瘤标记物检测
治疗前后,分别收集2组静脉血,检测其中肿瘤标记物含量,主要项目包括癌胚抗原(CEA)、鳞状上皮细胞癌抗原(SCC)及糖蛋白抗原125(CA125)。
1.8 2组毒副作用观察
治疗期间,观察2组出现的毒副作用,主要项目包括过敏反应、心血管毒性、肝功能损伤、骨髓抑制、神经毒性及胃肠道反应等。
1.9 统计学方法
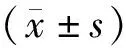
2 结果
2.1 2组近期疗效比较
治疗后,观察组有效率及控制率均明显高于对照组(P<0.05),见表1。

表1 两组患者疗效比较
注:*为与对照组比较,P<0.05。
2.2 2组生活质量比较
治疗前,2组情绪功能、躯体功能、社会功能、认知功能及角色功能评分均基本一致(P>0.05)。治疗后,2组上述评分均明显增高,且观察组均明显高于对照组(P<0.05),见表2。
2.3 2组肿瘤标记物比较
治疗前,2组CEA、SCC及CA125水平均基本一致(P>0.05)。治疗后,2组上述肿瘤标记物含量均明显增高,且观察组均明显高于对照组(P<0.05),见表3。

组别情绪功能躯体功能社会功能认知功能角色功能观察组 治疗前5.62±0.564.09±0.414.57±0.453.17±0.322.24±0.23 治疗后9.24±0.93∗#7.97±0.77∗#8.25±0.83∗#6.62±0.65∗#5.16±0.52∗#对照组 治疗前5.57±0.544.12±0.434.59±0.463.22±0.312.31±0.25 治疗后7.41±0.72∗6.43±0.66∗5.98±0.59∗5.16±0.51∗4.51±0.42∗
注:*为与对照组比较,P<0.05;#为与本组治疗前比较,P<0.05。

表3 2组肿瘤标记物水平比较
注:*为与对照组比较,P<0.05;#为与本组治疗前比较,P<0.05。
2.4 2组毒副作用比较
治疗期间,两组过敏反应、心血管毒性、肝功能损伤、骨髓抑制、神经毒性及胃肠道反应的发生率均无明显差异(P>0.05),见表4。
3 讨论
研究结果表明,近年来NSCLC的临床发病率呈现逐渐增高趋势,由于NSCLC早期诊断难度较大且发病较为隐匿,故多数NSCLC患者确诊时已处于晚期阶段[8-9]。化疗是晚期NSCLC的最常用的治疗手段,对于提高临床治疗效果、减少瘤细胞的转移及控制肿瘤细胞的增殖等方面均具有重要的意义,然而尽管临床上化疗药物的种类较多,但部分患者一线化疗效果并不理想,故临床仍需对化疗的方法进行不断的优化[10-12]。
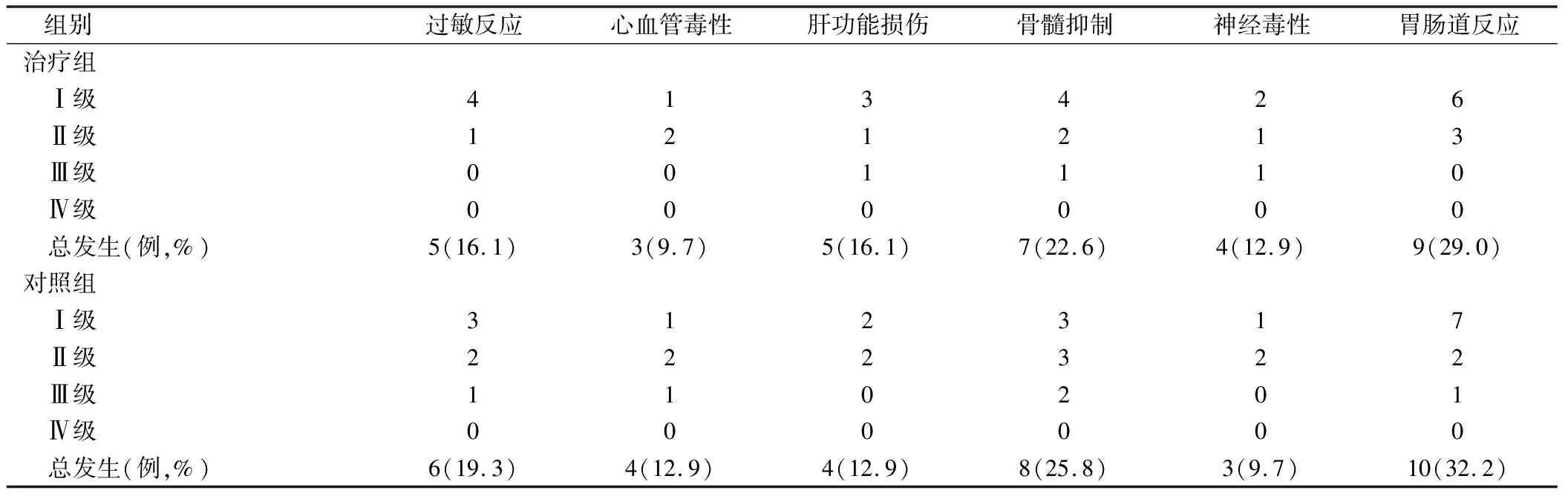
表4 2组毒副作用比较/例
多西他赛是临床经典的紫杉类抗肿瘤药物之一,该药物能够有效促进肿瘤细胞微管蛋白的聚合与解聚作用,从而形成具有较强稳定性的非功能微管蛋白束,最终达到抑制癌细胞的增殖与分裂作用[13]。大量研究结果表明,多西他赛是包括NSCLC在内的多种晚期恶性肿瘤的最佳支持治疗方案,对于延长患者的生存时间具有重要意义[14]。阿帕替尼是临床常用的小分子抗血管生成药物,可与血管内皮生长因子受体2(VEGFR-2)特异性结合,从而抑制VEGF与VEGFR-2的结合作用,阻断促血管生成的VEGF通路,进而阻碍肿瘤病灶微血管的形成作用,最终达到抗肿瘤的目的[15]。此外,该药物还具有逆转耐药基因等作用,降低化疗药物所引起的耐药性,从而提高化疗的成功率[16]。为此,笔者采用阿帕替尼联合多西他赛治疗晚期NSCLC,期望能够为NSCLC的临床治疗提供一定的依据。
本研究结果显示,观察组有效率及控制率均明显高于对照组,过敏反应、心血管毒性、肝功能损伤、骨髓抑制、神经毒性及胃肠道反应等毒副作用发生率与对照组均无明显差异,而CEA、SCC及CA125等各项肿瘤标记物含量均明显低于对照组,提示阿帕替尼有提高多西他赛单药治疗NSCLC疗效的可能,且不造成明显毒副作用。此外,观察组情绪功能、躯体功能、社会功能、认知功能及角色功能评分等生活质量评分均明显低于对照组,提示阿帕替尼有提高多西他赛单药治疗NSCLC疗效的可能。
综上所述,阿帕替尼联合多西他赛治疗晚期NSCLC显示出较好的疗效,有待进一步深入研究。

