金丝草化学成分及其体外抗HBV 活性
王慧娜, 尹志峰, 尹 鑫, 李洪波, 赵桂琴∗
(1.承德医学院中药研究所,河北省中药研究与开发重点实验室,河北 承德067000;2. 承德市农林科学院,河北 承德067000)
金丝草为禾本科金发草属植物金丝草Pogonatherum crinitum(Thunb.)Kunth 的干燥全草,味微苦、性寒,无毒,具有清热解毒、凉血止血、解暑利尿等功效,民间用于治疗感冒高热、尿路感染、黄疸型肝炎和糖尿病等症。研究表明,金丝草提取物对小鼠肝损伤有一定保护作用[1],可剂量依赖性的抑制乙型肝炎病毒(HBV) 分泌表面抗原(HBsAg)[2]。目前从金丝草中分离得到的化学成分主要为黄酮、甾体及酚酸类[3]。
为阐明金丝草抗HBV 药效物质基础,寻找抗HBV 活性天然化合物,本课题组采用活性追踪方法,对金丝草70%乙醇提取物的活性部位开展了分离纯化、结构鉴定及活性评价工作[4-6]。本研究从正丁醇活性部位分离得到的8 个化合物,所有化合物均为首次从金发草属植物中分离得到,化合物6 对HepG2.2.15 细胞分泌表面抗原(HBsAg) 及e 抗原(HBeAg) 有一定的抑制作用,IC50分别为55.5、69.5 μg/mL。
1 材料
VG Zabspec 高分辨磁质谱仪(英国Micromass公司);WNMR-1-500 超导核磁共振仪(TMS 为内标,武汉中科波谱技术有限公司);RZ-6 型冷冻干燥机(德国Martin Christ 公司);LC-10 A 型高效液相色谱仪(日本岛津公司);X-4 型显微熔点测定仪(河南豫华仪器有限公司);GZX-9070MBE 型电热恒温鼓风干燥箱(上海博讯实业有限公司医疗设备厂);DNM-9602 型酶标仪(北京普朗新技术有限公司);RE-52B 型旋转蒸发仪(上海亚荣生化仪器厂);二氧化碳孵箱(美国Forma 公司);SQP 124-1CN 型电子分析天平(德国Sartorius公司)。
Sephadex LH-20(瑞典GE Healthcare 公司);柱色谱硅胶(青岛海洋化工厂);AB-8 大孔吸附树脂(南开大学化工厂)。HBeAg ELISA 检测试剂盒(北京科卫临床诊断试剂有限公司);HBsAg ELISA 检测试剂盒(北京科卫临床诊断试剂有限公司);DMEM 培养基(美国Gibco 公司);胎牛血清(杭州四季青试剂有限公司);噻唑蓝(MTT,美国Amresco 公司);拉米夫定(3TC,美国葛兰素史克公司,批号K026520,含有量>99%);色谱纯甲醇(北京迈瑞达公司)。HepG2.2.15 细胞株由美国Mount Sinai 医学中心构建,军事医学科学院引进馈赠,自行传代培养。
金丝草药材2016 年12 月购于河北安国药材交易中心,经军事医学科学院放射与辐射医学研究所生药学博士李彬鉴定为禾本科金发草属植物金丝草Pogonatherum crinitum(Thunb.)Kunth 的干燥全草,样品标本(JSC201612) 保存于承德医学院中药研究所。
2 提取与分离
金丝草干燥全草20 kg,用8 倍量70%乙醇回流提取3 次,每次2 h,合并提取液,减压浓缩得浸膏4.2 kg。浸膏依次用石油醚、氯仿、乙酸乙酯及水饱和正丁醇萃取,分别得石油醚部位(24 g)、氯仿部位(165 g)、乙酸乙酯部位(121 g)、正丁醇部位(260 g) 及水层浸膏。
正丁醇部位经大孔树脂柱色谱,依次用水,30%、60%、95%乙醇洗脱。60%乙醇洗脱物63 g用硅胶柱色谱分离,分别用氯仿-甲醇(20 ∶1、10 ∶1、5 ∶1) 及氯仿-甲醇-水(90 ∶35 ∶6、60 ∶35 ∶10) 梯度洗脱,薄层色谱同步检测,合并相似组分得Fr.A~E 5 个部分。
取Fr.B 部位5.6 g,甲醇溶解,硅胶拌样后干法上柱,经硅胶柱色谱分离,氯仿-甲醇(20 ∶1、10 ∶1、5 ∶1) 梯度洗脱,薄层色谱同步检测,合并相似组分得Fr.B2A ~B2D 4 个部分。Fr.B2A 部分经Sephadex LH-20 柱 (氯仿-甲醇,1 ∶1) 分离,重结晶法 (甲醇-水) 纯化, 得化合物6(13.7 mg)。取Fr.C 部位6.1 g,甲醇溶解,硅胶拌样后干法上柱,经硅胶柱,氯仿-甲醇-水(20 ∶1、10 ∶1、5 ∶1) 梯度洗脱, 合并相似组分得Fr.C2A ~C2E 5 个部分。Fr.C2A 部分经Sephadex LH-20 柱(氯仿-甲醇,1 ∶1) 反复分离纯化,得化合物7(22.6 mg)。Fr.D 部位4.2 g,经聚酰胺柱色谱分离,乙醇-水(1 ∶4、1 ∶1、7 ∶3) 梯度洗脱,合并相似组分得Fr.D2A ~D2D 4 个部分,Fr.D2B 部分经反复聚酰胺柱色谱,乙醇-水(1 ∶1) 洗脱,结合半制备HPLC 纯化, 得化合物1(10.1 mg)、5(11.9 mg)。Fr.E 部位3.1 g,经硅胶柱色谱反复分离,氯仿-甲醇-水(90 ∶35 ∶6、60 ∶35 ∶10) 洗脱,Sephadex LH-20 纯化,甲醇-水(55 ∶45) 洗脱,得化合物3 (10.8 mg)、4(13.7 mg)。95%乙醇洗脱物33 g 经硅胶柱,氯仿-甲醇 (20 ∶1、10 ∶1、5 ∶1) 及氯仿-甲醇-水(90 ∶35 ∶6、60 ∶35 ∶10) 梯度洗脱,经薄层色谱检测后合并相同组分,得Fr.F~I 5 个部分,Fr.G 部分3.5 g,经硅胶柱,氯仿-甲醇-水(90 ∶35 ∶6、60 ∶35 ∶10)洗脱,重结晶法(氯仿-甲醇,1 ∶1)纯化,得化合物2(13.1 mg)、8(8.8 mg)
3 结构鉴定
化合物1:黄色粉末,mp 263 ~265 ℃,ESIMS m/z:593[M+H]-,分子式为C28H32O14。1HNMR(DMSO-d6, 400 MHz) δ: 12.92 (1H, s,5-OH),8.02 (2H, d, J=8.8 Hz, H-2′, 6′),7.15 (2H, d, J = 8.8 Hz, H-3′, 5′), 6.97(1H,s,H-3),6.80(1H,d,J=2.0 Hz,H-8),6.80(1H,d,J=2.0 Hz,H-8),6.80(1H,d,J=2.0 Hz,H-6),5.05(1H,d,J=7.2 Hz,H-1″), 4.52 (1H, d, J=2.2 Hz, H-1‴), 3.88(3H, s, H-OCH3),1.05 (3H, d, J=6.2 Hz,H-6‴);13C-NMR(DMSO-d6,100 MHz) δ:181.3(C-4),163.1(C-2),162.4 (C-7),162.0 (C-9),160.6(C-4′),156.5 (C-5),128.1 (C-2′,6′), 122.0 (C-1′), 114.4 (C-3′, 5′), 105.1(C-10),100.1(C-1‴),99.5(C-1″),99.2(C-6), 94.1 (C-8), 75.8 (C-3″), 75.2 (C-5″),72.6(C-2″),71.6(C-4‴),70.2(C-3‴),69.9(C-2‴),69.1 (C-4″),67.6 (C-5‴),65.6 (C-6″),55.3(C-OCH3),17.1(C-6‴)。以上数据与文献[7] 基本一致,故鉴定为5-羟基-4′-甲氧基黄酮-7-O-芸香糖苷。
化合物2:黄色针晶(氯仿-甲醇),mp 189 ~191 ℃, ESI-MS m/z:289[M+H]+, 分子式为C15H12O6。1H-NMR(CDCl3, 400 MHz) δ: 13.11(1H,s,1-OH),7.36(1H,d,J=10.0 Hz,H-6), 7.13 (1H, d, J=10.0 Hz, H-5), 6.35(1H,d,J=2.0 Hz, H-4),6.30 (1H, d, J=2.0 Hz, H-2), 5.93 (1H, brs, 7-OH), 4.07(3H,s,8-OCH3),3.86(3H,s,3-OCH3);13CNMR(CDCl3, 100 MHz) δ: 180.5 (C-CO),166.3 (C-8), 163.1 (C-7), 157.1 (C-1),150.1 (C-3), 145.7 (C-4a), 144.1 (C-4b),122.3 (C-6), 114.7 (C-8a), 113.5 (C-5),103.9(C-8b),96.8 (C-2),92.4 (C-4),62.4(C-8-OCH3),55.6 (C-3-OCH3)。以上数据与文献[8] 基本一致,故鉴定为1,7-二羟基-3,8-二甲氧基呫吨酮。
化合物3:黄色粉末,mp 181 ~183 ℃,ESIMS m/z:577[M-H]+, 分子式为C30H26O12。1HNMR(DMSO-d6, 600 MHz) δ: 12.98 (1H, s,5-OH), 10.35 (1H, brs, 4′-OH), 9.96 (1H,brs,4‴-OH),7.91 (2H, d, J=9.0 Hz, H-2′,6′),7.45 (1H, d, J=16.2 Hz, H-7‴), 7.37(2H,d,J=8.4 Hz,H-2‴,6‴),6.89(2H,d,J=9.0 Hz, H-3′, 5′), 6.80 (1H, s, H-3),6.78(1H,d,J=2.4 Hz,H-8),6.64(2H,d,J=8.4 Hz, H-3‴,5‴),6.44 (1H, d, J=2.4 Hz,H-6),6.31 (1H, d, J=16.2 Hz, H-8‴),5.11 (1H, d, J = 7.8 Hz, H-1″); 13C-NMR(DMSO-d6, 150 MHz) δ: 181.7 (C-4), 166.6(C-9‴),164.0(C-7),162.5(C-2),161.1(C-9),160.8 (C-4′), 159.5 (C-4‴), 156.6 (C-5),144.7 (C-7‴), 130.1 (C-2‴, 6‴), 128.4 (C-2′,6′), 124.7 (C-1‴), 121.0 (C-1′), 116.2(C-3′,5′),115.8 (C-3‴,5‴),113.7 (C-8‴),105.4 (C-10), 103.1 (C-3), 99.4 (C-1″),99.2(C-6), 94.8 (C-8), 76.1 (C-3″), 73.8(C-5″), 72.9 (C-2″), 69.7 (C-4″), 63.3 (C-6″)。以上数据与文献[9] 基本一致,故鉴定为芹菜素-7-O-β-D-(6″-E-p-香豆酰基) -葡萄糖苷。
化合物4:白色粉末,mp 172 ~174 ℃,ESIMS m/z:577[M-H]+, 分子式为C27H30O14。1HNMR(C5D5N,400 MHz) δ:8.21 (1H, s, H-2),8.08(1H,d,J=8.9 Hz,H-5),7.01(1H,d,J=8.9 Hz,H-6),7.40(2H,d,J=8.0 Hz,H-2′,6′), 6.87 (1H, d, J=8.0 Hz, H-3′,5′),5.14 (1H, d, J=8.0 Hz, H-1″), 4.96(1H,d,J=7.2,H-1‴);13C-NMR(C5D5N,100 MHz) δ: 175.4 (C-4), 162.1 (C-7), 158.3(C-4′),157.6(C-9),153.1(C-2),130.4(C-2′, 6′), 126.3 (C-1′), 124.2 (C-3), 127.5(C-5),115.9 (C-6),104.1 (C-8),119.5 (C-10), 116.0 (C-3′, 5′), 101.8 (C-1‴), 101.5(C-1″),78.9 (C-5‴),78.5 (C-5″), 78.2 (C-3‴),78.1(C-3″),74.7(C-2″),74.6 (C-2‴),71.1 (C-4″, 4‴),62.2 (C-6‴), 62.1 (C-6″)。以上数据与文献[10] 基本一致,故鉴定为大豆素-7,4′-二-O-葡萄糖苷。
化合物5:淡黄色粉末,mp 215~217 ℃,ESIMS m/z:625[M+H]+,分子式为C28H32O16。1HNMR (DMSO-d6, 400 MHz) δ: 7.81 (1H, d,J=2.0 Hz,H-2′),7.51(1H,dd,J=8.4,2.0 Hz,H-6′), 6.85 (1H, d, J=8.4 Hz, H-5′),6.45(1H,d,J=2.0 Hz,H-8),6.21(1H,d,J=2.0 Hz,H-6),5.63(1H,d,J=7.2 Hz,H-1″),4.54 (1H, s, H-1‴), 1.09 (3H, d, J=6.0 Hz, H-6‴);13C-NMR (DMSO-d6,150 MHz)δ:177.4 (C-4), 164.2 (C-7), 161.3 (C-5),156.6 (C-2), 156.6 (C-9), 149.4 (C-4′),147.0 (C-3′), 133.1 (C-3), 122.2 (C-1′),121.1 (C-6′), 115.4 (C-5′), 113.3 (C-2′),104.1 (C-10), 101.2 (C-1″), 100.9 (C-1‴),98.8(C-8), 93.9 (C-6), 76.5 (C-2″), 76.0(C-3″),74.3 (C-5″),71.8 (C-4‴), 70.7 (C-3‴),70.6(C-4″),68.4(C-5‴),68.4(C-2‴),66.9(C-6″),55.8(C-4′-OCH3),17.6(C-6‴)。以上数据与文献[11] 基本一致,故鉴定为5,7,3′-三羟基-4′-甲氧基黄酮-3-O-芸香糖苷。
化合物6:白色颗粒结晶(甲醇-水),mp 201~203 ℃, ESI-MS m/z:208[M+H]+, 分子式为C11H13NO3。1H-NMR (DMSO-d6, 600 MHz) δ:12.62(1H, brs, HCOOH),8.14 (1H, d, J=8.0 Hz, H-NH),7.27 (2H, dd, J=7.4, 6.4 Hz,H-3′,5′), 7.21 (1H, d, J=6.4 Hz, H-4′),7.20(2H,d,J=7.4 Hz,H-2′,6′),4.37(1H,ddd, J=9.0, 8.4, 4.8 Hz, H-2), 3.01(1H,dd,J=13.0,4.8 Hz,H-3b),2.81(1H,dd,J=13.8,9.0 Hz,H-3a),1.75(3H,s,HCH3);13C-NMR (DMSO-d6,150 MHz) δ:169.1(C-NHCO),137.0(C-1′),133.1(C-1),129.2(C-3′, 5′), 128.3 (C-2′, 6′), 126.4 (C-4′),53.2(C-2),36.5(C-3),22.1(C-CH3)。以上数据与文献[12] 基本一致,故鉴定为N-乙酰苯丙氨酸。
化合物7:黄色油状液体,ESI-MS m/z:144[M+H]+,分子式为C6H9NO3。1H-NMR(DMSO-d6,600 MHz)δ:1.95(3H,m,H-3a),2.11(2H,m, H-3b, 4a), 2.35 (1H, m, H-4b), 3.66(3H,s,H-OCH3),4.15(1H,dd,J=9.2,4.0 Hz, H-2), 7.93 (1H, brs, H-NH);13C-NMR(DMSO-d6, 150 MHz) δ: 176.7 (C-5), 173.3(C-1),54.3(C-OCH3),52.3(C-2),29.1(C-4),24.1(C-3)。以上数据与文献[13] 基本一致,故鉴定为焦谷氨酸甲酯。
化合物8:白色颗粒结晶(氯仿-甲醇),mp 101~103 ℃,ESI-MS m/z:189[M+H]+,分子式为C9H16O4。1H-NMR (DMSO-d6, 400 MHz) δ:11.99(2H, s, H-OH), 2.19 (4H, t, J=7.2 Hz,H-2, 8), 1.49 (4H, m, H-3, 7), 1.25(6H,brs,H-4,5,6);13C-NMR(DMSO-d6,100 MHz) δ: 174.5 (C-1), 33.0 (C-2, 8), 28.4(C-3, 7), 24.3 (C-4, 6)。 以 上 数 据 与 文 献[14] 基本一致,故鉴定为杜鹃花酸。
4 体外抗HBV活性
选取生长良好的HepG2.2.15 细胞,用胰蛋白酶消化成单细胞悬液,接种于96 孔细胞培养板,每孔200 μL,37 ℃,5%CO2培养24 h。药物以适量DMSO 溶解(阳性对照,拉米夫定),DMEM 培养液2 倍稀释成6 个质量浓度,分别加入到细胞培养上清中,培养4 d 后更换相同质量浓度药物培养液,收集用药后第8 天细胞培养上清,按HBsAg、HBeAgELISA 检测试剂盒说明书测定吸光度值,计算抗原抑制率及半数抑制浓度(IC50)[15]。MTT 法测试药物细胞毒性[16],计算细胞存活率及半数细胞毒浓度(CC50)。数据用Origin 软件处理,采用t检验。见表1。
结果表明,化合物6 对HepG2.2.15 细胞分泌表面抗原(HBsAg) 及e 抗原(HBeAg) 均有一定的抑制作用,IC50分别为55.5、69.5 μg/mL,且选择指数SI 均大于2。
5 讨论
金丝草为金发草属植物中可入药的品种之一,民间可用于治疗黄疸型肝炎[17]。在课题组前期研究基础上,本实验针对金丝草70%乙醇提取物的正丁醇萃取部位进行抗HBV 活性成分的分离纯化、结构鉴定及体外活性检测。共分离得到8 个单体化合物,其中包括4 个黄酮苷、1 个呫吨酮苷元、2个氨基酸类及1 个高级脂肪酸。体外活性检测结果表明,化合物6 对HepG2.2.15 细胞分泌HBsAg 及HBeAg 均有一定的剂量依赖性的抑制作用具有一定的深入研究价值,以期阐明金丝草药材的药效物质奠定基础,并为抗HBV 新药的研发提供科学依据。
表1 化合物6 的体外抗HBV 活性Tab.1 Anti-HBV activity of compound 6 in vitro
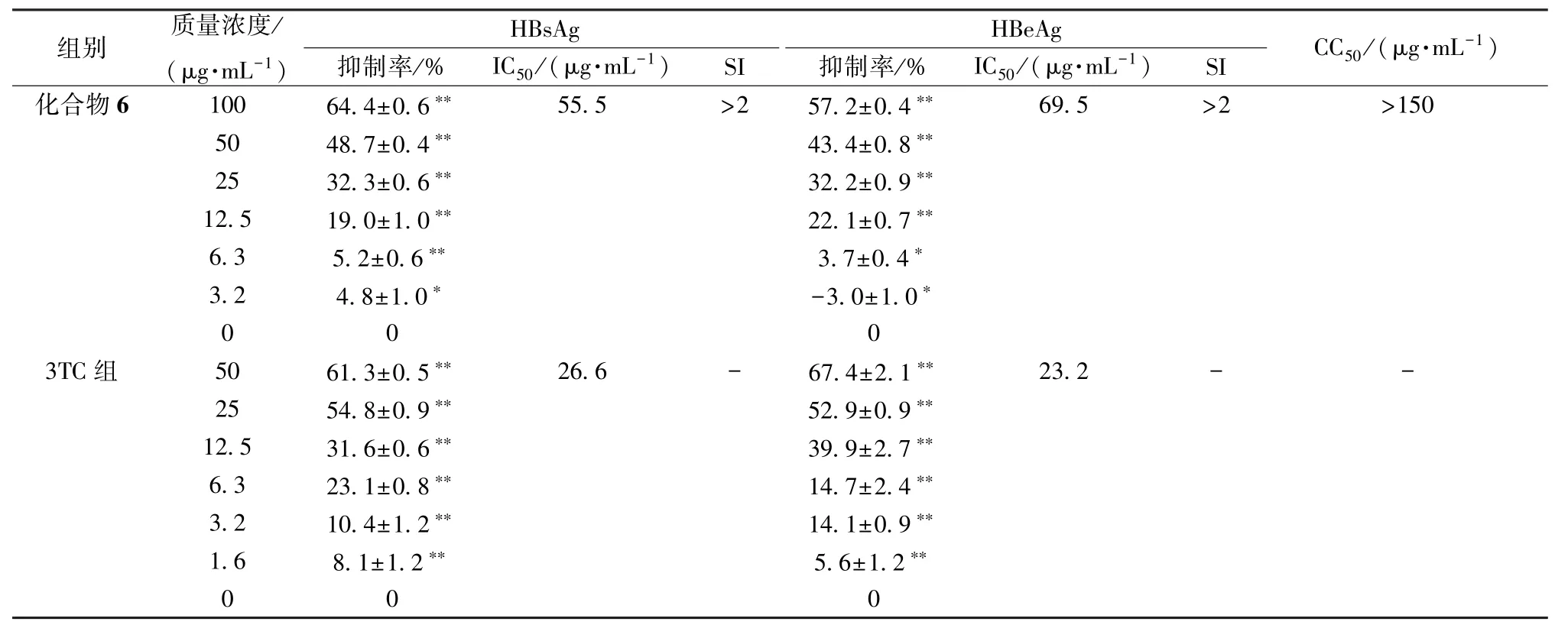
表1 化合物6 的体外抗HBV 活性Tab.1 Anti-HBV activity of compound 6 in vitro
注:IC50为半数抑制浓度;CC50为半数细胞毒浓度;SI 为选择指数,CC50/IC50;3TC 为拉米夫定;与0 μg/mL 组比较,∗P<0.05,∗∗P<0.01
组别 (质μ量g·m浓L度-1/) 抑制率/% IC H 50B/s(Aμg g·mL-1) SI 抑制率/% IC H 50B/e(Aμg g·mL-1) SI CC50/(μg·mL-1)化合物6 100 64.4±0.6∗∗55.5 >2 57.2±0.4∗∗69.5 >2 >150 50 48.7±0.4∗∗43.4±0.8∗∗25 32.3±0.6∗∗32.2±0.9∗∗12.5 19.0±1.0∗∗22.1±0.7∗∗6.3 5.2±0.6∗∗3.7±0.4∗3.2 4.8±1.0∗-3.0±1.0∗0 00 3TC 组 50 61.3±0.5∗∗26.6 - 67.4±2.1∗∗23.2 - -25 54.8±0.9∗∗52.9±0.9∗∗12.5 31.6±0.6∗∗39.9±2.7∗∗6.3 23.1±0.8∗∗14.7±2.4∗∗3.2 10.4±1.2∗∗14.1±0.9∗∗1.6 8.1±1.2∗∗5.6±1.2∗∗0 00

