锶-铜异金属配位聚合物的合成、晶体结构及发光性质研究
冯子坤, 熊 刚, 孙亚光
(沈阳化工大学 应用化学学院, 辽宁 沈阳 110142)
配位化学的主要研究对象为配位化合物[1],配位聚合物(Coordination Polymers)属于配位化合物,通常是由过渡金属离子与含氧、含氮等多齿有机配体通过自组装过程形成的晶体材料[2].近年来,配位聚合物的设计合成已经引起了化学工作者的广泛关注,不仅因为配合物具有新颖的网络拓扑结构,而且在很多领域,如磁性材料[3-4]、荧光材料[5]、催化材料[6-7]、光学材料[8]和吸附分离[9]等,都具有潜在的应用价值,是近年来研究的热点之一.
4-[2-(4-吡啶)乙烯基]苯甲酸(HPC)是一个既含有氮杂环又含有芳香环的功能型配体,由于含氮配体种类和构型的多样性,因此,在已报道过的配合物中,含氮配体占有很大部分.例如,苯并咪唑及其衍生物[10]、三氮唑及其衍生物[11]等等,它们能够和适当的金属离子结合成稳固的M—N配位共价键,所以,可以提供更多的配位模式,为新型配合物的形成创造了良好的条件[12-13].同时与过渡金属配位聚合物相比,碱土金属离子表现出较高的配位数和更为自由的配位几何构型,使其更容易形成丰富多样的结构[14].本文以4-[2-(4-吡啶)乙烯基]苯甲酸为配体,与硝酸锶和碘化亚铜在溶剂热条件下反应,得到了一例二维网状配位聚合物[SrCu2I2(HPC)2]n·nDMF.X射线单晶结构分析表明:配合物1是由Cu2I2无机链与由HPC中的羧酸连接Sr(Ⅰ)组成的Sr(HPC)2链组装而成的二维网状结构.通过研究配合物的荧光光谱,发现配合物1在450 nm处有较强的发射谱,源于I→Cu的电荷转移,发射蓝色荧光.
1 实验部分
1.1 试剂与仪器
所有试剂均为市售分析纯,使用过程中未做任何纯化处理,实验中所用水为蒸馏水.元素分析使用Perkin-Elemer 470 型元素分析仪;红外光谱测定使用Nicolet IR-408 型红外光谱仪(KBr压片),波长范围为4 000~400 cm-1;粉末X射线衍射采用BRUKER D8 ADVANCE(Cu Kα 辐射)测定;单晶测定采用Bruker SMART1000 CCD 面探衍射仪;荧光光谱采用日立F-4600荧光分光光度计测试;核磁共振氢谱采用Bruker Avance 500 型核磁共振仪测定.
1.2 配位聚合物的合成
1.2.1 配体的合成
将4.9 mL的4-甲基吡啶和7.6 g的4-醛基苯甲酸混合于40 mL乙酸酐中,并在搅拌的前提下145 ℃加热回流8 h,待冷却至室温后,将其抽滤,并用水洗涤数次,然后用乙醇洗涤数次,再用乙醚洗涤数次,最后将固体真空干燥,可得到黄白色粉末,产率为71 %.配体HPC合成路线如下:

HPC配体的1H NMR(500 MHz,DMSO-d6)δ:7.95(d,2H),8.58(d,2H),7.74(d,2H),7.62(d,2H),7.45(d,2H).
1.2.2 [SrCu2I2(HPC)2]n·nDMF的合成
取HPC(1 mmol,0.225 2 g)、Sr(NO3)2(1 mmol,0.211 6 g)、CuI(0.5 mmol,0.095 2 g)和10 mL DMF 混合均匀,置于25 mL 聚四氟乙烯内衬并密封于不锈钢反应釜中,在160 ℃烘箱中反应24 h,然后经24 h程序降温至室温,得到橘黄色的块状晶体;用DMF洗净并在空气中自然晾干,产率为:69 %.元素分析:w(C)/%,36.89,w(H)/%,2.71,w(N)/%,4.35(实验值);w(C)/%,36.86;w(H)/%,2.66;w(N)/%,4.30(理论值).红外数据(KBr,cm-1):(s:强峰,m:中强度峰,w:弱峰)3 423.77(m),2 923.88(w),2 359.91(w),2 340.60(w),1 648.7(s),1 592.69(s),1 539.08(s),1 491.50(w),1 402.53(s),959.45(m),851.50(m),809.17(m),770.69(w),703.44(w),672.36(w),535.80(w).
1.3 配合物的晶体测定
选取适当尺寸的晶体,在293 K下,采用BRUKER SMART 1000 型X-射线衍射仪,以经石墨单色器单色化的Mo-Kα射线(λ=0.071 073 nm)作入射光收集数据.非氢原子均采用直接法解出,并用最小二乘法进行各向异性温度因子修正;氢原子的位置通过理论加氢得到.配合物1的主要晶体学数据见表1.

表1 配合物1的晶体学数据
2 结果与讨论
2.1 分子结构描述
通过单晶X射线衍射结果可知:此配合物属于单斜晶系,P21/a空间群.分子配位模式如图1所示.在配合物1的不对称结构单元中含1个Sr(Ⅱ)、2个Cu(Ⅱ)、2个HPC配体和1个配位DMF.中心离子Sr(Ⅱ)的配位数是位于八配位的呈略微扭曲的双帽反三棱柱几何构型的中心位置,其顶点被8个氧原子占据,其中O1、O2、O3A、O2A、O3和O4A来自于4个HPC配体上的羧基上氧原子,O5和O5A来源于配位DMF分子中的氧原子.Sr—O键长分布在0.247 1(4)nm到0.274 4(4) nm之间,O—Sr—O键角在49.54(12)°到157.62(13)°之间.两个晶体学独立的Cu(Ⅰ)中心离子的配位几何构型相同,均是四配位的正方形构型,其顶点由3个碘原子和1个来自于HPC配体上的吡啶氮原子N1所组成,Cu—I键长在0.256 49(16)nm到0.304 00(19)nm之间,Cu—N键长为0.201 4(5)nm和0.203 4(5)nm,I—Cu—I键角在57.74(4)°到121.04(4)°之间,N—Cu—I键角在106.34(18)°到134.45(16)°之间,配合物的主要键长和键角见表2、表3,这与文献中已报道的Sr配合物中的键长和键角相似[15].
HPC上的羧基氧原子O2和O3以及DMF分子上的羰基氧原子O5均使用μ2桥连配位模式将相邻的Sr(Ⅱ)连接成Sr(HPC)2一维链[图2(a)],该链沿着b轴排列,相邻的Sr(Ⅱ)原子之间的距离为0.385 0 nm.I1和I2阴离子以μ2桥连配位模式将相邻的Cu(Ⅰ)连接形成Cu2I2双核单元.在双核单元中,Cu1—Cu2之间的距离为0.266 20(16) nm,小于两个Cu(Ⅰ)离子的范德华半径之和(0.28 nm),因此,可以推测存在弱的Cu—Cu键[16].I2阴离子使用μ4的多齿的配位模式将相邻的Cu2I2双核单元连接形成一维Cu2I2无机链[图2(b)].如图3所示,相邻的Sr(HPC)2一维链与一维Cu2I2无机链之间通过HPC配体中吡啶氮原子在ab平面连接形成了一个二维层状结构.一维Sr(HPC)2链与一维Cu2I2无机链是交替排列的,相邻链之间的距离大约为1.4 nm.目前为止,在文献中HPC配体主要与Zn(Ⅱ)和Cd(Ⅱ)等过渡金属制备单一金属的配位聚合物[17],由其所构成的异金属合成的配位聚合物未见报道.
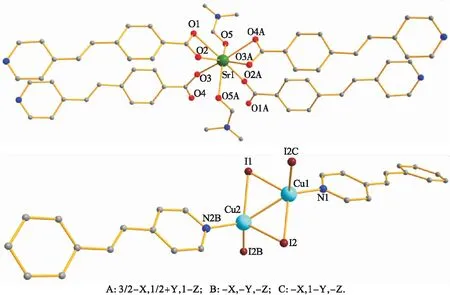
图1 配合物1中Sr2+和Cu2+的配位模式
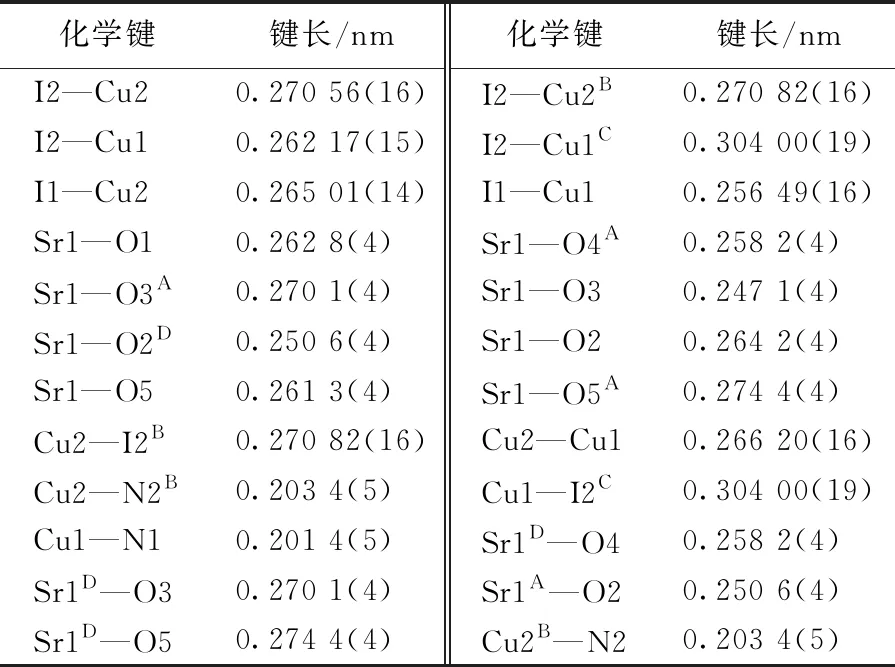
表2 配合物1的主要键长

表3 配合物1的主要键角
A: 3/2-X,1/2+Y,1-Z; B: -X,-Y,-Z; C:-X,1-Y,-Z; D:3/2-X,-1/2+Y,1-Z.

图2 配合物1中的Sr(HPC)2和Cu2I2一维链
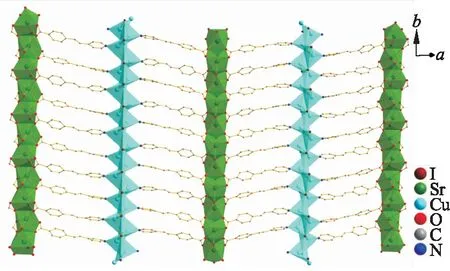
图3 配合物1的二维网状结构
2.2 配合物的PXRD
为了检测所获得单晶样品的纯度,在室温下,2θ在5°~50°之间,对配合物进行粉末X射线衍射测试分析,结果如图4所示.从PXRD的表征结果可以看出:实验测得的PXRD衍射峰位置与模拟的PXRD衍射峰位置基本一致,说明所合成的配合物1的物相结构与模拟结构基本一致.这一结果表明所合成的配合物1为纯相.

图4 配合物1的粉末衍射谱图以及单晶结构数据模拟谱图
3 配合物的发光性质
配合物1和配体HPC的荧光光谱由日立F-4600荧光分光光度计测试,激发波长为320 nm,其荧光发射光谱如图5所示.由图5可以看出:配体的发射光谱主要位于350~450 nm波长范围内,主要的激发峰位于365 nm,可归属于π*—π跃迁;配合物1的发射光谱呈现两个较强而宽的荧光发射峰,分别在398 nm和450 nm处,这分别源于π*—π跃迁和 I→Cu 的电荷转移(XMCT),其中450 nm处的发射强度略强,处于可见光区域且显示蓝光发射,因此,配合物1可作为潜在的蓝光荧光材料.
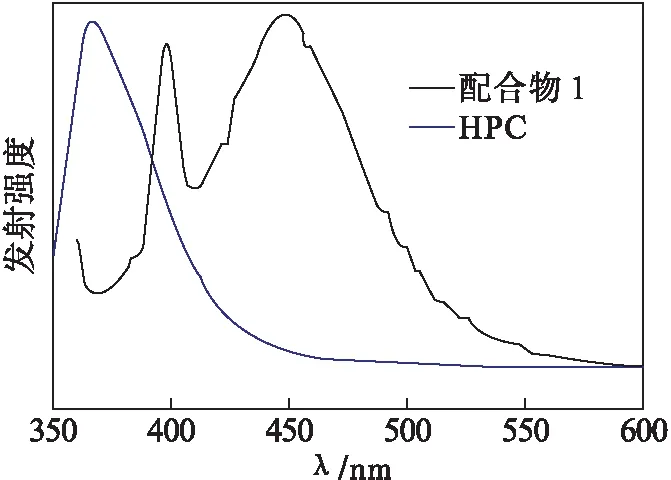
图5 配合物1和配体HPC的荧光发射光谱
4 结 论
通过溶剂热法,以吡啶-4-乙烯基-对苯甲酸(HPC)为配体,碘化亚铜和硝酸锶为金属源,合成了一种新颖的二维异金属配合物,该配合物是由Cu2I2无机链与Sr(HPC)2链组装而成.研究配合物的荧光光谱发现:配合物1在450 nm处有强的发射谱,发射蓝色荧光,因此,配合物1可作为潜在的蓝光荧光材料.

