甲硝唑口颊片的释放度测定及不同测定方法的结果比较
谢莉 张亿 朱蓉 熊玲 陈红
(成都市食品药品检验研究院,成都 610045)
甲硝唑是临床使用历史较久的一种广谱抗厌氧菌药和抗滴虫药,其不同给药途径分别发挥着全身作用和局部作用。当其发挥全身作用时,由于较多副作用的产生,已逐渐被替硝唑、奥硝唑等硝基咪唑类衍生物替代。当其制成栓剂、凝胶等剂型局部给药时,发挥着良好的疗效,并且副作用少。甲硝唑口颊片可用于牙龈炎、牙周炎、冠周炎及口腔溃疡,一般将其置于牙龈和龈颊沟间含服,用于口腔溃疡时黏贴于黏膜患处。目前该品种有两个生产厂家。中国药典以及其他国家药典均未收载该品种。两厂家样品的执行标准分别为YBH03122014[1]以及WS1-(X-523)-2003Z[2],两标准进行的释放度检查采用的装置均为小杯法,溶出介质均为0.1mol/L的盐酸溶液,测定方法分别为HPLC法和UV吸收系数法。但由于唾液的pH值为6.0~7.5[3],原释放度检查方法采用的溶出介质酸度太高,不能模拟药物溶出的真实生理环境,介质选择不合理。且美国FDA溶出方法数据库中公布的口腔用药膜或药物贴片的溶出介质多为磷酸盐缓冲液[4],本研究采用磷酸盐缓冲液(pH6.6)作为溶出介质。
小杯法是我国特有的溶出度检查方法,最早收载于1995年版中国药典。该方法被收载的主要原因是20多年前,仪器的检测灵敏度低,小剂量固体制剂在篮法和桨法装置下的样品溶液浓度低于仪器检测灵敏度,小杯法通过使用较少的溶出介质,提高了样品溶液的浓度,使得小剂量固体制剂的溶出度有法可控,得以全面控制该类固体制剂的质量。而现阶段仪器的检测灵敏度普遍较高,用桨法检查小剂量固体制剂也能找到与之相适的高灵敏度检测方式,保留小杯法的现实意义值得重新考虑。
流通池法是一种较新的释放度检查方法,有闭环和开环两种系统,以满足不同药品的需求。其中,闭环式流通池法将样品置于样品架或者玻璃珠上,在恒流泵的作用下,溶出介质经过恒温装置由流通池下端进入,通过样品表面后,经过流通池上端的过滤装置流出,回到介质瓶,溶出介质循环使用,样品溶液从介质瓶进行采集。开环式流通池法为新鲜介质经过样品的溶出介质后不回到介质瓶,滤过后进入样品收集器。流通池法的流体力学与传统溶出度检查法完全不同,且可以用于微量药物制剂、药物支架、缓控释制剂、透皮贴剂、速释制剂等,能解决制剂漂浮的问题,并且在体内外相关性上有更好的发展空间[5]。目前,流通池法被国际广泛认可,被收载于美国药典(USP)、欧洲药典(EP)、英国药典(BP)及日本药局方(JP),中国药典尚未收载该方法,由于仪器昂贵,目前国内针对该方法的研究报道也较少[6-11],国外使用该方法进行溶出度测定的品种也极少。
考虑到小杯法被收入中国药典的历史局限性,且其他国家药典均未收载小杯法,为与国际接轨,本研究采用USP四法流通池法和中国药典一法篮法分别对甲硝唑口颊片释放度进行检查,并与原标准的小杯法进行比较。
1 仪器与试药
CE7 smart溶出度仪(瑞士Sotax公司),SotaxAT7 smart溶出度仪(瑞士Sotax公司),Sotax AT xtend溶出度仪(瑞士Sotax公司),MPS溶媒制备仪(瑞士Sotax公司),1260高效液相色谱仪(美国Aglilent公司),BP211D 电子天平(Sartorius公司),Whatman GF/F玻璃纤维滤膜,Whatman GF/D玻璃纤维滤膜。
甲硝唑对照品(批号:100191-201507,中国食品药品检定研究院),甲硝唑口腔黏贴片(规格:3mg;A厂,批号170103;B厂,批号:170904),甲醇为色谱纯,其他试剂均为分析纯。
2 方法与结果
2.1 释放度试验方法
2.1.1 流通池法
采用USP溶出度四法流通池法的闭合系统装置,将本品放入片夹,置于锥形部装满玻璃珠(直径1mm)的流通池内,以磷酸盐缓冲液(pH6.6)100mL为溶出介质,温度为37℃,流速为4mL/min,于20、50、90、120、180、240和300min取已在线滤过的样品溶液1mL,作为供试品溶液。
2.1.2 篮法
采用中国药典溶出度一法篮法装置,以磷酸盐缓冲液(pH6.6)500mL为溶出介质,转速为50r/min,温度为37℃,于20、50、90、120、180、240和300min取已在线滤过的样品溶液1mL,作为供试品溶液。
2.2 HPLC方法
以SPOLAR C18(150mm×4.6mm, 5μm)为色谱柱;以甲醇-水(20:80)为流动相,流速为1.0mL/min,柱温为35℃;检测波长为320nm。取甲硝唑对照品适量,精密称定,加溶出介质溶解并定量稀释制成分别约含0.006、0.015和0.03mg/mL的溶液,作为相应方法的对照品溶液。分别精密量取供试品溶液和浓度对照品溶液各20μL,注入液相色谱仪,记录色谱图,按外标法以峰面积计算。
2.3 方法学验证
甲硝唑在3.012~50.20μg/mL范围内线性良好(r=0.9999),线性方程为:Y=62.99X-5.561。分别取浓度为6.024、15.06和30.12μg/mL的对照品溶液,分别重复测定6次,RSD均小于0.1%。精密量取各方法下300min时间点供试品溶液适量,分别加入相当于甲硝唑已知浓度30%、50%和100%的对照品溶液依法进行测定,结果回收率为99.0%~99.8%。供试品溶液在24h内稳定。
2.4 释放度结果
采用所建流通池法和篮法与YBH03122014中采用的小杯法共3种方法分别对两个厂家的甲硝唑口颊片的释放度进行测定,计算累积释放百分率,结果见表1。
2.5 释放度数据分析
采用相似因子法对相同装置不同厂家的f2因子进行比较,结果采用新建立的流通池法和篮法测得两厂家样品的释放曲线的f2因子分别为27和29,原标准采用的小杯法测得两厂家的释放曲线的f2因子为45,在3种方法下,两厂家的样品均不相似。
采用多个模型对数据进行拟合,最终采用拟合效果最优的Weibull模型(r>0.999)得到溶出参数,比较达到重要溶出率所需要的时间T25、T50、Td和T80(药物溶出25%、50%、63.2%和80%所需的时间),结果见表2。在不同方法下,分别将两厂家样品的各特征溶出参数进行统计学分析,结果A厂样品在篮法和流通池法下所得的溶出参数无显著性差异(P>0.05),B厂样品在3种方法下,两两方法间的溶出参数均存在显著性差异(P<0.01)。
3 讨论
3.1 释放度条件优化
本研究对药品的放置方式进行考察,分别采用平放在玻璃珠面上和使用片夹两种方式进行试验,结果两种放置方式结果无差异。在进行B厂样品的研究过程中,曾采用孔径为0.7μm的Whatman GF/F玻璃纤维滤膜置于在线的过滤器,结果因为过滤器处压力过高,流通池法有明显漏液,篮法第一个时间点未取到供试品溶液。换成2.7μm的Whatman GF/D玻璃纤维滤膜,两问题均得到解决。A厂样品因其未崩散,未发现上述问题。
3.2 释药状态与处方分析
本研究在试验过程中发现,A厂样品在3种装置下,药片均渐渐溶胀,释放试验结束时药片呈半透明的溶胀状态;B厂样品在各装置下,药片约1h全部崩解。将两厂家样品的辅料进行对比,A厂使用的辅料中有羟丙甲纤维素,其在冷水中溶胀成澄清或微浑浊的胶体溶液,该辅料的加入可能与该厂家样品最终呈半透明的溶胀状态有关。在3种不同释放度检查方法下,A厂样品所得的到释放数据极其相似,而B厂样品所得数据则差异较大,这可能与两厂家的处方不同有关,是否还与两厂家的工艺有关,还需要进一步的研究。另外,甲硝唑口颊片治疗口腔疾病发挥的是局部作用,如果药品迅速崩解,其停留在口腔的时间将会缩短,不利于其局部作用的发挥,且笔者曾研究市售两厂家的甲硝唑口腔黏贴片(因规格和名称不同,处方差异大,未在本文中进行对比),实验结束仍保持半透明的溶胀状态,建议B厂对其产品的处方和工艺进行优化。

表1 两厂家样品不同溶出方法下的累积释放百分率(%, n=6)Tab.1 Cumulative release percentages of samples from two manufacturers with different test methods (%, n=6)
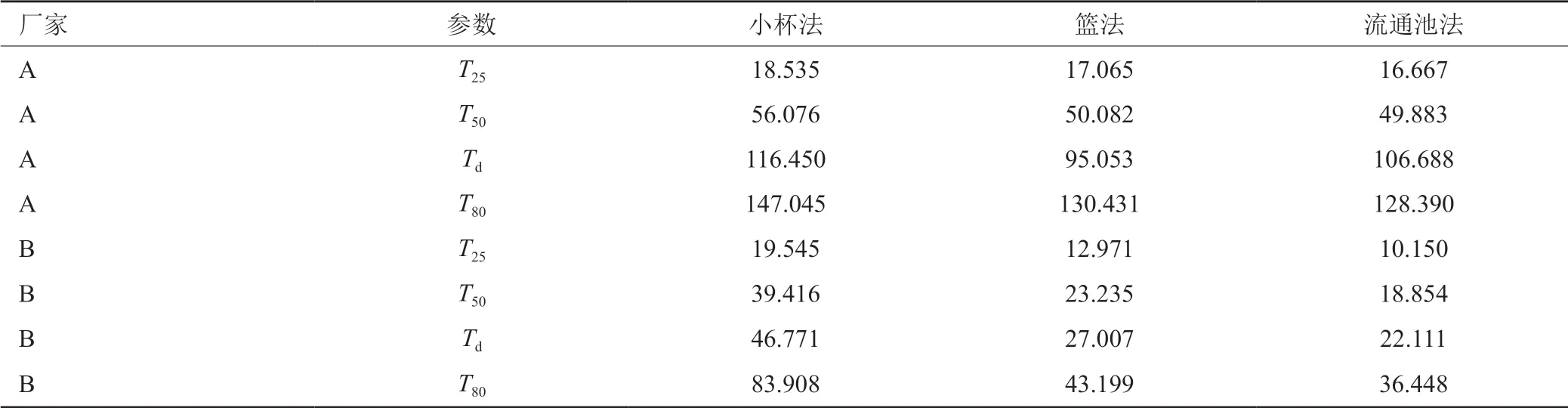
表2 各厂家样品不同方法的威布尔参数计算结果Tab.2 Weibull parameters of metronidazolebuccal tablets
3.3 本品种下流通池法与篮法比较
新建立的流通池法和篮法测得两厂家样品的释放曲线的f2因子非常接近(分别为27和29,释放曲线均不相似),两方法均可用于甲硝唑口颊片的释放度检查。释放度实验结束后,两厂药品呈现不同的状态,A厂药品不崩散,B厂药品崩散,在篮法和流通池法下所得的释放参数中,A厂药品无显著性差异,B厂药品存在显著性差异。由此可初步得出,篮法和流通池法均可用于A厂样品的释放度检查,是否可适用于所有不崩散的药品,还需要对不崩散的不同品种药品进行进一步研究。由于流通池法溶出度仪的价格昂贵(是普通溶出仪的几倍甚至10倍),如果能得出对某一类制剂(如非崩散型制剂)进行释放度检查,流通池法与传统方法(如篮法)能得出相似溶出参数的推论,可节约资源,降低厂家的生产成本。
3.4 关于甲硝唑口腔贴片的建议
中国药典2015年版四部制剂通则中对口腔贴片的描述是黏贴于口腔,经黏膜吸收后起局部或全身作用的片剂[12]。而我国批准的以甲硝唑为单一原料药局部用于牙龈炎、牙周炎、冠周炎及口腔溃疡的片剂通用名为甲硝唑口腔黏贴片(有甲、乙两个公司药品)和甲硝唑口颊片(有A、B两个厂家药品)。其中甲硝唑口腔黏贴片的药品特征为规格5mg,药片小而薄(片重约0.04g),药片释放度实验结束后不崩散,甲硝唑口颊片的药品特征为规格3mg,药片大而厚(片重约0.5g),药片释放度实验结束后A厂药品不崩散,B厂药品崩散。两通用名下相应药品的处方差异大,主要是辅料种类和用量差别大,释放行为差异大(主要是甲硝唑口颊片两厂家产品间的差异),但二者均为甲硝唑口腔贴片,适应症与用法均相同。建议相关部门规范该类药品的通用名,建议统一为甲硝唑口腔贴片,与药典制剂通则一致,有助于研究者对该类药品的质量标准进行优化,同时节约了药品流通及管理过程的资源。同时建议药品的生产厂家及时对药品的处方和工艺进行优化,找出影响产品质量的关键参数,进行深入研究,提升自身药品的质量,确保药品质量的可靠性和稳定性,以提升药品质量来增加产品的市场竞争力。

