直肠癌放射治疗中快速自动计划设计的可行性研究
张海英,陈元华,朱 骥,李桂超,胡伟刚,彭佳元
复旦大学附属肿瘤医院放射治疗中心,复旦大学上海医学院肿瘤学系,上海 200032
直肠癌是常见的消化道肿瘤之一[1]。放射治疗是直肠癌的常规治疗手段之一[2-5]。现有的放射治疗计划设计系统(treatment planning system,TPS)能够进行调强适形放疗(intensitymodulated radiotherapy,IMRT)计划设计,帮助计划设计者优化剂量分布,使其与靶区适形并保护正常组织。在IMRT治疗中,治疗计划质量对放疗的潜在疗效有直接影响,且计划质量高度依赖于设计者的经验水平。此外,传统IMRT计划设计优化是一个反复优化迭代的过程,较为耗时。
为提高计划设计效率,并使计划质量保持在较高水平,自动计划设计技术应运而生,目前已发展出几大分支[6]:一种是基于脚本语言的自动计划设计技术;另一种是基于知识的自动计划设计技术。在以上的自动计划方法中,计划设计者仍然需要通过耗时的优化过程才能达成目标。而对于复杂病例,迭代优化过程中还需反复试错,才能找到可行方案。
如何才能突破放射治疗中IMRT计划设计效率的瓶颈呢?在自适应放射治疗领域,当患者在不同的治疗分次中,体内解剖结构(尤其是肿瘤靶区形状)发生变化时,会通过自适应技术调整治疗计划,使调整后的治疗计划更加适用于当前状态的患者解剖结构。传统的自适应方法可以由计划设计者针对患者变化的解剖结构进行人工二次计划设计。当患者解剖结构未发生根本性变化时,研究人员通过使用基于射野形变的自动计划设计技术来快速调整之前的放疗计划[7],使剂量分布与当前分次的靶区更加适形。
受自适应放射治疗中射野形变技术的启发,我们开发了快速自动计划(quick auto-planning,QAP)系统,并将其运用于不同直肠癌患者的IMRT计划设计中。通过新的快速射野形变算法与射野权重计算方法,研究以下可行性:将直肠癌的调强放射治疗计划设计时间缩短到10 s以内;快速自动计划设计的计划质量接近于模板计划质量和人工计划质量。
1 材料和方法
1.1 QAP方法
QAP算法流程见图1,主要包含以下步骤。
1.1.1 3D靶区投影得到2D轮廓
一般来说,3D靶区就是计划靶区体积(planning target volume,PTV)。模板计划是一个临床已接受的用于实际治疗的典型治疗计划样本,目标计划是新患者待设计计划。目标计划的射野分布继承于模板计划的射野分布。对于所有射野方向,PTV被投影至等中心平面以获得在该射野方向视观内的2D PTV轮廓。等中心平面为穿过等中心点,正交于射野中心轴的平面。因为射野一般仅限于PTV区域,所以不需要考虑PTV外其他结构。
1.1.2 模板PTV轮廓与目标PTV轮廓的边界分析
将模板PTV轮廓S与目标PTV轮廓S’的质心对齐之后,通过边界分析将S映射到S’。该步骤在极坐标下进行,将模板轮廓S和目标轮廓S’分别描述为R=S(θ)与R’=S’(θ),模板轮廓函数S与半径R和角度θ相关,而目标轮廓函数S’与半径R’和角度θ相关。如果形变函数为V(θ),则得到下式:

那么,形变函数为:
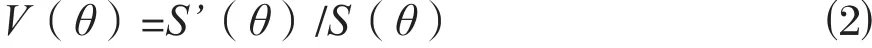
1.1.3 射野开口形变
将模板计划射野开口F与目标计划射野开口F’分别描述为R=F(θ)与R'=F'(θ),模板计划射野开口函数F与半径R、角度θ相关,目标计划射野开口函数F’与半径R’、角度θ相关。由式⑵得到形变函数V(θ)之后,目标计划射野开口F’,可通过模板计划射野开口F由下式得到:
对所有射野方向的所有子野都进行射野开口形变。
1.1.4 射野权重计算
由于目标患者肿瘤位置及其尺寸可能与模板患者不同,需要重新计算目标计划的剂量权重,使目标计划各射野贡献于参考点(等中心点)的剂量与模板计划相同。
对于等中心照射技术,等中心的点剂量(point dose,PD)由式⑷、⑸得到[8]:

下标s与t分别表示模板计划射野与目标计划射野,MU为计划的总跳数,W为射野权重,TMR为组织最大剂量比,OF是校准距离为SCD的输出因子,SAD因子等于(SCD/SAD)2。使:

可以得到:
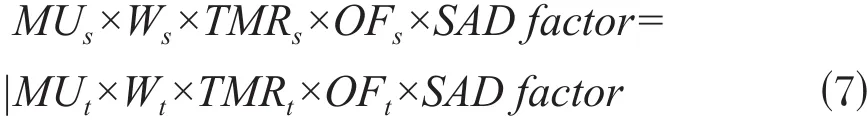
因此,目标计划射野权重可由下式得到:

根据式⑻,目标计划所有射野的总权重为:
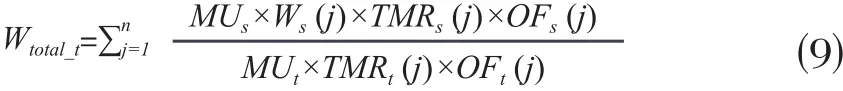
其中,j为射野编号,n为射野总数。最后,将式⑻中的射野权重Wt归一到式⑼中的总射野权重Wtotal_t。目标计划各射野的最终射野权重为:
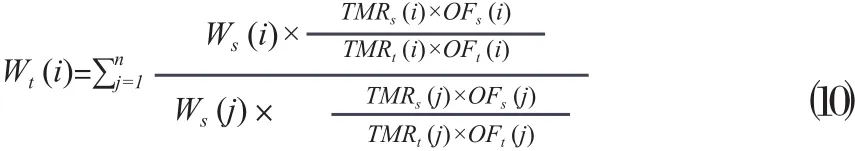
其中,i也为射野编号。
最后,目标计划由得到的射野开口和对应的射野权重组合而生成。所有步骤均由自制的基于MATLAB(美国MathWorks公司产品)环境开发的QAP系统执行。最后再将计划导回Pinnacle TPS,借助剂量计算引擎,完成剂量计算和剂量评价。

图 1 QAP算法流程图Fig. 1 The work fl ow of the methodology of the QAP algorithm
1.2 可行性分析
本研究选取了9例直肠癌患者对QAP技术进行可行性验证。处方剂量为50 Gy(2 Gy/次)的等剂量线至少覆盖95%的PTV。1号患者的IMRT计划在Pinnacle TPS(荷兰Philips公司产品)上设计完成,在Elekta Synergy VMAT加速器(瑞典Elekta公司产品)上执行,该计划共包含7个共面6 MV光子射野。将该计划作为模板计划样本,通过QAP系统为其他8例目标患者生成QAP计划。为比较QAP计划与人工计划的质量,8例目标患者由剂量师完成人工计划设计,用于随后的QAP计划与人工计划之间的比较。
对于QAP计划设计,首先将模板计划与目标计划的PTV导入QAP系统,然后将模板计划信息(包括射野角度、射野中心、射野形状及剂量权重等)导入QAP系统。通过上述射野形变和权重计算算法,生成QAP计划。最后将新生成的8例目标患者的计划回传至Pinnacle TPS,借助剂量计算引擎来进行最终的剂量计算与剂量评价。
在剂量评价中,靶区的评价指标为D1%、D99%、Dmean、均匀指数(homogeneity index,HI)和适形指数(conformity index,CI)。HI=(D2%-D98%)/Dp,CI=VRI/TV,其中Dx%为x%靶区体积接受的剂量,Dp为处方剂量,VRI为处方剂量线所包裹的体积,TV为靶区体积。HI值越小,说明靶区内剂量越均匀;CI越接近于1,说明适形性越好。对于正常组织,膀胱,左右股骨头的评价指标为Dmean。
QAP计划与人工计划各项剂量评价指标,通过SPSS 22.0软件,采用配对t检验进行统计分析,P<0.05为差异有统计学意义。
2 结 果
2.1 QAP效率评估
QAP系统在MacBook Pro笔记本电脑上运行,该电脑硬件配置为:2.8 GHz Intel Core i7 处理器,10 GB 1 222 MHz DDR3内存和1块固态硬盘。8例目标计划的计算时间均小于6 s(不包括靶区文件和计划文件的读取时间)。相比于人工计划设计用时(平均1 h),QAP计划所用时间明显缩短,显著提高了计划设计的效率。
2.2 QAP计划质量评估
表1为模板计划、QAP计划、人工计划的靶区剂量和正常组织剂量统计。通过比较模板计划和QAP计划的剂量指标发现,QAP计划的PTV D99%略小于模板计划,PTV D1%略大于模板计划。QAP计划在膀胱与左股骨头的Dmean上略大于模板计划,右股骨头Dmean略小于模板计划。
通过对比QAP计划与人工计划的靶区和正常组织剂量指标发现,QAP计划的PTV D99%略小于人工计划,PTV D1%略大于人工计划。对于正常组织,QAP计划在膀胱Dmean上略小于人工计划;在左、右股骨头Dmean上略大于人工计划。其他剂量指标详见表1。其中V100%为靶区体积接受100%处方剂量的体积百分数。

表 1 模板计划、QAP计划、人工计划的靶区剂量和正常组织剂量统计Tab. 1 Dose statistics for PTV and organs at risk dose of the template plan, QAP plans and manual plans
PTV与正常组织(膀胱与左右两侧股骨头)在两个正交等中心层面(0°和90°)上的相对位置与体积交叠情况见图2。模板计划(图2A)与随机选取的3例QAP计划(图2B~2D),在PTV与正常组织的相对位置及体积交叠情况差异较大,是QAP计划与模板计划正常组织剂量存在差异的原因所在。
模板计划(3A)与1例QAP计划(3B)的PTV形状和剂量分布见图3。在冠状位和矢状位层面上,该QAP计划的PTV在头脚方向与模板计划存在较大差异,但QAP系统完成了从模板计划到QAP计划的形变。最终,QAP计划的100%、95%与90%等剂量线与模板计划一样,都紧紧包绕在PTV周围。虽然QAP计划的CI值略差于模板计划,但是QAP计划的剂量分布同样与PTV适形。
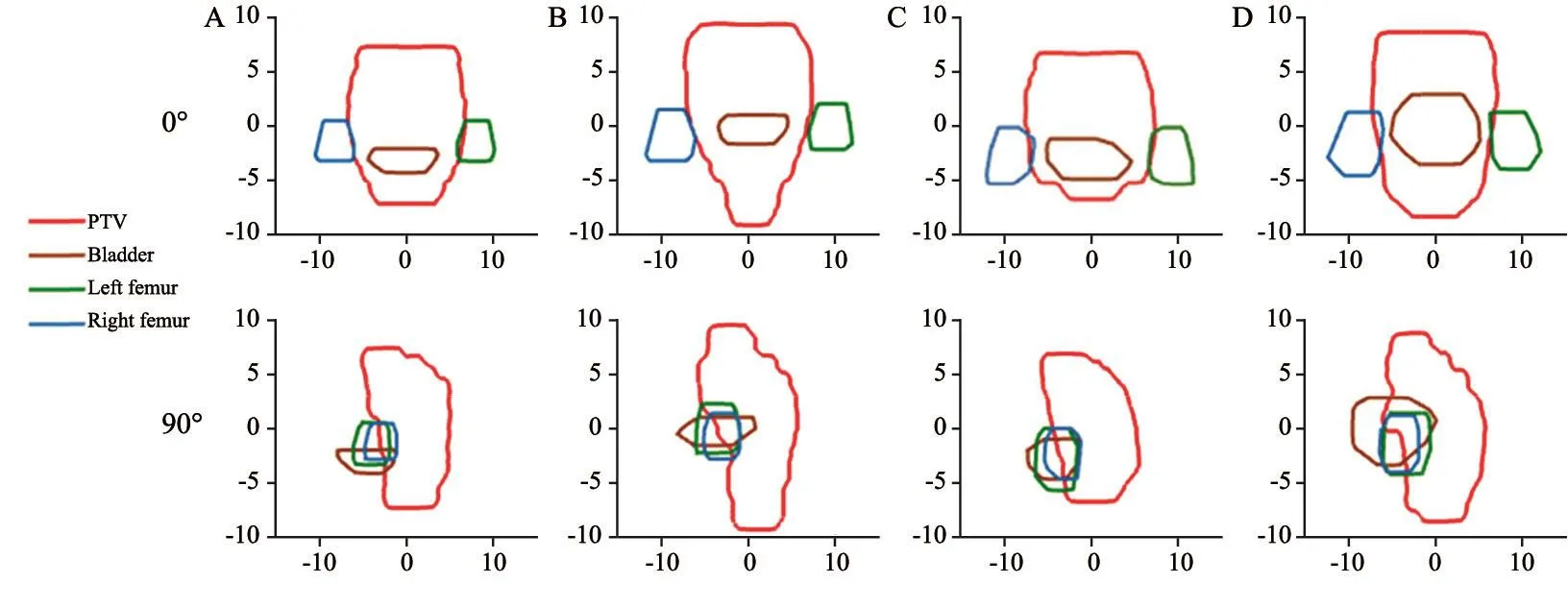
图 2 模板计划(A)和QAP计划(B~D)在0°和90°射野方向视观上PTV与正常组织的位置及交叠情况Fig. 2 PTV and organ at risk locations and overlapping in 0° and 90° BEV directions of the template plan (A) and the QAP plans (B-D)
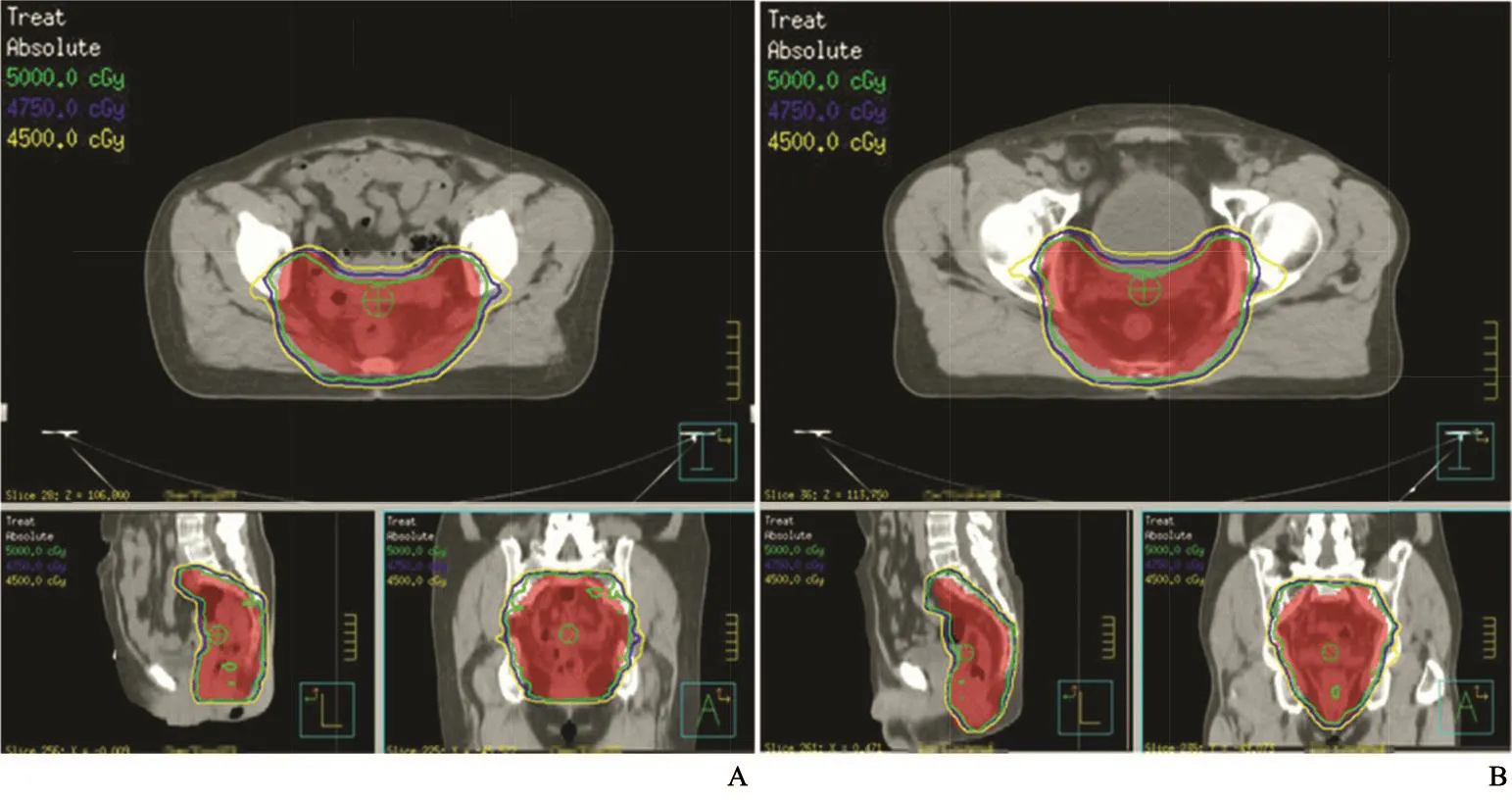
图 3 模板计划(A)与1例QAP计划(B)PTV形状和剂量线(处方剂量的100%、95%与90%)Fig. 3 PTV shape and iso-dose line (100%, 95% and 90% of the prescription dose) of the template (A) and one QAP plan (B)
3 讨 论
在本研究中,本中心自主开发了基于PTV轮廓边界分析的射野形变算法和射野权重计算方法,并将其整合到QAP系统中。此方法快速高效地完成了直肠癌的IMRT自动计划设计,虽然计划质量略低于模板计划和人工计划,但是非常接近。另外,计划设计时间从人工优化的1 h缩短到了本系统的6 s内,这使得在医师完成靶区及正常组织勾画后立刻自动生成放射治疗计划并开始进行放射治疗成为可能。
此前的射野开口形变技术主要局限于自适应放疗领域[7],用于应对治疗过程中解剖结构发生的变化,其有效性已经得到证实。在Ahunbay等[7]的方法中,笛卡尔坐标系下的射野形变向量与X及Y的位置有关。为进一步提高效率,本研究在极坐标下进行轮廓变形和射野开口形变。为更好地适用于患者间的计划生成,本研究直接使用TMR和OF计算射野权重,而不是采用Ahunbay等[7]的目标函数优化方法。
本系统可以利用其快速计划设计能力在小于6 s的时间内完成IMRT计划设计。有报道指出,肿瘤体积在放射治疗前的等待期内会发生变化[9],等待时间是放疗预后的不利因素。在计划设计期间,肿瘤体积或位置可能随时间的变化而变化,这会影响剂量评价的准确性,应尽可能减少患者等待时间[10]。本系统显著地缩短了计划设计时间,从而可以在一定程度上减少患者放射治疗前等待时间。
本研究结果表明,QAP系统可以胜任在PTV形状具有较大差异时的射野形变工作并达到接近于模板计划和人工计划的质量。然而,也观察到自动计划中正常组织与模板计划和人工计划存在差异。其原因在于:首先,目标计划中的正常组织与模板计划的正常组织位置和大小存在差异;其次,射野形变中未考虑正常组织的因素。在后续的研究中,正常组织的因素也将纳入射野形变中,以求对正常组织给予更有效的保护。
本QAP系统开发了新的射野形变技术,并将该技术在直肠癌患者IMRT计划设计中进行了可行性测试。测试结果表明该系统可显著提高直肠癌的计划设计效率,并且其计划质量接近于传统的IMRT优化技术设计的计划质量。

