体外膜肺氧合在高危经皮冠状动脉介入治疗患者中的应用
李发鹏, 张 健, 王宝珠, 刘 成, 于子翔, 孙惠萍, 杨毅宁, 马 翔
(新疆医科大学第一附属医院心脏中心, 新疆维吾尔自治区心血管病研究重点实验室, 乌鲁木齐 830054)
近年来,随着社会老龄化,冠心病发病率逐渐上升,且冠脉病变复杂严重,合并症多,使得高风险患者越来越多[1],这些高风险患者在行经皮冠状动脉介入治疗(PCI)术中易发生心室颤动、呼吸心脏骤停、心脏压塞等严重并发症。体外膜肺氧合(extracorporeal membrane oxygenation,ECMO) 来源于体外循环技术,将血液从体内引到体外,经膜式氧合器氧合,再用泵将血灌入体内。静脉-动脉-ECMO(VA-ECMO)是指将患者的静脉血通过血泵引流至体外,经过膜式氧合器后,将氧合过的血由动脉输入体内,从而建立一个简单的体外循环。VA-ECMO辅助治疗期间,可为机体提供一个短期的循环支持,保证患者血流动力学状态稳定,为进一步治疗提供条件[2]。ECMO 的优势虽然明显,但其在高风险 PCI 患者中应用的报道还很少,只有少量经验可供临床参考[3]。本研究回顾性分析新疆医科大学第一附属医院心脏中心2017年12月-2019年1月采用 ECMO支持治疗20例高危PCI患者的临床资料,现报道如下。
1 资料与方法
1.1 研究对象收集2017年12月-2019年1月采用ECMO支持治疗高危PCI患者20例,年龄为(61.2±11.17)岁,其中男性16例(80%),女性4例(20%);有吸烟病史者16例(80%);合并高血压病史者15例(75%);合并糖尿病史者8例(40%);术前发生急性心肌梗死者10例(50%);术前合并心源性休克者3例(15%);术前发生心脏骤停行心肺复苏术1例(5%);心脏超声射血分数为(54.4±9.81)%;左主干病变者14例(70%),三支病变者13例(65%),狭窄达到85%以上或次全闭塞或完全闭塞者18例(90%)(表1)。纳入标准:冠状动脉造影示冠状动脉左主干和(或)3支病变,狭窄达到85%以上,甚至完全闭塞;或同时合并超声心动图示左心室增大,射血分数( ejection fraction,EF)降低,NYHA心功能Ⅲ-Ⅳ级;或同时合并急性心肌梗死、心源性休克、频繁发作心绞痛,需药物干预或机械辅助。不能耐受或经心外科会诊评估后属于外科干预禁忌证;或患者意愿明确表示拒绝行外科手术治疗。排除标准:严重不可逆的除心脏外的器官衰竭,影响存活(如严重缺氧性脑损伤或转移性肿瘤);急性主动脉夹层;严重凝血功能障碍或存在抗凝禁忌证,如严重肝损伤;血管条件差(如严重外周动脉疾病、过度肥胖、截肢)等。

表1 20例患者一般资料
注:CA=心脏骤停;CS=心源性休克;EF=左室射血分数;AMI=急性心肌梗死;N=未见明显异常;LM=左主干;LAD=前降支;LCX=回旋支;RCX=右冠状动脉。
1.2 体外膜肺氧合应用及管理
1.2.1 采用设备及耗材 MAQUET心肺辅助系统Heart-Lung Support System CARDIOHELP System,MAQUET体外循环套包(BE-PLS 2050), MAQUET体外循环插管(BE-PAL)及穿刺附件,空氧混合器,变温水箱等。
1.2.2 ECMO插管 所有患者均采用经皮穿刺股动、静脉,并预埋2把血管缝合器,并插入动静脉置管,建立VA-ECMO。
1.2.3 ECMO管理及PCI 辅助血流量40~50 mL·kg-1·min-1,气流量2~2.5 L/min,氧浓度0.5~0.6,通过测量外周血压或PCI穿刺导管测压,维持平均动脉压(mean arterial pressure,MAP)>70 mmHg(1 mmHg = 0.133 kPa) ,水箱设置温度36.5℃,辅助期间维持体温36.0℃~37.0℃。抗凝方案按照PCI术标准执行。待患者循环稳定后立即行PCI术,术中常规间隔1 h监测ACT及血气分析,携带ECMO转运回CCU病房的患者日常监测超声评估心功能变化及患者血气情况,据此调整ECMO流量。
1.2.4 ECMO撤离 (1)小剂量血管活性药物即可维持血流动力学稳定(收缩压>90 mmHg)。(2)无致命性心律失常。(3)无酸碱平衡及电解质紊乱。(4)辅助流量减少到正常心排血量的10%~20%,一般为1~1.5 L。(5)超声心动图显示左室射血分数>40%。全部符合以上条件给予撤离ECMO。
1.3 数据收集回顾性分析ECMO支持下高危PCI患者资料,包括一般情况,冠心病危险因素,冠脉病变情况,ECMO使用时间,术前术后射血分数变化情况,住院期间MACE事件发生等。手术过程中数据包括冠脉狭窄情况,置入支架数、PCI术中并发症、ECMO并发症、存活出院率等。
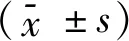
2 结果
2.1 20例患者术中情况、术后并发症及预后情况20例患者均在PCI术前置入ECMO进行辅助支持,并均采取经皮穿刺置管方式,成功行PCI术治疗,成功率为100%;ECMO辅助时间最短1.5 h,最长51 h,平均时间为10.21 h;分别置入支架1~5枚;术中3例患者发生一过性心脏骤停,余未见有室颤、呼吸心脏骤停、心脏压塞等;4例发生低血压,收缩压<90 mmHg,经抢救均好转;16例患者均在PCI术后经充分评估病情后即刻成功撤离ECMO,4例患者将ECMO带回CCU病房监护待病情稳定再次评估后成功撤离ECMO;术后1例发生肺栓塞;3例并发术区渗血;1例发生下肢动静脉血栓;20例均未发生严重出血事件及下肢缺血事件、感染事件;20例患者均存活出院(表2)。

表2 20例患者术中情况、术后并发症及预后情况
2.2 术后并发症与一般情况及合并症的相关性根据20例患者有无术后并发症,对其性别、吸烟、高血压、糖尿病、心源性休克(CS)、心脏骤停(CA)、急性心肌梗死(AMI)进行了卡方检验,结果提示术后有无并发症与是否吸烟、是否存在术前心源性休克和术前心脏骤停、是否出现术中心脏骤停和/或低血压术中并发症具有显著相关性。而术后有无并发症与性别、是否合并高血压、糖尿病、急性心肌梗死的关系无统计学意义(P>0.05)(表3)。
2.3 术后并发症与年龄、辅助时间、EF值及冠状动脉病变情况的相关性根据20例患者有无术后并发症,对其年龄、支架植入数量、ECMO辅助时间、EF值及冠状动脉病变情况进行了独立样本t检验或秩和检验,结果显示有术后并发症患者的ECMO辅助时间显著高于无术后并发症患者(P<0.05);且有术后并发症患者的右冠状动脉狭窄程度显著高于无术后并发症患者(P<0.05)。而有无术后并发症与年龄、支架植入数量、EF值及左主干、前降支、回旋支狭窄程度无显著相关性(表4)。

表3 术后并发症与一般情况及合并症的相关性/例
注:术中并发症包括术中心脏骤停和/或低血压,*P<0.05。

表4 术后并发症与年龄、ECMO辅助时间、EF值及冠状动脉病变情况的相关性
注:EF=左室射血分数;LM=左主干;LAD=前降支;LCX=回旋支;RCX=右冠状动脉。*P<0.05。
3 讨论
从1977年第一例经皮冠状动脉腔内成形术(PTCA)及1987年第一例PCI,冠心病患者PCI治疗有了突飞猛进的发展[4]。随着PCI适应证不断拓展,高危复杂冠心病患者越来越多。而这些高危复杂冠心病主要表现为高龄、存在左心室功能差、多支冠脉血管严重病变、急性心肌梗死、合并全身多脏器功能障碍。本研究中入选的20例高危复杂冠心病患者共同特点是在PCI过程中极易出现严重的血流动力学紊乱,继而在术中出现恶性心律失常、冠脉无复流、心源性休克、心脏骤停等恶性事件,造成不良后果[5]。ECMO以体外循环系统为基础,采用体外循环技术进行生命支持的一种有效的循环辅助手段,同时具有呼吸支持功能,能够快速改善失代偿期心功能不全、呼吸衰竭患者的低氧血症和循环状态。潘绪等[6]研究报道,ECMO用于危重经皮冠状动脉介入治疗,6例高危复杂冠心病患者在ECMO辅助下完成PCI术,术中患者无一例心室颤动、心包填塞以及心跳骤停等严重并发症出现。其中1例死亡,5例存活出院。为了进一步避免这些患者PCI术中发生恶性事件及提高术后生存率,本组20例患者均在PCI术前置入ECMO进行辅助支持,共有3例患者在术中发生一过性心脏骤停及低血压,若没有ECMO辅助支持,很难维持循环,且很难能够顺利的完成PCI。20例患者均成功完成PCI术,有4例患者因合并严重的心源性休克,将ECMO带回心脏重症监护室继续治疗,待病情稳定后评估后均成功撤离ECMO。16例患者待PCI术后病情稳定,严格按照ECMO撤机流程,并进行评估后在心导管室成功撤离ECMO。20例患者均好转出院。在PCI手术过程中,当指引导丝通过冠脉血管病变时、以及球囊扩张时、冠脉内斑块旋磨时、支架推送及扩张时、反复推注黏稠的造影剂时,一个临时的冠脉阻塞都有可能导致出现致命的心输出量减低或不可逆的恶性心律失常,导致手术无法进行,且患者抢救无效死亡。VA-ECMO将来自右心房的静脉血经膜肺氧合后注入动脉系统,构成体外循环。ECMO不依赖心脏节律和功能,当心脏停搏时,可给予完全循环支持,血流量可达到4~6 L/min,为进一步抢救及治疗赢得时间,降低PCI术中风险。因此本研究显示,高危复杂PCI使用ECMO辅助支持是安全可行的。此外,更为重要的是ECMO能改善急性心肌梗死后心源性休克患者的血流动力学,为急诊PCI创造条件,降低急性心肌梗死后心源性休克患者的病死率。
ECMO常见并发症有出血及血栓、感染、肢体缺血性损伤、溶血、神经系统损伤及血管破裂等。本研究中术后1例发生肺栓塞,给予调整抗凝治疗3月后复查肺CTA肺栓塞消失。3例并发术区渗血,给予压迫止血,并适当减少肝素用量,并把激活凝血时间(ACT)调整至140~160 s后均好转;1例发生下肢动静脉血栓,但无下肢缺血坏死;20例均未发生严重出血事件及下肢缺血事件、感染事件。20例患者均采取经皮穿刺置管,避免血管切开,有效避免出血及感染。常规建立下肢侧支循环防止下肢缺血性损伤。本研究中ECMO辅助时间最短1.5 h,最长51 h,平均时间10.21 h;其中16例患者辅助时间在2 h左右,辅助时间越长,并发症发生几率越大,当患者病情稳定进一步评估后,不需要辅助支持时,需尽早撤离ECMO,减少ECMO相关并发症的发生。ECMO运行期间密切关注患者及机器的各种参数,出现病情变化时给予及时处置;通过积极的监测及护理,减少各种并发症的发生,从而改善患者的预后。本研究分析比较了术后并发症与一般情况、合并症、ECMO辅助时间、EF值及冠状动脉病变情况的相关性,结果显示术后有无并发症与是否吸烟、是否存在术前心源性休克和术前心脏骤停、是否出现术中心脏骤停和/或低血压术中并发症具有显著相关性。有术后并发症患者的ECMO辅助时间显著高于无术后并发症患者(P<0.05);且有术后并发症患者的右冠状动脉狭窄程度显著高于无术后并发症患者(P<0.05),提示尤其左主干病变合并右冠状动脉全闭塞或次全闭塞的急性冠脉综合征患者无论是否出现心源性休克等并发症,应优先考虑ECMO辅助。
ECMO支持下对高危复杂冠心病患者实施PCI是安全可行的。早在30年前ECMO就被用于辅助PCI,为其提供一个稳定的血流动力学环境。但国内外目前关于ECMO用于辅助高危复杂冠心病患者PCI的相关报道较少。迄今为止,对于高危复杂冠心病患者何时使用ECMO辅助的问题,没有明确统一的适应证。且对于高危复杂PCI尚缺乏统一的定义,通过本研究入选病例,认为高危PCI需要包括以下特点:首先,患者及临床表现方面:高龄、心源性休克、急性ST段抬高型心肌梗死、心搏骤停心肺复苏后、顽固性不稳定性心绞痛、左心室射血分数低下、肾衰竭、全身多脏器衰竭。其次,冠状动脉病变复杂:唯一供血血管狭窄、慢性完全闭塞、左主干病变、分叉、钙化、扭曲、静脉桥血管病变。尤其是在应用血管活性药物或主动脉内球囊反搏(IABP)无效且血流动力学不稳定的PCI患者。

