中国成人炎症性肠病合并艰难梭菌感染处理专家共识
《现代消化及介入诊疗》杂志共识专家组
艰难梭菌是临床最常见的机会致病菌,感染率、致死率及复发感染率居高不下。炎症性肠病(inflammatory bowel disease,IBD)是艰难梭菌感染(Clostridiumdifficileinfection,CDI)的独立危险因素,近年来世界范围内IBD患者艰难梭菌感染率呈增加趋势。IBD患者感染艰难梭菌后,通常病情加重,住院时间延长。迄今为止,尚无专门针对IBD合并CDI临床处理的指南、行业标准或专家共识出台。本共识制定小组组织国内外消化领域知名专家,共同撰写中国成人炎症性肠病合并艰难梭菌感染处理专家共识,旨在为IBD合并CDI患者临床诊疗提供参考。
1 定义与流行病学
【1】炎症性肠病合并艰难梭菌感染(IBD-CDI)系指IBD腹泻患者在粪便或肠黏膜组织中检测出产毒艰难梭菌
参照中华医学会消化病学分会炎症性肠病学组“炎症性肠病诊断与治疗共识意见(2018年北京)”诊断IBD患者[1],24 h内腹泻(布里斯托分级3级及以上)3次以上[2],以及粪便或肠黏膜组织中检出艰难梭菌A或B毒素,即可诊断为IBD-CDI[3]。
【2】国内外IBD-CDI发病率呈增加趋势,加重患者病情,增加医疗负担
世界范围内IBD患者艰难梭菌感染率呈增加趋势(约5.1%~16.7%)。国外研究显示,成人克罗恩病住院患者CDI发病率为1.0%~7.7%,成人溃疡性结肠炎住院患者CDI发病率为2.8%~11.1%[4],中国的数据与之大致相当[5-8]。CDI可大大增加IBD患者短期和长期(感染5年后)死亡率、血栓形成率[9]、结肠切除率[10]、治疗失败率、复发率、医疗支出及住院时间[11]。IBD-CDI菌株核糖体分型与非IBD患者基本一致。自2002年以来,核糖体分型B1/ NAP1/ 027、078等高毒力菌株出现,曾引起国外多次爆发流行,造成极大人力、物力损失。2014年我国大陆首次在溃疡性结肠炎患者粪便标本中分离出B1/NAP1/ 027菌株,提醒临床需对该菌株引起重视[12]。
2 危险因素及临床表现
【3】IBD人群发生CDI的危险因素与普通人群大致相同,年轻IBD患者及社区获得性CDI更常见
与普通人群类似,接触CDI患者、近期住院、先前发生过CDI等均是IBD人群发生CDI的危险因素[13-16]。近期使用抗生素、类固醇类药物、英夫利昔单抗等生物制剂均是IBD患者CDI复发的危险因素[17]。IBD年轻患者及社区获得性CDI较常见。抗生素是否是IBD人群发生CDI的危险因素尚有争议[18]。少数证据表明NSAIDs和PPIs是IBD人群发生CDI的危险因素[19]。
【4】IBD-CDI临床表现不典型,与活动期IBD难区分
水样便是IBD-CDI的主要临床症状,可出现血便或脓血便等非典型特征,严重时可发生中毒性结肠炎,很难与活动期IBD区分[20]。IBD-CDI与活动期IBD的实验室检查结果也类似(如白细胞增多症、贫血及低白蛋白血症等)[21]。部分IBD-CDI病人有低热或厌食等全身表现。IBD-CDI缺乏典型结肠镜特征,伪膜少见[22]。IBD-CDI病程长,死亡率高,炎症主要累及结肠,有时累及小肠,特别是结肠切除术后以及有结肠储袋炎的患者[4]。
3 诊断
【5】临床应对IBD高危人群检测艰难梭菌
以下IBD患者应检测艰难梭菌:①所有活动期IBD住院患者;②缓解期IBD患者出现腹泻,或近期有危险因素暴露(如与CDI患者接触、胃肠手术、管饲、肠道准备等);③有严重结肠炎,无细菌学证据,需要经验性CDI治疗的IBD患者;④结肠切除造口术后出现可疑症状者;⑤老年人群、免疫力低下、糖尿病、肾功能衰竭、营养不良等患者。
【6】CDI的检测方法有多种,需综合考虑不同检测方法的敏感度、特异性、耗时、费用等因素,推荐使用两步法或三步法进行CDI诊断
CDI诊断一般通过直接检出粪便艰难梭菌毒素获得。检查方法的选择取决于它的适用性、成本、耗时、灵敏度和特异性[23-25](表 1)。

表1 艰难梭菌感染不同诊断方法比较
EIAs: 酶免疫方法;GDH: 谷氨酸脱氢酶试验; PCR:聚合酶联反应
两步法: 同步联合检测GDH和毒素EIAs试验,二者结果不一致时进行细胞培养细胞毒性试验及核酸扩增确证;三步法:首先使用GDH试验初筛,GDH阳性进行毒素EIAs试验,二者结果不一致时进行细胞培养细胞毒性试验及核酸扩增确证[26]。
【7】不推荐重复检测及对无症状携带者进行检测
研究表明,重复检测(7 d内)价值有限。无症状携带者进行CDI检测临床价值不大,除非用于流行病学研究[27]。
【8】暂不推荐生物标志物作为辅助诊断
没有足够的证据表明乳铁蛋白等生物标志物可作为辅助诊断[28-29]。
4 治疗
【9】甲硝唑和万古霉素可作为IBD-CDI的一线治疗药物,对迁延复发者推荐使用粪菌移植(fecal bacteria transplantation,FMT)治疗
目前尚缺乏IBD-CDI治疗相关循证医学证据,更多的是依靠专家的建议及临床经验[30]。IBD-CDI可分为轻、中、重及严重并发症四个等级[31]。轻度、中度初治推荐甲硝唑,重度口服万古霉素治疗[32]。有严重并发症患者(如中毒性巨结肠炎,肠穿孔等)推荐万古霉素联合静脉使用甲硝唑或外科干预[33](图 1)。
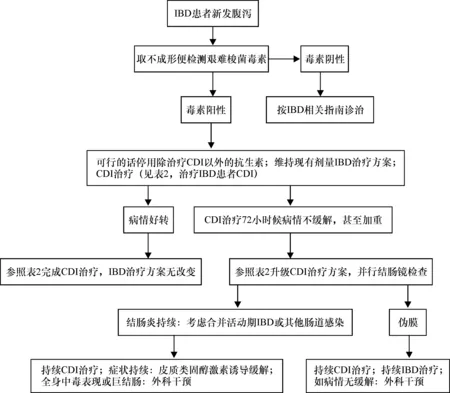
图1 IBD-CDI推荐处理流程
艰难梭菌感染复发(rCDI)是一个普遍性问题,大约1/4的甲硝唑或口服万古霉素初治患者1~3个月内复发。IBD患者CDI复发率高达39%。对于复发患者,考虑到甲硝唑的累积毒性效应,建议使用万古霉素作为常规治疗药物[34]。再次复发者可考虑万古霉素脉冲式给药,延长用药时间,也可考虑使用非达霉素(大环内酯类,2011年FDA批准上市)治疗,其疗效和毒性与万古霉素相当,但4周内复发率明显降低(15.4%vs.25.3%),然而较贵的价格限制了其广泛使用,因此常用于rCDI患者(表 2)。此外,非达霉素是否可降低IBD患者CDI复发率尚未确定[35-37]。
研究表明FMT可降低CDI复发率,但也有研究表明FMT可能加重IBD-CDI患者的炎性反应[38]。目前认为FMT对IBD患者CDI复发有一定疗效,FMT有一定的疗效,但低于非IBD患者CDI复发,且感染等并发症发生率高[39]。目前暂不推荐FMT作为CDI-IBD常规治疗方案,推荐IBD患者三次及以上CDI复发时采用FMT[40-42]。

表2 IBD-CDI治疗策略
ALB:Albumin;WBC:White blood cell; ICU:Intensive Care Unit
【10】糖皮质激素、免疫抑制剂及英夫利昔单抗等生物制剂可用于控制IBD-CDI患者炎症反应,但安全性及使用时机需进一步评估
采用糖皮质激素控制合并CDI的活动期IBD炎性反应是必要的[43],但糖皮质激素治疗时机、剂量、是否需合并使用抗生素等尚存在争议[44]。此外,仍有部分研究认为,IBD患者接受激素治疗,CDI风险增加,预后变差[45]。
IBD-CDI患者可以维持现有剂量的免疫抑制剂(甲氨蝶呤,硫唑嘌呤等)以及英夫利昔单抗等生物制剂[44]。也有研究认为免疫抑制剂和生物制剂是CDI的危险因素,因此IBD-CDI患者使用免疫抑制剂和生物制剂的安全性尚需进一步评估[4]。
5 监管及预防
IBD-CDI感染控制主要集中在抗生素的管理、阻断医院内传播、益生菌、疫苗的使用等方面。
【11】严格抗生素管理,限制广谱抗生素的使用频率、时长及剂量
①尽管抗生素是否是IBD人群发生CDI的危险因素尚有争议,仍推荐尽量减少广谱抗生素使用次数、剂量,缩短持续使用时间[38]。
②应根据当地流行病学和存在的菌株核糖体分型、耐药情况等进行有针对性的抗生素管理。可考虑限制氟喹诺酮类、克林霉素和头孢菌素的使用(外科抗生素预防除外)[46]。
【12】采用手卫生、接触隔离、环境消毒等管控措施可有效延缓甚至阻断医院内传播
接触IBD-CDI患者摘掉手套后应立即用皂液或含酒精的卫生产品进行手卫生[47]。如果接触到粪便或可能被粪便污染的区域,优先使用皂液洗手[48]。
IBD-CDI 患者应采取接触隔离措施,至少在停止腹泻的48 h后才可以结束隔离,如感染率仍高,则应延长隔离时间直至患者出院为止。对已知或怀疑为IBD-CDI的患者应安排在带有专用卫生间的独立房间。患者房间内的非一次性物品应仅用于该房间,患者使用过的物品应彻底消毒;进入已知或怀疑为IBD-CDI患者房间的医务人员或探视者应采取隔离屏障(包括手套、隔离衣)。鼓励患者勤洗手、勤淋浴,减少皮肤上的孢子。无症状携带者无需治疗及隔离[37]。
对IBD-CDI高发区域使用含氯消毒剂或其他有效杀灭芽孢的消毒剂对污染环境进行消毒,可有效减少 CDI[49-50]。
【13】不推荐使用益生菌作为预防用药
除了一些临床试验外,没有足够证据支持益生菌作为CDI的预防用药,且益生菌有潜在的血液感染可能性( 特别是对于病情严重及免疫受损的患者)。目前不推荐益生菌作为IBD-CDI的预防药物[51-52]。
【14】目前临床暂无有效的疫苗
近些年疫苗研究有一定进展,部分疫苗已经进入二、三期临床试验,但目前尚无有效疫苗上市[53]。
6 结语
抗菌药物的广泛应用,以及艰难梭菌高产毒株型的出现及传播,带来极大的医疗和社会压力。与世界发达国家或地区相比,我国对IBD-CDI临床认知不充分,实验室检测能力不足,同时缺乏有效的流行病学监测与科学研究,是一个亟待加强的领域。本共识对全球范围内该领域的进展进行回顾与综述,结合我国实际国情,期望为国内IBD-CDI的诊断、治疗、感染控制提供参考,有助于规范IBD-CDI诊疗。
共识意见牵头专家: 刘思德(南方医科大学南方医院)、房静远(上海交通大学医学院附属仁济医院)
共识意见参与专家( 按姓氏拼音排序):
白文元(河北医科大学第二医院)、白杨(南方医科大学南方医院)、陈烨(南方医科大学南方医院)、陈萦晅(上海交通大学医学院附属仁济医院)、丁元伟(广州医科大学附属第二医院)、郭红(陆军军医大学新桥医院)、何兴祥(广东药学院附属第一医院)、霍光明(杜克-新加坡国立大学医学院)、霍丽娟(山西医科大学第一医院)、李子俊(广东省人民医院)、陆红(上海交通大学医学院附属仁济医院)、苗新普(海南省人民医院)、缪应雷(昆明医科大学附属第一医院)、聂勇战(空军军医大学西京医院)、沙卫红(广东省人民医院)、田德安(华中科技大学同济医学院附属同济医院)、王芬(中南大学湘雅三医院)、王蔚虹(北京大学第一医院)、王学红(青海大学附属医院)、王玉芳(四川大学华西医院)、徐丽姝(广东省人民医院)、张建中(中国疾病预防控制中心传染病预防控制所)、张万岱(南方医科大学南方医院)、智发朝(南方医科大学南方医院)、朱宝利(中国医学科学院微生物所)、左秀丽(山东大学齐鲁医院消化内科)
执笔:王浦(南方医科大学南方医院)、王斯琪(南方医科大学南方医院)

