传统和新型制氢方法概述
陈思晗 ,张 珂 ,常丽萍 *,王 辉 ,2
(1.太原理工大学煤科学与技术省部共建国家重点实验室培育基地,山西 太原 030024;2.萨斯喀彻温大学化学和生物工程系,加拿大萨斯喀彻温 萨斯卡通S7N 5A)
能源是社会存在、经济发展的物质基础和重要动力。据国际能源署预计,到2040年全球能源需求将增长30%[1]。但目前主要使用的化石能源的开发和使用对生态环境已经产生了许多负面的影响,如大气污染、水源和土壤污染、酸雨等。绿色、清洁和高效发展是新时代发展的主题,是经济发展规律的必然要求和能源发展的必然趋势。氢能具有清洁、高效、可持续发展等特点,是21世纪最具发展潜力的清洁能源之一,是未来能源战略的关键[2]。氢能具有以下三方面的特点:(1)氢能是公认的清洁型能源之一,氢气经燃烧后只生成水,对环境没有任何污染[3],氢的热值很高,其热量相当于同质量的汽油燃烧产生热值的三倍;(2)氢能是具有可再生性的二次能源,地球上游离态的氢极少,必须从含氢的物质中制得;(3)氢气具有可储存、可输送的性质,可作为一种能源储存或运输。目前,全球的氢产量约为5000万t/a,并以6%~7%的速度逐年增长。其中商业用的氢气中有96%是从煤、石油和天然气等化石燃料制取而来。
1 化石燃料制氢
1.1 煤制氢
我国是煤炭资源相对丰富的国家。煤作为我国最主要的化石能源,占据能源结构的70%左右[4],且可预计未来很长一段时间中,煤仍是我国的主要能源。可以预计,煤制氢方法仍将是未来中国特色的制氢路线。
1.1.1 传统的煤制氢
煤的主要成分是碳,煤制氢的原理是通过利用碳取代水中的氢元素生成氢气和二氧化碳,或通过煤的焦化(或称高温干馏)和煤的气化生成氢气和其它煤气成分。煤焦化制氢是在隔绝空气条件下,使煤在900~1000℃高温下制得焦碳,该过程中所产生的气相副产物就是焦炉煤气,其中氢气含量相对较高,约占焦炉煤气的55%~60%[5];煤的气化是利用温度和压力使煤中的有机质与气化剂发生煤热解、气化和燃烧等化学反应,将固体煤转化为气体,该过程中会得到CO2、CO和H2等气态产物。一方面,直接将煤气化得到的气体产物进行净化、分离、提纯等系列处理可得到一定纯度的氢[6];另一方面,煤气中的CO可以通过水煤气变换反应(CO+H2O→CO2+H2)制取氢气;还可以利用气化煤气和热解煤气的组成特性,通过气化煤气中含量相对较高的CO2和热解煤气中含量相对较大的CH4(23%~27%)进行重整反应(CO2+CH4→2CO+2H2)制取氢气。传统煤制氢法工艺成熟,但仍不可避免产生大量的气相污染物,水煤气变换也存在水资源浪费的现象。而CH4和CO2重整制取氢气的方法作为双气头煤基多联产工艺的关键技术[7],是具有应用前景的方法之一。科研工作者在传统煤制氢的基础上,也进行了以煤为原料制氢的其它方法的研究。
1.1.2 煤浆电解制氢
1979 年, Coughlin[8]和 Farooque[9]提 出 煤 浆 电解制氢,该技术使煤炭的清洁利用和生产氢气相结合的愿望得以实现。与传统的水电解相比,煤浆电解制氢过程中所需的最小电压仅为0.21V[10],远小于水电解所需的电压1.23V。煤浆电解反应如下:
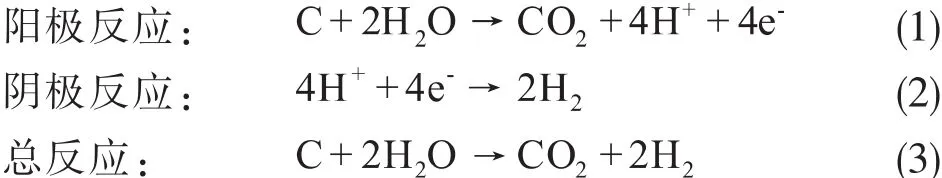
煤浆电解制氢过程在动力学上不利,以铂作为催化剂可有效催化该反应,但贵金属铂由于其高成本不适合大规模工业应用。为减少催化剂带来的高成本,采用与金属铂性质相似的金属钯负载于碳纤维上作为煤浆电解制氢的催化剂。Yu等[11]开发了新型负载在碳纤维上的Pd-Co纳米电催化剂(PdCo/CFs),并且首先应用于煤浆电解制氢。与纯Pd/CFs催化剂相比,PdCo/CFs电催化性能改善了约16.9%,是用于煤浆电解制氢中较有前途的阳极催化剂。
1.1.3 煤炭超临界水气化制氢
煤炭超临界水气化制氢技术是由西安交通大学动力工程多相流国家重点实验室提出[12-13]。该法利用超临界水的性质,在煤气化过程中以超临界水为媒介,使煤中的碳和氢元素转化为H2和CO2,并将水中的部分氢元素转化为H2。如图1所示[14],当物料通过量为2000 t/d时,氢气生产成本为0.111美元/Nm3。
煤炭超临界水气化制氢具有以下几方面优点:1)氢气产量高。反应生成氢气所需的氢元素不仅来自于煤中,还有一部分是源于作为媒介的超临界水中。该法使蒸汽重整反应和水煤气变换反应在同一个反应器中进行,因此气体产物中的氢气收率和质量分数高于传统气化工艺中的氢气收率和质量分数。2)超临界水的性质使有机煤质中的氮和硫等元素以无机盐的形式沉积,避免了污染物的排放。3)工业上利用氢气(如氨合成,甲醇生产和石化工业)所需压力往往高于气化炉出口的压力,若对氢气进行再压缩需要消耗能量,煤超临界水气化技术可以提供约25MPa的高压氢气。

图1 超临界水气化在不同处理规模下的氢气生产成本
1.2 天然气制氢
天然气是十分重要的气态化石燃料,与煤制氢方法相比,天然气制氢投资低,温室气体二氧化碳排放量少[15]。
1.2.1 传统天然气制氢
传统的天然气制氢工业是天然气蒸汽重整制氢,自1926年首次应用至今,经过持续的工艺改进,是目前工业上天然气制氢应用最广的方法[16]。采用列管式固定床反应器[17]。在制氢过程中主要发生的反应如下:
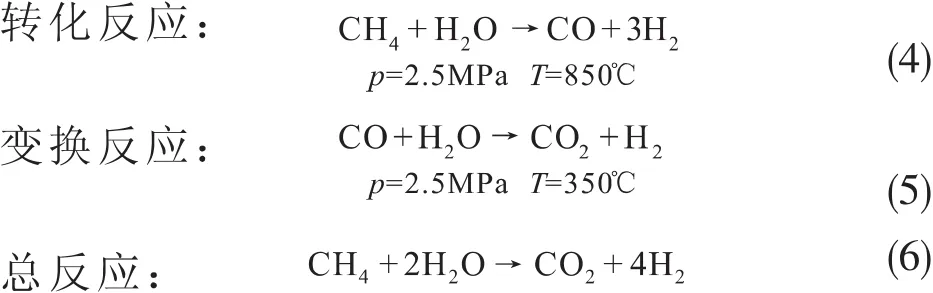
该制氢过程的总反应为吸热反应,反应原料为天然气和水,其中天然气是反应物原料也是燃料。整个制氢过程工艺流程如图2所示[18]。原料天然气进行增压至 2.5MPa,预热至 360~380℃,再对其进行脱硫处理。将经脱硫处理后的天然气与去离子水加热生成的工艺蒸汽相混合,经反应(4)、(5)得到氢气。氢气经提纯可达到99.9%的纯度,生成的H2压力约1.6MPa。天然气蒸汽重整制氢过程中需要吸收大量的热使制氢过程能耗升高,燃料成本占生产成本的 52%~68%[19]。
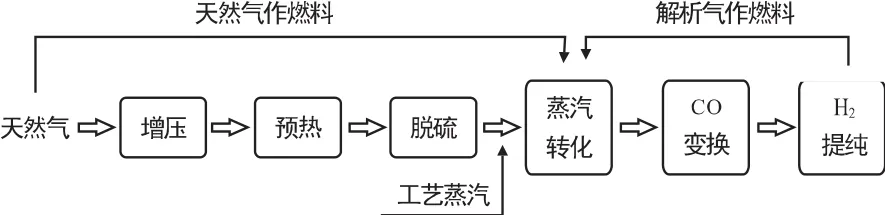
图2 天然气蒸汽重整制氢工艺流程图
除了天然气水蒸汽重整制氢工艺外,大规模工业应用的工艺还有天然气部分氧化制氢和联合重整制氢工艺。
1.2.2 铁基天然气化学循环制氢
天然气生产氢气过程中会产生CO2,而CO2的分离回收需要额外的设备,不仅增加投资成本、降低氢气的生产效率,而且CO2的捕获效率较差[20]。基于化学循环的概念提出利用金属的不同氧化态氧化天然气。Chiesa等[21]研究了一种用于氢气生产的铁基化学循环重整系统,该体系中发生如下化学反应:
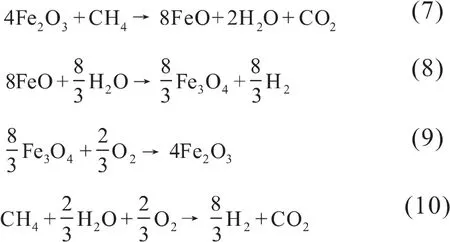
其工艺流程如图3所示。具体描述:1)在燃料反应器中,天然气通过吸热反应(7)被氧化,富氧赤铁矿Fe2O3还原为FeO。气态出口物由水和CO2组成,CO2在水冷凝后可用于地质储存。2)在蒸汽反应器中发生放热反应(8),大部分金属氧化物FeO与蒸汽反应形成Fe3O4和H2。该过程需要大量水蒸汽使金属氧化,因此气体出口蒸汽是H2和H2O的混合物。3)空气反应器中的金属氧化物Fe3O4(微量未反应的FeO)完全氧化成Fe2O3,发生反应如式(9)。该过程是高放热反应,可以维持整个系统的热平衡。贫氧空气(污染空气)从反应器排出。
利用铁基天然气化学循环制氢的总反应(10)与天然气蒸汽重整制氢相似,但该法可以通过简单的冷却和冷凝从蒸汽反应器中排出H2和水蒸汽混合物来直接产生纯的和加压的氢,并且在该过程不需要额外的气体处理(重整,转移)和分离过程。根据Chiesa等人的计算,CO2捕获效率为100%时可实现氢气的生产效率高达77%。
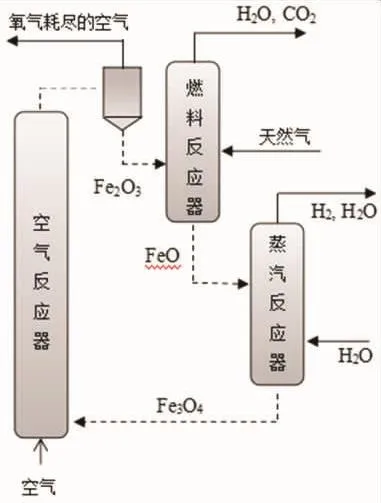
图3 铁基天然气化学循环重整制氢工艺流程图
1.2.3 天然气裂解制氢
通常的天然气制氢过程会产生温室气体CO2,对环境造成影响。寻找和实现方便、快捷、无碳排放制氢的方法成为解决能源和环境平衡的重要课题。热催化裂解甲烷技术使甲烷直接裂解生成碳和氢气(CH4(g)→C(s)+H2(g)ΔH=75.6kJ/mol),可以在生产氢气的同时实现CO2的零排放。
天然气裂解制氢有热催化裂解、等离子体裂解和熔融金属裂解等方法。
热催化裂解甲烷技术中催化剂的选择尤为重要,按其种类可分为碳质催化剂和金属催化剂。碳质催化剂耐高温、抗硫中毒性较好,且催化活性稳定,其中在热催化裂解甲烷中活性炭活性最高[22]。金属催化剂中,Ni-CeO2/SiO2可以在较低的合成温度下实现较高的甲烷转化率。经实验在580℃催化甲烷裂解,甲烷的转化率高达90%,在降低反应温度的同时实现高甲烷转化率[23]。
1.2.4 天然气联产氢气和甲酸工艺
Jorge A等[24]开发出一种天然气联产氢气和甲酸的工艺流程,该工艺过程不需要外加热量或电力来满足其能量需求,且在整个过程中不会产生温室气体CO2,实现了CO2的零排放。整个天然气联产氢气和甲酸的反应是由天然气燃烧、干重整、水煤气变换反应、甲酸甲酯合成和随后的水解生成甲酸的反应来实现的,其具体的工艺流程如图4所示。该工艺过程在常温常压下输入天然气、水和氧气作为原料,通过一系列反应可输出35.46 MPa的氢气和纯度高达99.9%的甲酸。通过运营成本分析显示,当系统的操作点选择为最大化氢气产量时,收入与成本比为8.8。
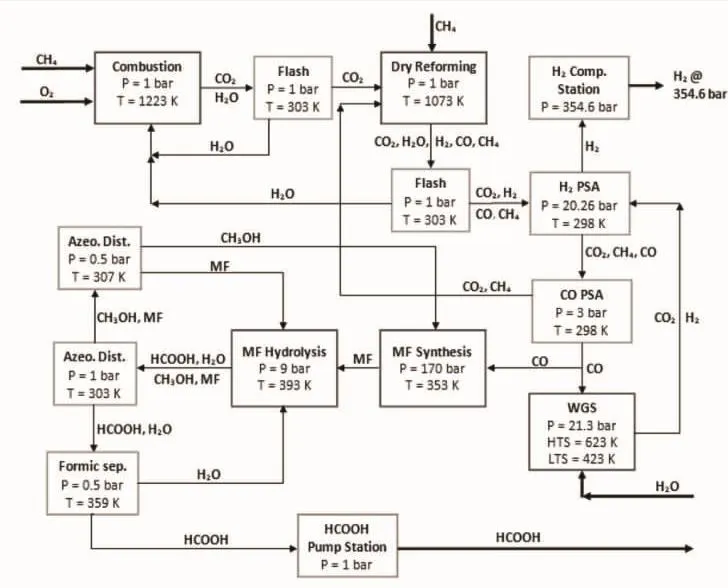
图4 天然气联产氢气和甲酸的工艺流程图
化石燃料为原料的制氢方法经济性较好,且氢气的提取率和纯度都有很高的水平,适合工业上的大规模制氢[25]。而我国由于煤炭等资源丰富,制氢原料中利用化石燃料所占的比例比世界所占比例还高。尽管化石燃料储量有限,利用化石燃料制得氢气时会对环境造成不可逆转的污染,但在研究出更为先进的制氢技术前,化石燃料制氢法作为过度的工艺,未来几十年内仍将在制氢工艺上发挥举足轻重的作用。
2 其他制氢方法
由于化石燃料不可再生,且制氢过程中产生污染,利用其他原料制氢是未来制氢方法的必然趋势。除工艺上相对成熟的化石燃料制氢法外,目前还存在具有发展前景的其它制氢方法,如:生物质制氢、水分解制氢、热化学循环制氢等。
2.1 生物质制氢
生物质制氢技术包括热化学转化法和生物法,分别通过利用热化学法或微生物将生物质 (麦秸、稻草等)通过裂解或酶催化反应制得氢气。据统计,全世界每年的生物质产量约为300亿t,但其中被用作能源的仅占4%,可用于制氢的资源潜力很大[26]。生物质热化学制氢有普通气化、热裂解和超临界水气化等方法。其中,普通气化法易产生焦油且气化率低导致制氢效率较低[27-28];热裂解法在对湿生物质脱水处理的过程耗能高[29];生物质超临界水制氢可直接对湿生物质直接处理降低干燥过程所需能耗,且具有高气化率,但仍需解决设备的堵塞和腐蚀等问题[30]。而生物法制氢技术迄今仅限于实验室研究,实验数据多数为短期结果,连续稳定运行的研究实例很少[31]。
2.2 水分解制氢
水分解制氢法的反应原料是水,而地球上的水分布广泛、资源丰富,利用该法制氢不会发生反应原料耗尽或不可再生的窘境。目前我国工业上利用水电解法生产氢气的产量占总氢气产量的4%。在电解制氢过程中的主要能耗是电能,产生1m3H2所需电费占整个电解制氢生产成本的80%左右[32]。电解制氢所需的电能需要由热能或其他形式能源转换,一般的热电转换效率只能达到30%~40%左右。这样,由一次能源变为氢能的总效率只有25%~34%左右。若利用水力资源、风力资源和太阳能资源发电与水电解制氢相结合,可以实现资源的合理利用和互补,对经济和环境都具有非常重要的意义。
科学家发现利用太阳能入射光的能量可以使水分子发生氧化还原反应而生成氢气,即光催化分解制氢。此法利用取之不尽的太阳能,潜力不可限量,但由于太阳能量密度低会直接影响光分解水制氢的效率,且在目前发现的光分解水时所用的催化剂中,大多数仅能吸收4%太阳光的紫外线,导致制氢效率较低[33]。
2.3 热化学循环制氢
热化学循环水分解制氢的概念早在1964年由科学家Funk和Reinstrom[34]提出,该法不是利用热量或电能直接使水分解产氢,而是在不同阶段和不同温度下在含有其它元素或化合物的水分解系统中,使得水经过多步骤反应后最终变为氢气和氧气。在众多热化学循环中,碘硫循环(I-S裂解水)最具发展前景,该循环流程如图5所示[35]。碘硫循环的成本低,化学过程可连续操作,在整个闭合循环中只需加入原料水。碘硫循环制氢法的预期效率可达到52%,联合制氢与发电效率可达到60%。
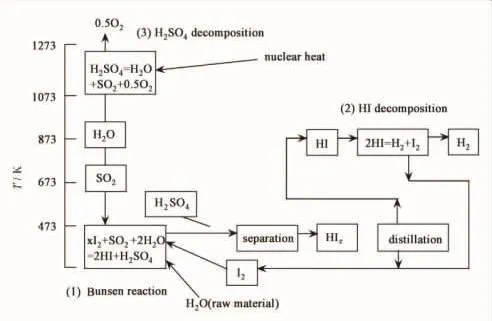
图5 热化学碘硫循环示意图
Wang[36]结合工业背景及碘硫循环多年的研究经验,提出引入硫化氢与硫酸反应(H2S+H2SO4→SO2+S+2H2O)取代需要较高温度的硫酸分解反应(H2SO4→SO2+1/2 O2+H2O),形成了硫化氢热化学裂解循环制氢的新工艺。硫化氢分解循环以硫化氢作为反应物,通过循环反应生成硫酸和氢气,使得煤炭转化利用工程中产生的含硫污染物得到资源化回收。但I-S裂解水和H2S化学裂解循环的关键步骤Bunsen反应中,水和碘需要且反应温度必须高于碘的熔点,这将导致后续过程能耗升高、效率降低、并易引起碘蒸气沉积造成的反应器堵塞等问题。利用碘-甲苯溶液作为碘源在非水体系有机溶剂内进行Bunsen反应,可以将反应温度降至室温,达到避免副反应、降低腐蚀危害,防止碘挥发和沉积,并有效分离产物与未转化反应物等良好结果[37]。
3 结语
随着世界范围内人们对环境保护的要求和对清洁能源的关注,氢气的需求量日益增加。我国制氢所用原料中化石燃料占据相当大的比例,且未来几十年化石燃料制氢法也仍将占据举足轻重的地位。提高化石燃料的制氢效率,减少化石燃料制氢过程中产生的污染是必须关注的重点。化石燃料作为一次能源储量有限,氢气生产主要原料的改变是必然趋势。

